名校
解题方法
1 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.1mol Cl2溶于水中,转移的电子数为NA |
| B.标准状况下,22.4L SO3中氧原子的数目为3NA |
C.1mol·L-1 NH4Cl溶液中, 的数目小于NA 的数目小于NA |
| D.1L pH=1的CH3COOH溶液中,H+的数目为0.1NA |
您最近一年使用:0次
2021-12-31更新
|
266次组卷
|
5卷引用:石家庄示范性高中2022届高三上学期调研考试化学试题
2021高三·全国·专题练习
解题方法
2 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温下,1 L pH=13的Ba(OH)2溶液中含有的OH-的数目为0.2NA |
| B.100 mL 1 mol·L-1AlCl3溶液中所含Al3+的数目为0.1NA |
| C.0.1 mol·L-1的CuSO4溶液中Cu2+数为0.1NA |
| D.10 g 46%的甲酸(HCOOH)水溶液中所含氧原子数为0.5NA |
您最近一年使用:0次
3 . 设 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A.标况下,224LHF中所含原子数约为 |
B.0.1molCaO2晶体中,所含阴阳离子的总数目为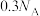 |
C.足量的S粉与1molCu完全反应,转移电子数为 |
D.2LpH=2的H3PO4溶液中所含H+总数目为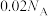 |
您最近一年使用:0次
4 . 已知含硫元素的几种物质间具有如图转化关系。 表示阿伏加德罗常数值,下列说法正确的是
表示阿伏加德罗常数值,下列说法正确的是
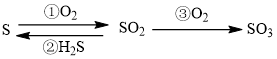
 表示阿伏加德罗常数值,下列说法正确的是
表示阿伏加德罗常数值,下列说法正确的是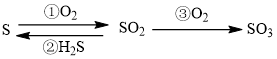
A.反应①中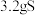 充分燃烧后生成 充分燃烧后生成 |
B.反应②中若转移 个电子,生成 个电子,生成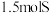 |
C. 个 个 分子与足量氧气经反应③可以制得 分子与足量氧气经反应③可以制得 个 个 分子 分子 |
D. 的二氧化硫水溶液中 的二氧化硫水溶液中 的物质的量为 的物质的量为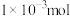 |
您最近一年使用:0次
2021-12-18更新
|
314次组卷
|
3卷引用:上海市虹口区2022届高三一模化学试题
名校
解题方法
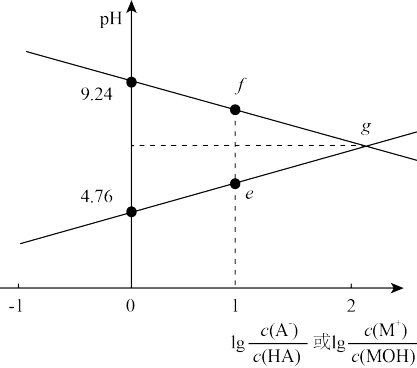
5 . 常温下,等浓度MOH碱溶液和HA酸溶液互相滴定,溶液中pH与 或
或 的关系如图所示,下列说法错误的是
的关系如图所示,下列说法错误的是
 或
或 的关系如图所示,下列说法错误的是
的关系如图所示,下列说法错误的是
A.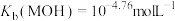 | B.水的电离程度:e=f<g |
| C.e、f点对应溶液中c(A-)相等 | D.g点酸碱恰好完全中和且溶液呈中性 |
您最近一年使用:0次
2021高三·全国·专题练习
6 . pH=13的Ba(OH)2溶液中Ba2+数目为0.1NA (____)
您最近一年使用:0次
2021高三·全国·专题练习
7 . PH=1的HCl中含有NA个Cl-。(____)
您最近一年使用:0次
8 . 从含铅烟灰(主要化学成分为PbO、Fe2O3、In2O3和In2S3)中分离回收铟和锡的工艺流程如图。
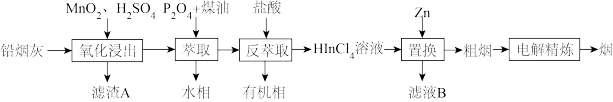
已知:①“萃取”时发生反应:In3++3H2A2(有机液)→In(HA2)3(有机液)+3H+;
Fe3++3H2A2(有机液) →Fe(HA2)3(有机液)+3H+
②“反萃取”时发生反应:In(HA2)3(有机液)+4HCl→3(HA2)3(有机液)+HInCl4。
回答下列问题:
(1)“浸出”过程中硫元素最终均以硫酸根的形式存在于浸出液中,请写出In2S3发生反应的化学方程式____ 。
(2)滤渣A的主要成分除含过量MnO2外,还有___ (填化学式)。
(3)“萃取”过程中的萃取剂可用H2A2表示,使In3+进入有机相,萃取过程发生的化学反应方程式为:In3++3H2A2 In(HA2)3+3H+,平衡常数为K=9.96。“萃取”过程中萃取剂和浸出液的用量比、萃取时间和萃取率(E%)的关系如表所示。“萃取”时萃取率的高低受溶液的pH影响很大,已知pH与萃取率的关系符合如下公式:lg
In(HA2)3+3H+,平衡常数为K=9.96。“萃取”过程中萃取剂和浸出液的用量比、萃取时间和萃取率(E%)的关系如表所示。“萃取”时萃取率的高低受溶液的pH影响很大,已知pH与萃取率的关系符合如下公式:lg =lgK-lg
=lgK-lg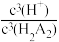 。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=___ (已知lg19=1.28,忽略萃取剂浓度的变化,结果保留三位有效数字)。
(4)盐酸的浓度与铟、铁的反萃取率的关系如图所示。则“反萃取”过程中应选择盐酸的最佳浓度为____ 。

(5)“置换”后所得浊液,需要经过过滤、洗涤、干燥等操作得到粗铟,在洗涤操作中,检验粗铟已洗涤干净的方法为___ 。
(6)电解精炼铟时阳极材料应选用____ ,随着电解的不断进行,电解液中c(In3+)会逐渐____ (“减小”或“不变”)。

已知:①“萃取”时发生反应:In3++3H2A2(有机液)→In(HA2)3(有机液)+3H+;
Fe3++3H2A2(有机液) →Fe(HA2)3(有机液)+3H+
②“反萃取”时发生反应:In(HA2)3(有机液)+4HCl→3(HA2)3(有机液)+HInCl4。
回答下列问题:
(1)“浸出”过程中硫元素最终均以硫酸根的形式存在于浸出液中,请写出In2S3发生反应的化学方程式
(2)滤渣A的主要成分除含过量MnO2外,还有
(3)“萃取”过程中的萃取剂可用H2A2表示,使In3+进入有机相,萃取过程发生的化学反应方程式为:In3++3H2A2
 In(HA2)3+3H+,平衡常数为K=9.96。“萃取”过程中萃取剂和浸出液的用量比、萃取时间和萃取率(E%)的关系如表所示。“萃取”时萃取率的高低受溶液的pH影响很大,已知pH与萃取率的关系符合如下公式:lg
In(HA2)3+3H+,平衡常数为K=9.96。“萃取”过程中萃取剂和浸出液的用量比、萃取时间和萃取率(E%)的关系如表所示。“萃取”时萃取率的高低受溶液的pH影响很大,已知pH与萃取率的关系符合如下公式:lg =lgK-lg
=lgK-lg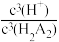 。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=(4)盐酸的浓度与铟、铁的反萃取率的关系如图所示。则“反萃取”过程中应选择盐酸的最佳浓度为

(5)“置换”后所得浊液,需要经过过滤、洗涤、干燥等操作得到粗铟,在洗涤操作中,检验粗铟已洗涤干净的方法为
(6)电解精炼铟时阳极材料应选用
您最近一年使用:0次
20-21高三下·浙江·期中
解题方法
9 . (1) Al(OH)3具有一元弱酸的性质,在水中电离时产生的含铝微粒具有正四面体结构,写出电离方程式:___________ 。
(2)人体血液里主要通过碳酸氢盐缓冲体系( )维持pH稳定。已知正常体温人体血液中,H2CO3的一级电离常数Ka1=10-6.1,
)维持pH稳定。已知正常体温人体血液中,H2CO3的一级电离常数Ka1=10-6.1, ≈
≈ ,1g2=03.由题给数据可算得正常人体血液的pH约为
,1g2=03.由题给数据可算得正常人体血液的pH约为___________ ,当过量的酸进入血液中时,血液缓冲体系中 的值将
的值将___________ (填“变大、变小、不变”)。
(2)人体血液里主要通过碳酸氢盐缓冲体系(
 )维持pH稳定。已知正常体温人体血液中,H2CO3的一级电离常数Ka1=10-6.1,
)维持pH稳定。已知正常体温人体血液中,H2CO3的一级电离常数Ka1=10-6.1, ≈
≈ ,1g2=03.由题给数据可算得正常人体血液的pH约为
,1g2=03.由题给数据可算得正常人体血液的pH约为 的值将
的值将
您最近一年使用:0次
10 . 25℃时,醋酸电离平衡常数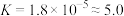 ,
,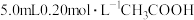 溶液与
溶液与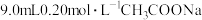 溶液混合均匀(混合后溶液体积不变)。请计算:
溶液混合均匀(混合后溶液体积不变)。请计算:
(1)求混合液的
_______ (保留2位有效数字,下同)。
(2)向混合液中加0.10mL(2滴) 盐酸,求此时溶液中
盐酸,求此时溶液中
_______  。(写出计算过程)
。(写出计算过程)
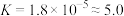 ,
,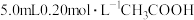 溶液与
溶液与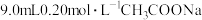 溶液混合均匀(混合后溶液体积不变)。请计算:
溶液混合均匀(混合后溶液体积不变)。请计算:(1)求混合液的

(2)向混合液中加0.10mL(2滴)
 盐酸,求此时溶液中
盐酸,求此时溶液中
 。(写出计算过程)
。(写出计算过程)
您最近一年使用:0次
2021-05-16更新
|
419次组卷
|
2卷引用:浙江省普通高中强基联盟协作体2021届高三下学期统测化学试题



