名校
解题方法
1 . 下列液体均处于25℃,有关叙述正确的是( )
| A.某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
| B.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
| C.将1L0.1mol·L-1的Ba(OH)2溶液稀释为2L,pH=12 |
| D.pH=8的NaOH溶液稀释100倍,其pH=6 |
您最近一年使用:0次
2020-02-19更新
|
129次组卷
|
2卷引用:贵州省锦屏中学2019-2020学年高二上学期期末考试化学试题
名校
2 . 设NA为阿伏伽德罗常数的值,下列叙述中不正确 的是
| A.25℃,pH=13的Ba(OH)2溶液中OH-数目为0.1NA |
| B.常温常压下,22.4L Cl2和5.6gFe充分反应转移电子数目为0.3 NA |
| C.8.0gCu2S和CuO的混合物中所含的铜原子数为0.1 NA |
| D.标准状况下,5.6L乙烷中含有的极性键数目为1.5NA |
您最近一年使用:0次
2019-03-07更新
|
245次组卷
|
2卷引用:甘肃省武威市第六中学2019届高三下学期第一次诊断考试化学试题
名校
解题方法
3 . 主族元素A、B、C、D的原子序数依次增加。甲、丙、戊是由这些元素组成的二元化合物,丙分子中原子个数比为1:1,乙是元素D的单质,通常为深红棕色液体,丁为淡黄色固体,0.01 mol/L戊溶液的pH为2,己为难溶于水、密度比水大的油状物。上述物质的转化关系如图所示。下列说法中不正确的是
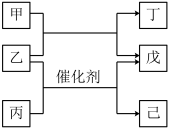

| A.四种元素既不同周期也不同主族 |
| B.元素的非金属性A<B<C |
| C.丙常温常压下为气态 |
| D.C的最高价氧化物对应的水化物为强酸 |
您最近一年使用:0次
2017-04-13更新
|
463次组卷
|
2卷引用:2017届山西省实验中学高三下学期质量检测理科综合化学试卷
解题方法
4 . 25 ℃时,pH=13的强碱溶液与0.01 mol·L-1 c(H+)的强酸溶液混合,所得混合液的pH=12,则强碱与强酸的体积比是
| A.11:1 | B.9:1 | C.1:11 | D.2:9 |
您最近一年使用:0次
名校
5 . 将100 mL 0.001 mol·L-1的盐酸和50 mL pH=3的硫酸溶液混合后,所得溶液的pH为
| A.4.5 | B.2.7 | C.3.3 | D.3 |
您最近一年使用:0次
2016-12-09更新
|
164次组卷
|
3卷引用:2015-2016学年湖北省宜昌葛洲坝中学高二上学期期中测试化学试卷
6 . 研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
2NO(g)+Cl2(g) 2ClNO(g) K2 ΔH2<0(Ⅱ)
2ClNO(g) K2 ΔH2<0(Ⅱ)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=_______ (用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后n(Cl2)=________ mol,NO的转化率α1=________ 。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2________ α1(填“>”“<”或“=”),平衡常数K2______ (填“增大”“减小”或“不变”)。若要使K2减小,可采取的措施是________ 。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH===NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1 L溶液A,溶液B为0.1 mol·L-1的CH3COONa溶液,则两溶液中c(NO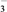 )、c(NO
)、c(NO )和c(CH3COO-)由大到小的顺序为
)和c(CH3COO-)由大到小的顺序为______________________________ 。(已知HNO2电离常数Ka=7.1×10-4mol·L-1,CH3COOH的电离常数Ka=1.7×10-5mol·L-1)可使溶液A和溶液B的pH相等的方法是________ 。
a.向溶液A中加适量水b.向溶液A中加适量NaOH
c.向溶液B中加适量水d.向溶液B中加适量NaOH
2NO2(g)+NaCl(s)
 NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)2NO(g)+Cl2(g)
 2ClNO(g) K2 ΔH2<0(Ⅱ)
2ClNO(g) K2 ΔH2<0(Ⅱ)(1)4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后n(Cl2)=
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH===NaNO3+NaNO2+H2O。含0.2 mol NaOH的水溶液与0.2 mol NO2恰好完全反应得1 L溶液A,溶液B为0.1 mol·L-1的CH3COONa溶液,则两溶液中c(NO
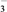 )、c(NO
)、c(NO )和c(CH3COO-)由大到小的顺序为
)和c(CH3COO-)由大到小的顺序为a.向溶液A中加适量水b.向溶液A中加适量NaOH
c.向溶液B中加适量水d.向溶液B中加适量NaOH
您最近一年使用:0次
2016-12-09更新
|
2665次组卷
|
14卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(山东卷)
2014年全国普通高等学校招生统一考试理科综合能力测试化学(山东卷)2014-2015吉林省延边二中高二12月阶段考试化学试卷2015-2016学年江西省丰城中学高二上学期期中考试化学试卷2015-2016学年浙江省东阳中学高二上学期12月阶段测化学试卷2015-2016学年江西省金溪一中高二下期中化学试卷2015-2016学年河北省邯郸一中高二下期中化学试卷2016-2017学年四川省眉山中学高二12月月考化学试卷湖北省孝感高级中学2018届高三9月摸底考试化学试题浙江省温州中学2017-2018学年高二上学期期中考试化学试题(已下线)2019高考备考二轮复习精品资料-专题9 化学反应速率与化学平衡(教学案)江西省抚州市南城县第二中学2019-2020学年高二上学期第二次月考化学试题河北省张家口市第一中学2019-2020学年高二12月月考化学试题2020届高三化学二轮冲刺新题专练——混合溶液中微粒浓度大小比较天津市耀华中学2020-2021学年高二上学期第二次段考化学试题
10-11高二上·湖北·期中
解题方法
7 . 下列有关溶液pH的说法正确的是( )
| A.将pH=11的氢氧化钠溶液加水稀释100倍,溶液中c(H+)=10-13mol/L |
| B.将pH=9的氢氧化钠溶液和pH=13的氢氧化钡溶液等体积混合,所得混合溶液的pH=11 |
| C.将pH=1的硫酸溶液和pH=5的盐酸等体积混合,所得混合溶液的pH=1.3 |
| D.pH=13的氢氧化钡溶液和pH=1的盐酸等体积混合,由于氢氧化钡过量,所得溶液的pH>7 |
您最近一年使用:0次
2016-04-15更新
|
342次组卷
|
5卷引用:2010年湖北省襄樊市四校联考-高二上学期期中考试化学卷
(已下线)2010年湖北省襄樊市四校联考-高二上学期期中考试化学卷(已下线)2011-2012学年湖北省荆州中学高二上学期期中考试化学试卷(已下线)2012-2013学年江苏省淮安市涟水县第一中学高一下期末考试化学卷2016届湖南省衡阳八中高三第一次模拟理综化学试卷广西壮族自治区贺州市桂梧高中2020-2021学年高二上学期(12月)第二次月考化学试题



