23. 阅读下列实验内容,根据题目要求回答问题。
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100mL稀H
2SO
4溶液;以0.14mol·L
-1的NaOH溶液滴定上述稀H
2SO
4 25.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)该学生用标准0.14mol·L
-1 NaOH溶液滴定硫酸的实验操作如下:
①检查滴定管是否漏水 ②取一定体积的待测液于锥形瓶中 ③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管
④装标准溶液和待测液并调整液面(记录初读数)⑤用蒸馏水洗涤玻璃仪器 ⑥把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
①滴定操作的正确顺序是(用序号填写)
___________;
②该滴定操作中应选用的指示剂是
___________;
③在⑥操作中如何确定终点?
___________。
(2)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视
___________。(3)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果
_________ (填“偏小”、“偏大”或“无影响”)
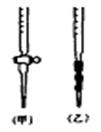
(4)用标准NaOH溶液滴定时,应将标准NaOH溶液注入
___________(选填“甲”或“乙”)中。
(5)观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的稀H
2SO
4溶液浓度测定值
___________(选填“偏大”“偏小”或“无影响”)
(6)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度(计算结果到小数点后二位)
___________。