19. 二甲醚是一种重要的清洁燃料。合成二甲醚是解决能源危机的研究方向之一。
(1)用CO
2和H
2可以合成二甲醚(CH
3OCH
3)
已知:



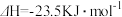
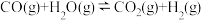

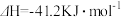
则反应
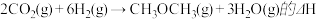
=
__________(2)已知在一定温度下,以下三个反应的平衡常数为k
1、k
2、k
3:
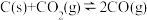
k
1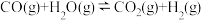
k
2
k
3则k
1、k
2、k
3之间的关系是
_____________(3)二甲醚(CH
3OCH
3)燃料电池可以提升能量利用率。利用二甲醚酸性介质燃料电池电解100mL 1mol
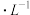
的食盐水(惰性电极),电解一段时间后,收集到标况下的氢气2.24L(设电解后溶液体积不变)
①二甲醚燃料电池的负极反应式为
_____________。
②电解后溶液的PH=
_________________________(4)工业合成氨的反应为:
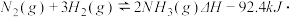
mol
-1已知合成氨反应在某温度下2L的密闭绝热容器中进行,测得数据如下表:
| 不同时间各物质的量/mol |
0 min | 1 min | 2 min | 3 min | 4 min |

| 1.50 | 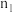
| 1.20 | 
| 1.00 |

| 4.50 | 4.20 | 3.60 | 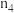
| 3.00 |

| 0.00 | 0.20 | 
| 1.00 | 1.00 |
根据表中数据计算:
①0 min~1 min内N
2的平均反应速率为
_________②该条件下反应的平衡常数k=
________(保留两位小数)
③反应达到平衡后,若往平衡体系中再加入N
2、H
2、NH
3各1mol,化学平衡向
_______(填“正向”、“逆向”或“不移动”),该反应的平衡常数k
___________(填“变大”“减小”或“不变”)
(5)常温下,将0.2mol
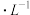
HCOOH和0.1mol
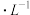
NaOH溶液等体积混合,所得溶液的PH<7,说明HCOOH的电离程度
____________HCOONa的水解程度(填“大于”或“小于”)。该溶液中[HCOOH]-[OH
-]+[H
+]=
______mol