16. 高炉废渣在循环利用前.需要脱硫(硫元素主要存在形式为S
2-,少量为SO
32-和SO
42-)处理。
(1)高温“两段法”氧化脱硫。第一阶段在空气中相关热化学方程式如下:
CaS(s)+2O
2(g)= CaS0
4(s) △H=-907.1kJmol
-1CaS(s)+3/2O
2(g)= CaO(s)+SO
2(g) △H=-454.3kJmol
-1①第二阶段在惰性气体中,反应CaS(s)+3CaS0
4(s)=4CaO(s)+4SO
2(g)的△H=
________kJmol
-1。
②整个过程中,CaS完全转化生成1molS0
2,转移的电子数为
_________mol。
③生成的S0
2用硫酸铜溶液吸收电解氧化,总反应为CuS0
4+S0
2+2H
20
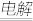
Cu+2H
2S0
4。写出电解时阳极的电极反应式
__________。
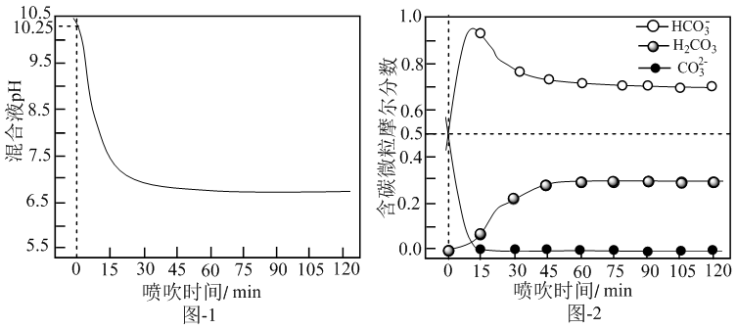
(2)喷吹C0
2脱硫。用水浸取炉渣,通入适量的C0
2,将硫元素以含硫气体形式脱去。当 C0
2的流量、温度一定时,渣-水混合液的pH、含碳元素各种微粒(H
2C0
3、HCO
3-、 CO
32-)的分布随喷吹时间变化如图-1和图-2所示。
①已知K
sp(CdS)=8.0×l0
-27,K
sp(CdCO
3)=4.0×l0
-12。取渣-水混合液过滤,可用如下试剂和一定浓度盐酸验证滤液中存在SO
32-。试剂的添加顺序依次为
_____________(填字母)。
a.H
2O
2 b.BaCl
2 c.CdCO
3②H
2CO
3第二步电离的电离常数为K
a2,则pK
a2=
_____________(填数值,已知pK
a2=—lgK
a2)。
③通入CO
215〜30min时,混合液中发生的主要脱硫反应离子方程式为
_____________。
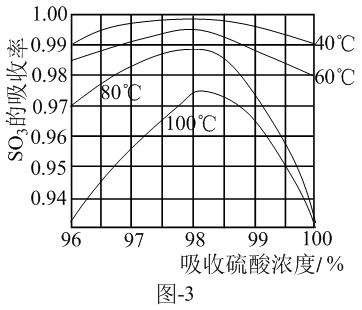
(3)硫酸工业生产中SO
3吸收率与进入吸收塔的硫酸浓度和温度关系如图-3,由图可知吸收SO
3所用硫酸的适宜浓度为98.3%,温度
_____________,而工业生产中一般采用60℃的可能原因是
_____________。