解题方法
1 . 下列实验不能达到目的的是
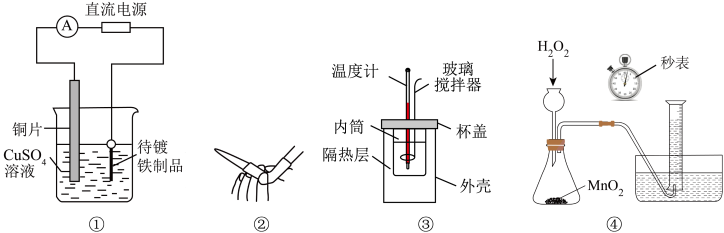
| A.①中待镀铁制品应与电源负极相连而形成铜镀层 |
| B.②中用于排出碱式滴定管中的气泡 |
| C.③中用于测定中和反应的反应热 |
D.④中测量 的分解速率 的分解速率 |
您最近半年使用:0次
解题方法
2 . 物质的性质决定用途,下列两者对应关系不正确的是
| A.液氨汽化时吸收大量的热,工业上可用作制冷剂 |
| B.锌具有还原性和导电性,所以可用作锌锰干电池的负极材料 |
C. 溶液呈酸性,可作为覆铜板制作印刷电路板的腐蚀液 溶液呈酸性,可作为覆铜板制作印刷电路板的腐蚀液 |
| D.聚四氟乙烯具有抗酸碱、自润滑等性能,可用于制作滴定管活塞 |
您最近半年使用:0次
名校
解题方法
3 . 下列实验装置使用不正确 的是
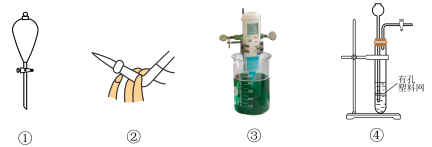
| A.图①装置可用于分离溴苯和水的混合物,且溴苯从下口放出 |
| B.可用图②方法排出碱式滴定管下端的气泡 |
| C.图③装置是用pH计测定溶液pH值,使用前pH计需洗涤和校正 |
| D.图④装置用于电石与水制取乙炔 |
您最近半年使用:0次
4 . 室温下,用0.1000mol·L−1NaOH滴定20.00mL0.1000mol·L−1HCl溶液过程中,溶液的pH随NaOH溶液体积的变化如下图所示。
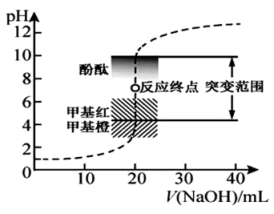
(1)酸碱式滴定管在加溶液滴定前,需要的操作是___________ 和___________ 。
(2)配制上述NaOH标准溶液时,下列仪器中不必要 用到的有___________ 。(用编号表示)。
①电子天平②烧杯③量筒④玻璃棒⑤容量瓶⑥胶头滴管⑦移液管
(3)当V(NaOH)=20.00mL时,溶液中所有离子的浓度存在的关系是___________ 。
(4)已知lg5=0.7.当加入的V(NaOH)=30.00mL时,溶液中pH=___________ 。
(5)在化学分析中,以AgNO3标准溶液滴定溶液中的Cl-时,采用K2CrO4为指示剂,利用Ag+和CrO 反应生成砖红色沉淀表示滴定终点。当溶液中的Cl-恰好完全沉淀时,溶液中的c(Ag+)=
反应生成砖红色沉淀表示滴定终点。当溶液中的Cl-恰好完全沉淀时,溶液中的c(Ag+)=___________ mol/L;c(CrO )=
)=___________ mol/L;
已知:①25℃时,Ksp(Ag2CrO4)=2.0×10-12,Ksp(AgCl)=1.8×10-10;

(1)酸碱式滴定管在加溶液滴定前,需要的操作是
(2)配制上述NaOH标准溶液时,下列仪器中
①电子天平②烧杯③量筒④玻璃棒⑤容量瓶⑥胶头滴管⑦移液管
(3)当V(NaOH)=20.00mL时,溶液中所有离子的浓度存在的关系是
(4)已知lg5=0.7.当加入的V(NaOH)=30.00mL时,溶液中pH=
(5)在化学分析中,以AgNO3标准溶液滴定溶液中的Cl-时,采用K2CrO4为指示剂,利用Ag+和CrO
 反应生成砖红色沉淀表示滴定终点。当溶液中的Cl-恰好完全沉淀时,溶液中的c(Ag+)=
反应生成砖红色沉淀表示滴定终点。当溶液中的Cl-恰好完全沉淀时,溶液中的c(Ag+)= )=
)=已知:①25℃时,Ksp(Ag2CrO4)=2.0×10-12,Ksp(AgCl)=1.8×10-10;
②当溶液中某种离子的浓度等于或小于1.0×10-5mol/L时,可认为已完全沉淀。
您最近半年使用:0次
解题方法
5 . 下列实验操作中正确的是
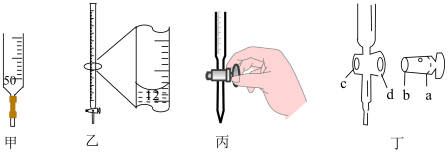

| A.量取一定体积的K2Cr2O7标准溶液可以选用图甲中滴定管 |
| B.如图乙所示,记录滴定终点读数为12.20mL |
| C.在滴定过程中,滴加酸液操作应如图丙所示 |
| D.图丁中,应将凡士林涂在旋塞的a端和旋塞套内的c端 |
您最近半年使用:0次
名校
6 . 下列实验装置使用不正确的是
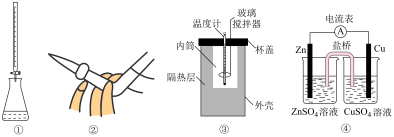

| A.图①装置用于标准酸溶液滴定未知碱溶液 |
| B.图②操作可排出盛有AgNO3溶液滴定管尖嘴内的气泡 |
| C.图③装置用于测定中和反应的反应热 |
| D.④装置盐桥中阳离子向CuSO4溶液中迁移 |
您最近半年使用:0次
解题方法
7 . 下列各仪器或装置能达到实验目的的是
 |  | 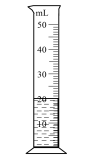 |  |
A.测定新制氯水的 | B.保存 的稀硫酸 的稀硫酸 | C.量取 的 的 溶液 溶液 | D.中和滴定 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
8 . 实验室为测定某CH3COOH的浓度,用酸式滴定管量取25.00mL醋酸溶液放入锥形瓶中,加指示剂,然后用0.1000 mol∙L-1NaOH标准溶液进行滴定。
(1)盛NaOH标准液的滴定管尖嘴部分留有气泡,排除气泡的方法应采用图中的______ 操作。(填“甲”、“乙”、“丙”、“丁”)
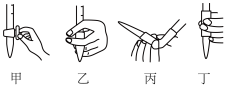
(2)指示剂应为______。
(3)滴定终点的判断方法为______ 。
(4)为提高测定的准确度,重复上述实验三次,0.1000 mol∙L-1NaOH标准溶液滴定前后的读数如表所示,则该CH3COOH的浓度为______ mol∙L-1(保留四位有效数字)。
(5)用0.1000 mol∙L-1NaOH标准溶液进行滴定,下列操作会导致测定结果偏高的是______。
(1)盛NaOH标准液的滴定管尖嘴部分留有气泡,排除气泡的方法应采用图中的

(2)指示剂应为______。
| A.甲基橙 | B.酚酞 | C.石蕊 |
(3)滴定终点的判断方法为
(4)为提高测定的准确度,重复上述实验三次,0.1000 mol∙L-1NaOH标准溶液滴定前后的读数如表所示,则该CH3COOH的浓度为
实验次数 | 醋酸溶液体积/mL | NaOH滴定前读数/mL | NaOH滴定后读数/mL |
第1次 | 25.00 | 0.10 | 24.05 |
第2次 | 25.00 | 0.50 | 23.50 |
第3次 | 25.00 | 0.20 | 24.25 |
(5)用0.1000 mol∙L-1NaOH标准溶液进行滴定,下列操作会导致测定结果偏高的是______。
| A.碱式滴定管内滴定前有气泡,滴定后气泡消失。 |
| B.读取标准液读数时,滴定前仰视,滴定到终点后俯视。 |
| C.配制0.1000 mol∙L-1 NaOH溶液时,称出的NaOH固体中含有不与酸反应的杂质。 |
| D.碱式滴定管未润洗就装入标准液进行滴定。 |
您最近半年使用:0次
名校
解题方法
9 . 实验小组用 的NaOH溶液滴定20.00mL未知浓度的
的NaOH溶液滴定20.00mL未知浓度的 溶液。下列说法正确的是
溶液。下列说法正确的是
 的NaOH溶液滴定20.00mL未知浓度的
的NaOH溶液滴定20.00mL未知浓度的 溶液。下列说法正确的是
溶液。下列说法正确的是
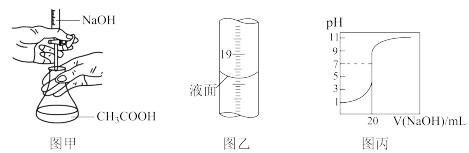
| A.可以用如图甲所示装置和操作进行滴定 |
| B.滴定结束时俯视滴定管读数,测量结果偏低 |
| C.图乙所示滴定管中液面的读数为18.20mL |
| D.图丙可以表示滴定过程中溶液的pH与滴加NaOH溶液体积的关系 |
您最近半年使用:0次
名校
解题方法
10 . 酸碱中和滴定是一种重要的实验方法。
I.某学生用 溶液测定某未知浓度的盐酸溶液;其操作可分解为如下几步:
溶液测定某未知浓度的盐酸溶液;其操作可分解为如下几步:
A.用蒸馏水洗净滴定管
B.用待测定的溶液润洗酸式滴定管
C.用酸式滴定管取稀盐酸,注入锥形瓶中,加入酚酞
D.另取锥形瓶,再重复操作2~3次
E.检查滴定管是否漏水
F.取下碱式滴定管用标准 溶液润洗后,将标准液注入碱式滴定管“0”刻度以上处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下
溶液润洗后,将标准液注入碱式滴定管“0”刻度以上处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
完成以下填空:
(1)滴定时正确操作的顺序是用序号字母填写:________ ,___→__→F→__→__→__→D。
(2)在中和滴定实验中,下列仪器只需用蒸馏水洗净,不能用待盛放液体润流的是____。
(3)若某次滴定前、滴定后盛放 溶液在滴定管中的液面位置如图。则此次滴定实验消耗
溶液在滴定管中的液面位置如图。则此次滴定实验消耗 溶液的体积为
溶液的体积为_____ mL。

(4)本次实验数据记录表:
从表中可以看出,第1次滴定记录的 溶液体积明显多于后两次
溶液体积明显多于后两次 溶液的体积,则可能的原因是______。
溶液的体积,则可能的原因是______。
Ⅱ.氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将1mL血液用蒸馏水稀释后,向其中加入足量草酸铵 晶体,反应生成
晶体,反应生成 沉淀,将沉淀用稀硫酸处理得溶液。
沉淀,将沉淀用稀硫酸处理得溶液。
②将①得到的溶液,再用酸性溶液滴定。
③终点时用去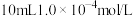 的溶液。
的溶液。
(5)写出用 滴定
滴定 的离子方程式
的离子方程式_______ 。
(6)判断滴定终点的方法是_______ 。
(7)计算:血液中含钙离子的浓度为_____  。
。
I.某学生用
 溶液测定某未知浓度的盐酸溶液;其操作可分解为如下几步:
溶液测定某未知浓度的盐酸溶液;其操作可分解为如下几步:A.用蒸馏水洗净滴定管
B.用待测定的溶液润洗酸式滴定管
C.用酸式滴定管取稀盐酸,注入锥形瓶中,加入酚酞
D.另取锥形瓶,再重复操作2~3次
E.检查滴定管是否漏水
F.取下碱式滴定管用标准
 溶液润洗后,将标准液注入碱式滴定管“0”刻度以上处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下
溶液润洗后,将标准液注入碱式滴定管“0”刻度以上处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
完成以下填空:
(1)滴定时正确操作的顺序是用序号字母填写:
(2)在中和滴定实验中,下列仪器只需用蒸馏水洗净,不能用待盛放液体润流的是____。
| A.酸式滴定管 | B.碱式滴定管 | C.移液管 | D.锥形瓶 |
(3)若某次滴定前、滴定后盛放
 溶液在滴定管中的液面位置如图。则此次滴定实验消耗
溶液在滴定管中的液面位置如图。则此次滴定实验消耗 溶液的体积为
溶液的体积为
(4)本次实验数据记录表:
| 滴定次数 | 盐酸体积(mL) |  溶液体积读数(mL) 溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 18.10 |
| 2 | 20.00 | 0.00 | 15.98 |
| 3 | 20.00 | 0.00 | 16.02 |
 溶液体积明显多于后两次
溶液体积明显多于后两次 溶液的体积,则可能的原因是______。
溶液的体积,则可能的原因是______。| A.滴定前滴定管尖嘴有气泡,滴定结束无气泡 | B.锥形瓶用水洗涤 |
C. 标准液保存时间过长,有部分变质 标准液保存时间过长,有部分变质 | D.滴定结束时,俯视读数 |
Ⅱ.氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将1mL血液用蒸馏水稀释后,向其中加入足量草酸铵
 晶体,反应生成
晶体,反应生成 沉淀,将沉淀用稀硫酸处理得溶液。
沉淀,将沉淀用稀硫酸处理得溶液。②将①得到的溶液,再用酸性溶液滴定。
③终点时用去
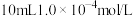 的溶液。
的溶液。(5)写出用
 滴定
滴定 的离子方程式
的离子方程式(6)判断滴定终点的方法是
(7)计算:血液中含钙离子的浓度为
 。
。
您最近半年使用:0次



