1 . 亚硝酸钠 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是A.滴定前滴定管尖嘴处有气泡,滴定后无气泡会使测得的 含量偏高 含量偏高 |
B.亚硝酸根( )空间结构为V形 )空间结构为V形 |
| C.酸性高锰酸钾溶液可以鉴别食盐和亚硝酸钠 |
D.滴定过程离子反应为: |
您最近一年使用:0次
解题方法
2 . 化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟侯氏制碱法制备NaHCO3,进一步 得到产品Na2CO3和NH4Cl两种产品,并测定碳酸钠中碳酸氢钠的含量。过程如下:
Ⅰ.NaHCO3 的制备
实验流程及实验装置图如下:
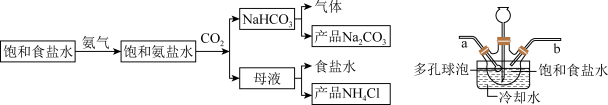
回答下列问题:
(1)a导管末端多孔球泡的作用_______ 。
(2)b中通入的气体是_______ , 写出实验室制取该气体的化学方程式_______ 。
(3)生成NaHCO3的总反应的化学方程式为_______ 。
Ⅱ.Na2CO3中NaHCO3含量测定
i.称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中:
ii.移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用0.1000mol·L-1盐酸标准溶液滴定至溶液由浅红色变无色(第一滴定终点), 消耗盐酸V1mL;
iii.在上述锥形瓶中再加入2滴指示剂N,继续用0.1000mol·L-1盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸V2mL;
iv.平行测定三次,V1 平均值为22.25,V2平均值为23.51。
回答下列问题:
(4)指示剂N为_______ , 第二滴定终点的现象是_______ 。
(5)Na2CO3中NaHCO3的质量分数为_______ ( 保留三位有效数字)。。
(6)第一滴定终点时,某同学仰视读数,其他操作均正确,则NaHCO3质量分数的计算结果_______ (填“偏大”“偏小”或“无影响”)。
Ⅰ.NaHCO3 的制备
实验流程及实验装置图如下:

回答下列问题:
(1)a导管末端多孔球泡的作用
(2)b中通入的气体是
(3)生成NaHCO3的总反应的化学方程式为
Ⅱ.Na2CO3中NaHCO3含量测定
i.称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中:
ii.移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用0.1000mol·L-1盐酸标准溶液滴定至溶液由浅红色变无色(第一滴定终点), 消耗盐酸V1mL;
iii.在上述锥形瓶中再加入2滴指示剂N,继续用0.1000mol·L-1盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸V2mL;
iv.平行测定三次,V1 平均值为22.25,V2平均值为23.51。
回答下列问题:
(4)指示剂N为
(5)Na2CO3中NaHCO3的质量分数为
(6)第一滴定终点时,某同学仰视读数,其他操作均正确,则NaHCO3质量分数的计算结果
您最近一年使用:0次
2022-05-11更新
|
543次组卷
|
5卷引用:安徽省马鞍山市2022届高三下学期第三次教学质量监测(三模) 理综化学试题
安徽省马鞍山市2022届高三下学期第三次教学质量监测(三模) 理综化学试题(已下线)专题17化学实验综合题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16化学实验综合题-2022年高考真题+模拟题汇编(全国卷)(已下线)专题17化学实验综合题-五年(2018~2022)高考真题汇编(全国卷)湖南省株洲市攸县第四中学2022-2023学年高三上学期第五次月考化学试题
名校
解题方法
3 . 下列有关中和滴定的说法正确的是( )
| A.用25 mL滴定管进行中和滴定时,用去标准液的体积为21.7 mL |
| B.用标准KOH溶液滴定未知浓度的盐酸,配制标准溶液的KOH固体中有NaOH杂质,则结果偏高 |
C.用c1 mol/L酸性高锰酸钾溶液滴定V2 mL未知浓度的H2C2O4溶液至滴定终点,用去酸性高锰酸钾溶液体积为V1 mL,则H2C2O4溶液的浓度为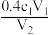 mol/L mol/L |
| D.用未知浓度的盐酸滴定已知浓度的NaOH溶液时,若读数时,滴定前仰视,滴定到终点后俯视,会导致测定结果偏高 |
您最近一年使用:0次
2020-11-22更新
|
375次组卷
|
17卷引用:合肥八中、阜阳一中2017-2018学年第一学期高二年级期末考试化学试题
合肥八中、阜阳一中2017-2018学年第一学期高二年级期末考试化学试题河北省衡水市衡水中学2018届高三第十六次模拟考试化学试题河北省定州中学2017-2018学年高二(承智班)下学期第一次月考化学试题江西省九江市同文中学2019届高三上学期期中考试化学试题山西省长治市城区第二中学校2018-2019学年高二上学期期末考试化学试题江西省上饶中学2019-2020学年高二上学期第一次月考(理科培优班)化学试题湖南省益阳市第六中学2019-2020学年高二上学期期中考试化学试题(已下线)专题8.2 水的电离和溶液的pH(练)-《2020年高考一轮复习讲练测》2020届高考化学小题狂练(全国通用版)专练15 弱电解质的电离平衡和溶液酸碱性(已下线)第26讲 水的电离和溶液的pH(精练)-2021年高考化学一轮复习讲练测(已下线)第26讲 水的电离和溶液的pH(精练)——2021年高考化学一轮复习讲练测(已下线)小题必刷31 酸碱中和滴定及拓展应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)第22讲 水的电离与溶液的pH (练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题25 水的电离和溶液的酸碱性(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)专题突破卷09 水溶液中的离子反应与平衡 ?-2024年高考化学一轮复习考点通关卷(新教材新高考)
4 . 根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 实验结论 |
| A | 用铂丝蘸取某溶液进行焰色反应,火焰呈黄色 | 溶液中无K+ |
| B | 用已知浓度HCl溶液滴定NaOH溶液,酸式滴定管用蒸馏水洗涤后,直接注入HCl溶液 | 测得c(NaOH)偏高 |
| C | 使石蜡油裂解产生的气体通入酸性KMnO4溶液,溶液褪色 | 石蜡油裂解一定生成了乙烯 |
| D | 向淀粉溶液中加入稀硫酸,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热,无砖红色沉淀出现 | 淀粉未水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
18-19高二下·浙江宁波·期中
名校
5 . 下列说法不正确 的是
| A.有机色素只要遇酸碱变色的pH值范围在滴定突跃范围内,并且变色明显,不易受空气影响的,都可以用作酸碱中和滴定的指示剂 |
| B.准确量取25.00mL的液体可选用移液管、量筒或滴定管等量具 |
| C.“中和滴定”实验中,容量瓶和锥形瓶用蒸馏水洗净后即可使用,滴定管和移液管用蒸馏水洗净后,须经干燥或润洗后方可使用 |
| D.做“食醋总酸含量的测定”实验时,先将市售食醋稀释10倍,然后用润洗后的酸式滴定管量取一定体积的稀释液于洁净的锥形瓶中 |
您最近一年使用:0次
2019-05-06更新
|
156次组卷
|
3卷引用:安徽省定远县第三中学2022-2023学年高三下学期二模化学试题
安徽省定远县第三中学2022-2023学年高三下学期二模化学试题(已下线)浙江省宁波市北仑中学2018-2019学年高二下学期期中考试化学试题浙江省宁波市北仑中学2020-2021学年高二下学期期中考试化学(1班)试题
6 . 某学习小组对某葡萄酒中SO2的含量进行检测,按下图连接好仪器。回答下列问题:
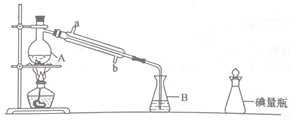
Ⅰ.样品蒸馏
取20.00mL样品和250 mL水置于仪器A中,仪器B是去掉塞子的碘量瓶,向其中装入25mL 乙酸铅溶液,然后向仪器A中加入10 mL盐酸,立即盖塞蒸馏;当碘量瓶中的液体约200 mL时,将插入碘量瓶液面下的导管向上提起并将导管置于液面上方1cm 处,再蒸馏2min左右;最后用少量蒸馏水冲洗碘量瓶中的导管,并将冲洗液并入碘量瓶中。同时做空白实验(即不加样品情况下按同法操作,防止实验误差)。
已知:SO2+H2O+Pb(CH3COO)2=PbSO3↓+2CH3COOH。
(1)仪器A 的名称是_________________ 。
(2)实验中使用的碘量瓶最适宜的规格是_________ (填标号)。
a.100 mL b.250 mL c.500 mL d.1000 mL
(3)如果实验最后未用少量蒸馏水冲洗碘量瓶中的导管,会导致测定结果__________ (填“偏高”“ 偏低”或“不影响”)。
Ⅱ.滴定操作
向取下的碘量瓶中加入10 mL盐酸和1mL淀粉溶液,摇匀后用0.01mol·L-1的碘标准溶液滴定,记录消耗的碘标准溶液的体积为V( 单位为mL)。
(4)滴定终点的现象是_____________________ ,该滴定反应的离子方程式是______________ 。
Ⅲ.结果分析
(5)甲组4 次实验测得V分别为
据此可计算此葡萄酒中SO2的含量为_______ mg·L-1
乙组认为甲组实验不严谨,可能会有误差,因为甲组未做_____________________ 。

Ⅰ.样品蒸馏
取20.00mL样品和250 mL水置于仪器A中,仪器B是去掉塞子的碘量瓶,向其中装入25mL 乙酸铅溶液,然后向仪器A中加入10 mL盐酸,立即盖塞蒸馏;当碘量瓶中的液体约200 mL时,将插入碘量瓶液面下的导管向上提起并将导管置于液面上方1cm 处,再蒸馏2min左右;最后用少量蒸馏水冲洗碘量瓶中的导管,并将冲洗液并入碘量瓶中。同时做空白实验(即不加样品情况下按同法操作,防止实验误差)。
已知:SO2+H2O+Pb(CH3COO)2=PbSO3↓+2CH3COOH。
(1)仪器A 的名称是
(2)实验中使用的碘量瓶最适宜的规格是
a.100 mL b.250 mL c.500 mL d.1000 mL
(3)如果实验最后未用少量蒸馏水冲洗碘量瓶中的导管,会导致测定结果
Ⅱ.滴定操作
向取下的碘量瓶中加入10 mL盐酸和1mL淀粉溶液,摇匀后用0.01mol·L-1的碘标准溶液滴定,记录消耗的碘标准溶液的体积为V( 单位为mL)。
(4)滴定终点的现象是
Ⅲ.结果分析
(5)甲组4 次实验测得V分别为
| 实验 | 1 | 2 | 3 | 4 |
| V/mL | 9.98 | 12.00 | 10.02 | 10.00 |
乙组认为甲组实验不严谨,可能会有误差,因为甲组未做
您最近一年使用:0次



