名校
1 . 工业废水中常含有一定量氧化性较强的 ,利用滴定原理测定
,利用滴定原理测定 含量(通常以1L废水中的微粒质量计量)的方法如下:
含量(通常以1L废水中的微粒质量计量)的方法如下:
步骤I:量取30.00mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤II:加入过量的碘化钾溶液充分反应: +6I-+14H+=2Cr3++3I2+7H2O
+6I-+14H+=2Cr3++3I2+7H2O
步骤III:向锥形瓶中滴入几滴指示剂。用滴定管量取0.1000mol/LNa2S2O3溶液进行滴定,数据记录如表:(I2+2Na2S2O3=2NaI+Na2S4O6)
(1)取Na2S2O3固体配制100mL0.1000mol/LNa2S2O3溶液需要的定量仪器有托盘天平、量筒和___________ 。
(2)步骤I量取30.00mL废水选择的仪器是___________ 。
(3)步骤III中滴加的指示剂为___________ ;滴定达到终点时的实验现象是___________ 。
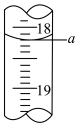
(4)步骤III中a的读数如图所示,则:___________ mL。
②计算废水中 含量为
含量为___________ g/L。
(5)以下操作会造成废水中 含量测定值偏高的是___________(填字母)。
含量测定值偏高的是___________(填字母)。
 ,利用滴定原理测定
,利用滴定原理测定 含量(通常以1L废水中的微粒质量计量)的方法如下:
含量(通常以1L废水中的微粒质量计量)的方法如下:步骤I:量取30.00mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤II:加入过量的碘化钾溶液充分反应:
 +6I-+14H+=2Cr3++3I2+7H2O
+6I-+14H+=2Cr3++3I2+7H2O步骤III:向锥形瓶中滴入几滴指示剂。用滴定管量取0.1000mol/LNa2S2O3溶液进行滴定,数据记录如表:(I2+2Na2S2O3=2NaI+Na2S4O6)
| 滴定次数 | Na2S2O3溶液起始读数/mL | Na2S2O3溶液终点读数/mL |
| 第一次 | 1.02 | 19.03 |
| 第二次 | 2.00 | 19.99 |
| 第三次 | 0.20 | a |
(2)步骤I量取30.00mL废水选择的仪器是
(3)步骤III中滴加的指示剂为
(4)步骤III中a的读数如图所示,则:
②计算废水中
 含量为
含量为(5)以下操作会造成废水中
 含量测定值偏高的是___________(填字母)。
含量测定值偏高的是___________(填字母)。| A.滴定终点读数时,俯视滴定管的刻度 |
| B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗 |
| C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 |
| D.量取Na2S2O3溶液的滴定管用蒸馏水洗后未用标准液润洗 |
您最近一年使用:0次
2023-04-29更新
|
195次组卷
|
2卷引用:四川省绵阳市南山中学2022-2023学年高二下学期期中考试化学试题



