2024高三下·全国·专题练习
1 . 某工厂采用辉铋矿(主要成分为 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制各
)联合焙烧法制各 和
和 ,工艺流程如下:
,工艺流程如下: 分解为
分解为 ,
, 转变为
转变为 ;
;
②金属活动性: ;
;
③相关金属离子形成氢氧化物的 范围如下:
范围如下:
“酸浸”中过量浓盐酸的作用为:①充分浸出 和
和 ;②
;②_______ 。
 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制各
)联合焙烧法制各 和
和 ,工艺流程如下:
,工艺流程如下: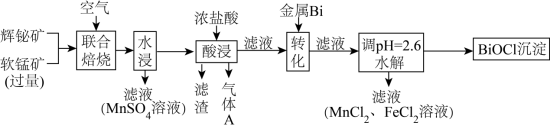
 分解为
分解为 ,
, 转变为
转变为 ;
;②金属活动性:
 ;
;③相关金属离子形成氢氧化物的
 范围如下:
范围如下:开始沉淀 | 完全沉淀 | |
 | 6.5 | 8.3 |
 | 1.6 | 2.8 |
 | 8.1 | 10.1 |
 和
和 ;②
;②
您最近一年使用:0次
名校
2 . 钛酸钡( )具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。
 )具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。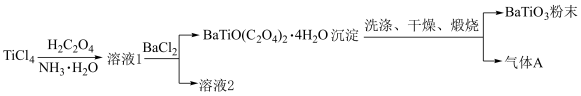
A.可用硝酸酸化的 溶液检验洗涤是否完全 溶液检验洗涤是否完全 |
| B.用溶液2提取的一种副产物可作肥料 |
| C.流程中的三步反应均为非氧化还原反应 |
D.向 中先加入 中先加入 后加入 后加入 的目的是防止 的目的是防止 水解 水解 |
您最近一年使用:0次
2023高三·全国·专题练习
名校
3 . 已知K2Cr2O7溶液中存在平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
+2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
 +H2O
+H2O 2CrO
2CrO +2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
+2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
| A.图中T1℃>T2℃ |
B.t1后溶液中有2c(Cr2O )+c(CrO )+c(CrO )=c(K+) )=c(K+) |
| C.T2℃时,上述反应的平衡常数的数量级是10-12 |
D.T1℃下,加入一定量K2Cr2O7固体后达到新平衡时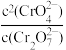 的值增大 的值增大 |
您最近一年使用:0次
2023-12-16更新
|
197次组卷
|
3卷引用:盐类的水解
2023高三·全国·专题练习
4 . 制备FeCl2:装置如图所示(加持装置省略);已知FeCl2极易水解。

(1)仪器a的名称是___________ 。
(2)装置二中制备FeCl2的化学方程式是___________ ;装置三的作用①___________ ;②___________ 。
(3)该装置存在一定的缺陷,可在___________ 位置(填“A”“B”或“C”)增加如下装置。如下装置中气体从___________ (填“a”或“b”)流入;洗气瓶中盛装的是___________ 。


(1)仪器a的名称是
(2)装置二中制备FeCl2的化学方程式是
(3)该装置存在一定的缺陷,可在

您最近一年使用:0次
2023高三·全国·专题练习
5 . 对滴有酚酞试液的CH3COONa溶液加热颜色变深。(______)
您最近一年使用:0次
名校
解题方法
6 . 常温下,向30mL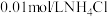 溶液中加入
溶液中加入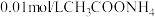 溶液,溶液的pH随加入
溶液,溶液的pH随加入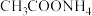 溶液的体积的变化如图。下列说法正确的是
溶液的体积的变化如图。下列说法正确的是

已知: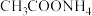 溶液的pH约为7
溶液的pH约为7
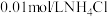 溶液中加入
溶液中加入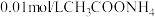 溶液,溶液的pH随加入
溶液,溶液的pH随加入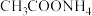 溶液的体积的变化如图。下列说法正确的是
溶液的体积的变化如图。下列说法正确的是
已知:
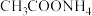 溶液的pH约为7
溶液的pH约为7A.上图说明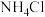 溶液中存在水解平衡 溶液中存在水解平衡 |
B.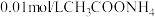 溶液中的 溶液中的 比 比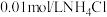 溶液中的大 溶液中的大 |
C.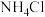 溶液中存在: 溶液中存在: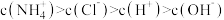 |
D.溶液的pH变化是 浓度改变造成的 浓度改变造成的 |
您最近一年使用:0次
2023-10-04更新
|
179次组卷
|
7卷引用:微专题 水溶液中函数图像的分析
名校
7 . 室温下,下列实验探究方案设计正确且能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向紫色石蕊溶液中通入过量二氧化硫,溶液先变红后褪色 | SO2为酸性氧化物且具有漂白性 |
| B | 将20℃ 0.5 mol·L-1CH3COONa溶液加热到40℃,用pH传感器测量溶液的pH | 温度对CH3COO-水解平衡的影响 |
| C | 向Na2CO3溶液中滴加浓盐酸,反应产生的气体直接通入Na2SiO3溶液中 | 非金属性:C>Si |
| D | 向浓度均为0.01mol·L-1的Na2CO3和Na2SO4的混合液中滴少量0.01mol·L-1的BaCl2溶液 | Ksp(BaCO3>Ksp(BaSO4) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . H2O2是一种绿色氧化还原试剂,在化学研究中应用广泛。某研究性学习小组设计如图所示实验装置,探究影响H2O2分解反应速率的因素。

(1)①写出锥形瓶中反应的化学方程式_________ 。
②设计实验方案:在不同条件下,测定_________ 。(要求所测得的数据能直接体现反应速率大小)
(2)探究影响H2O2分解反应速率的因素实验方案如下表所示,先向锥形瓶中加入质量分数为10%H2O2,再依次通过分液漏斗向锥形瓶中加入一定量的蒸馏水和FeCl3溶液,请回答问题:
①表格中a=_________ ,b=_________ 。
②通过实验_________ 和_________ (填写序号)探究浓度对反应速率影响。
(3)实验II、III中溶液颜色变深的原因是_________ 。
(4)已知FeCl3溶液对H2O2的催化分解分为反应i和反应ii两步进行:已知反应ii的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O;
①反应i离子方程式为_________ 。
②某同学设计实验证明催化过程中有Fe2+产生:取2mLH2O2溶液于试管中,向试管中滴加2滴FeCl3溶液,再滴加2滴_________ 溶液,产生蓝色沉淀。
(5)向实验II中反应后的溶液滴加KSCN溶液,溶液变红色,2min后溶液红色褪去;继续滴加KSCN溶液,溶液又变红色,一段时间后又褪色;此时再向溶液中滴加盐酸酸化后的BaCl2溶液,产生白色沉淀。请分析溶液红色褪去的原因_________ 。

(1)①写出锥形瓶中反应的化学方程式
②设计实验方案:在不同条件下,测定
(2)探究影响H2O2分解反应速率的因素实验方案如下表所示,先向锥形瓶中加入质量分数为10%H2O2,再依次通过分液漏斗向锥形瓶中加入一定量的蒸馏水和FeCl3溶液,请回答问题:
| 实验 序号 | 10%H2O2/mL | 蒸馏水/mL | 0.2mol·LFeCl3溶液/mL | 现象 |
| I | 10 | a | 0 | 无明显变化 |
| II | 10 | b | 2 | 锥形瓶变热,溶液迅速变红棕色,并有较多气泡产生;2min时,反应变缓,溶液颜色明显变浅 |
| III | 5 | 5 | 2 | 锥形瓶变热,溶液变棕色,开始5s后产生较少的气泡;2min时,反应速度加快 |
②通过实验
(3)实验II、III中溶液颜色变深的原因是
(4)已知FeCl3溶液对H2O2的催化分解分为反应i和反应ii两步进行:已知反应ii的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O;
①反应i离子方程式为
②某同学设计实验证明催化过程中有Fe2+产生:取2mLH2O2溶液于试管中,向试管中滴加2滴FeCl3溶液,再滴加2滴
(5)向实验II中反应后的溶液滴加KSCN溶液,溶液变红色,2min后溶液红色褪去;继续滴加KSCN溶液,溶液又变红色,一段时间后又褪色;此时再向溶液中滴加盐酸酸化后的BaCl2溶液,产生白色沉淀。请分析溶液红色褪去的原因
您最近一年使用:0次
2023-04-17更新
|
855次组卷
|
5卷引用:专题19 实验综合题
(已下线)专题19 实验综合题(已下线)广东省广州市天河区2023届高三二模化学试题变式题(实验综合题)广东省江门市2023届高三下学期第一次模拟考试化学试题广东省茂名市第一中学2023届高三下学期模拟预测化学试题广东省深圳外国语学校2024届高三上学期第三次月考化学试题
9 . 下列方案设计,现象和结论不正确的是
| 选项 | 目的 | 方案设计 | 现象和结论 |
| A | 探究铝在浓硝酸中会形成致密氧化膜 | 将去除氧化膜的铝片放入浓硝酸中,片刻后取出用水立即洗净,并快速放入硫酸铜溶液 | 铝片表面未见紫红色固体,说明铝片表面已形成致密的氧化膜 |
| B | 探究 、 、 的还原性强弱 的还原性强弱 | 向 溶液中加入少量氯水,再加 溶液中加入少量氯水,再加 萃取 萃取 | 若 层无色,则 层无色,则 的还原性强于 的还原性强于 |
| C | 比较 和 和 的氧化性强弱 的氧化性强弱 | 取适量 溶液于试管中,滴入 溶液于试管中,滴入 溶液,振荡,观察现象 溶液,振荡,观察现象 | 若产生气体使带火星木条复燃,说明 的氧化性强于 的氧化性强于 |
| D | 探究温度对 水解程度的影响 水解程度的影响 | 向25mL冷水和沸水中分别滴入5滴饱和 溶液 溶液 | 若沸水中溶液颜色比冷水中溶液颜色深,则说明升温能促进 水解 水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 溶液,溶液的
溶液,溶液的 达到平衡后,升高温度平衡逆向移动
达到平衡后,升高温度平衡逆向移动 的水解程度增大
的水解程度增大 溶液中加入少量
溶液中加入少量 固体,
固体,

