解题方法
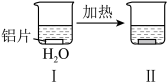
1 . 铝片与 溶液反应的探究实验如下图所示。下列说法错误的是
溶液反应的探究实验如下图所示。下列说法错误的是
 溶液反应的探究实验如下图所示。下列说法错误的是
溶液反应的探究实验如下图所示。下列说法错误的是
|
| |
无明显现象 | 铝片表面产生细小气泡 | 出现白色浑浊,产生大量气泡(经检验为 和 和 ) ) |
A. 溶液中存在水解平衡 溶液中存在水解平衡 |
B.Ⅲ中产生的细小气泡为 ,原因为 ,原因为 溶液显碱性 溶液显碱性 |
C.Ⅲ→Ⅳ的现象可说明加热可促进 的水解 的水解 |
D.Ⅳ中现象的原因为 与 与 相互促进水解产生了 相互促进水解产生了 和 和 |
您最近半年使用:0次
名校
解题方法
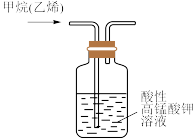
2 . 对下列图示实验的描述正确的是
|
|
| A.所示的实验:制取FeCO3 | B.所示的实验:用NaOH溶液滴定盐酸 |
|
|
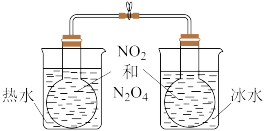
| C.用装置除去甲烷中的乙烯,以得到纯净的甲烷 | D.所示的实验:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断 的正反应是吸热反应 的正反应是吸热反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
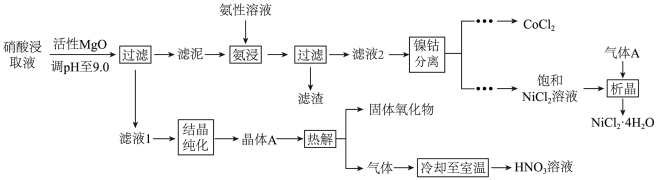
3 . 从处理后的矿石硝酸浸取液(含Ni2+、Co2+、Al3+、Mg2+)中,利用氨浸工艺可提取Ni、Co,并获得高附加值化工产品.工艺流程如下:
(1)Co位于元素周期表中的位置______________ (周期、族);
(2)“氨浸”时,由Co(OH)3转化为[Co(NH3)6]2+的离子方程式为______________________ ;
(3)(NH4)2CO3会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物.滤渣的X射线衍射图谱中,出现了NH4Al(OH)2CO3的明锐衍射峰;
①NH4Al(OH)2CO3属于______________ (填“晶体”或“非晶体”);
②(NH4)2CO3提高了Ni、Co的浸取速率,其原因是______________________ ;
(4)“析晶”过程中通入的酸性气体A为______________ .
(5)①“结晶纯化”过程中,没有引入新物质,晶体A含6个结晶水,则所得HNO3溶液中n(HNO3)与n(H2O)的比值,理论上最高为______________ ;
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用HNO3和___________ (填化学式)。
(1)Co位于元素周期表中的位置
(2)“氨浸”时,由Co(OH)3转化为[Co(NH3)6]2+的离子方程式为
(3)(NH4)2CO3会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物.滤渣的X射线衍射图谱中,出现了NH4Al(OH)2CO3的明锐衍射峰;
①NH4Al(OH)2CO3属于
②(NH4)2CO3提高了Ni、Co的浸取速率,其原因是
(4)“析晶”过程中通入的酸性气体A为
(5)①“结晶纯化”过程中,没有引入新物质,晶体A含6个结晶水,则所得HNO3溶液中n(HNO3)与n(H2O)的比值,理论上最高为
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用HNO3和
您最近半年使用:0次
4 . (1)已知25℃时,醋酸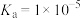 ,0.1mol/L的醋酸溶液的pH=
,0.1mol/L的醋酸溶液的pH=___________ 。
(2)相同物质的量浓度的五种溶液:①(NH4)2SO4 ②氨水③NH4HSO4 ④NH4Cl⑤(NH4)2Fe(SO4)2,c(NH4+)由大到小顺序是___________ (用序号表示)。
(3)可溶性铝盐常用作净水剂的原因:___________ (用离子方程式表示)。
(4)将等体积等物质的量浓度的CH3COONa和NaF溶液混合:c(CH3COOH)+c(HF)___________ c(OH-)-c(H+)(填 > 或 < 或 =)
(5)某温度下,测得的0.001mol/LHCl溶液中,由水电离出来的 。求此温度下,水离子积常数为
。求此温度下,水离子积常数为___________ 。在此温度下,将 的HCl溶液和
的HCl溶液和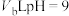 的
的 溶液混合均匀,测得溶液的pH=7,则
溶液混合均匀,测得溶液的pH=7,则
___________ 。
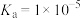 ,0.1mol/L的醋酸溶液的pH=
,0.1mol/L的醋酸溶液的pH=(2)相同物质的量浓度的五种溶液:①(NH4)2SO4 ②氨水③NH4HSO4 ④NH4Cl⑤(NH4)2Fe(SO4)2,c(NH4+)由大到小顺序是
(3)可溶性铝盐常用作净水剂的原因:
(4)将等体积等物质的量浓度的CH3COONa和NaF溶液混合:c(CH3COOH)+c(HF)
(5)某温度下,测得的0.001mol/LHCl溶液中,由水电离出来的
 。求此温度下,水离子积常数为
。求此温度下,水离子积常数为 的HCl溶液和
的HCl溶液和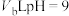 的
的 溶液混合均匀,测得溶液的pH=7,则
溶液混合均匀,测得溶液的pH=7,则
您最近半年使用:0次
名校
5 . 下列实验装置能够达到实验目的的是
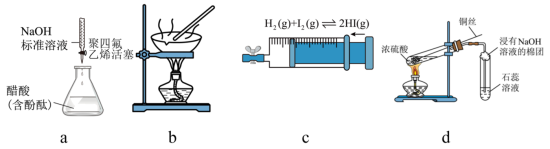
| A.图a测定醋酸的浓度 |
| B.图b由MgCl2溶液制取无水MgCl2 |
| C.图c探究压强对平衡的影响 |
| D.图d检验二氧化硫的漂白性 |
您最近半年使用:0次
名校
6 . 常温下,某 溶液的
溶液的 ,下列关于该溶液的说法中
,下列关于该溶液的说法中,不正确 的是
 溶液的
溶液的 ,下列关于该溶液的说法中
,下列关于该溶液的说法中| A.显酸性 | B.水电离出的 |
C. | D.加热, 变小 变小 |
您最近半年使用:0次
7 . 下列方案设计、现象和结论都正确的是
| 实验 | 目的 | 方案设计 | 现象和结论 |
| ① | 探究压强对 与 与 平衡的影响 平衡的影响 | 快速压缩装有 、 、 平衡混合气体的针筒 平衡混合气体的针筒 | 如果气体颜色变深,则增大压强,平衡向生成 的方向移动 的方向移动 |
| ② | 探究 与 与 氧化性的强弱 氧化性的强弱 | 向 和 和 的混合溶液中滴入 的混合溶液中滴入 酸化的 酸化的 溶液 溶液 | 溶液变红,说明氧化性: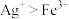 |
| ③ | 验证 溶液中存在水解平衡 溶液中存在水解平衡 | 取2  溶液于试管中,加2滴酚酞,再加入少量 溶液于试管中,加2滴酚酞,再加入少量 固体 固体 | 如果溶液红色变浅,则 溶液中存在水解平衡 溶液中存在水解平衡 |
| ④ | 相同温度下,比较 与 与 的酸性强弱 的酸性强弱 | 向等体积的水中分别通入 、 、 至饱和,再用 至饱和,再用 计测定两种溶液的 计测定两种溶液的 | 如果通 后所得溶液的 后所得溶液的 小,则 小,则 的酸性比弱 的酸性比弱 |
| A.① | B.② | C.③ | D.④ |
您最近半年使用:0次
2024高三下·全国·专题练习
8 . 某工厂采用辉铋矿(主要成分为 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制各
)联合焙烧法制各 和
和 ,工艺流程如下:
,工艺流程如下: 分解为
分解为 ,
, 转变为
转变为 ;
;
②金属活动性: ;
;
③相关金属离子形成氢氧化物的 范围如下:
范围如下:
“酸浸”中过量浓盐酸的作用为:①充分浸出 和
和 ;②
;②_______ 。
 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制各
)联合焙烧法制各 和
和 ,工艺流程如下:
,工艺流程如下: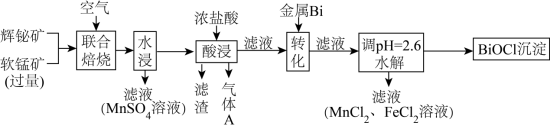
 分解为
分解为 ,
, 转变为
转变为 ;
;②金属活动性:
 ;
;③相关金属离子形成氢氧化物的
 范围如下:
范围如下:开始沉淀 | 完全沉淀 | |
 | 6.5 | 8.3 |
 | 1.6 | 2.8 |
 | 8.1 | 10.1 |
 和
和 ;②
;②
您最近半年使用:0次
名校
9 . 钛酸钡( )具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。
 )具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。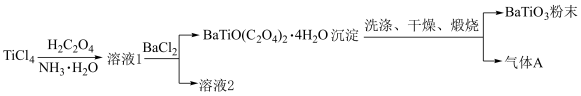
A.可用硝酸酸化的 溶液检验洗涤是否完全 溶液检验洗涤是否完全 |
| B.用溶液2提取的一种副产物可作肥料 |
| C.流程中的三步反应均为非氧化还原反应 |
D.向 中先加入 中先加入 后加入 后加入 的目的是防止 的目的是防止 水解 水解 |
您最近半年使用:0次
10 . 为了探究温度对水解平衡的影响,用手持技术测定一定浓度 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是
 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是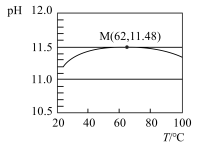
| A.该实验能证明升温促进水解 | B.点M之后 水解放热 水解放热 |
C.点M处溶液中 略大于 略大于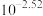 mol/L mol/L | D.点M后pH下降是因为升温对 的影响更大 的影响更大 |
您最近半年使用:0次