名校
解题方法
1 . 某实验小组对 溶液与
溶液与 溶液的反应进行探究。
溶液的反应进行探究。
已知:铁氰化钾的化学式为 ,用于检验
,用于检验 ,遇
,遇 离子产生蓝色沉淀
离子产生蓝色沉淀
(1)配制 溶液时,先将
溶液时,先将 溶于浓盐酸,再稀释至指定浓度。从化学平衡角度说明浓盐酸的作用
溶于浓盐酸,再稀释至指定浓度。从化学平衡角度说明浓盐酸的作用___________ 。
【探究现象ⅰ产生的原因】
(2)甲同学认为发生反应: (胶体)
(胶体) ;他取少量红褐色溶液于试管中,继续滴加1mol/L
;他取少量红褐色溶液于试管中,继续滴加1mol/L 溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是___________ (填化学式)。
(3)乙同学认为还发生了氧化还原反应。他取少许红褐色溶液于试管中,加入___________ ,有白色沉淀产生,证明产物中含有 。并依据反应现象判断出两种反应活化能较大的是
。并依据反应现象判断出两种反应活化能较大的是___________ (填“水解反应”或“氧化还原反应”)。
丙同学认为乙同学的实验不严谨,因为在上述过程中 可能被其它物质氧化。为了进一步确认
可能被其它物质氧化。为了进一步确认 被氧化的原因,丙同学设计了实验2。
被氧化的原因,丙同学设计了实验2。
【实验2】用如图装置(a、b均为石墨电极)进行实验。闭合开关后灵敏电流计指针偏转。

(4)实验2中正极的电极反应式为___________ 。
(5)丙同学又用铁氰化钾溶液检验正极的产物,观察到有蓝色沉淀产生。他得出的结论是___________ 。
【解释现象ⅱ产生的原因】
(6)综合上述结果,请从平衡移动角度解释,现象ⅱ产生的原因为___________ 。
 溶液与
溶液与 溶液的反应进行探究。
溶液的反应进行探究。已知:铁氰化钾的化学式为
 ,用于检验
,用于检验 ,遇
,遇 离子产生蓝色沉淀
离子产生蓝色沉淀| 【实验1】装置 | 实验现象 |
 | 现象ⅰ:一开始溶液颜色加深,由棕黄色变为红褐色。 现象ⅱ:一段时间后溶液颜色变浅,变为浅黄色。 |
(1)配制
 溶液时,先将
溶液时,先将 溶于浓盐酸,再稀释至指定浓度。从化学平衡角度说明浓盐酸的作用
溶于浓盐酸,再稀释至指定浓度。从化学平衡角度说明浓盐酸的作用【探究现象ⅰ产生的原因】
(2)甲同学认为发生反应:
 (胶体)
(胶体) ;他取少量红褐色溶液于试管中,继续滴加1mol/L
;他取少量红褐色溶液于试管中,继续滴加1mol/L 溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是
溶液,发现溶液红褐色变深且产生刺激性气味的气体,该气体是(3)乙同学认为还发生了氧化还原反应。他取少许红褐色溶液于试管中,加入
 。并依据反应现象判断出两种反应活化能较大的是
。并依据反应现象判断出两种反应活化能较大的是丙同学认为乙同学的实验不严谨,因为在上述过程中
 可能被其它物质氧化。为了进一步确认
可能被其它物质氧化。为了进一步确认 被氧化的原因,丙同学设计了实验2。
被氧化的原因,丙同学设计了实验2。【实验2】用如图装置(a、b均为石墨电极)进行实验。闭合开关后灵敏电流计指针偏转。

(4)实验2中正极的电极反应式为
(5)丙同学又用铁氰化钾溶液检验正极的产物,观察到有蓝色沉淀产生。他得出的结论是
【解释现象ⅱ产生的原因】
(6)综合上述结果,请从平衡移动角度解释,现象ⅱ产生的原因为
您最近一年使用:0次
解题方法
2 . 聚硅酸铁是目前无机高分子絮凝剂研究的热点,一种用钢管厂的废铁渣(主要成分Fe3O4,少量碳及二氧化硅)为原料制备的流程如下:

(1)为了提高废铁渣的浸出率,应该采用___________ (至少写一项)。
(2)“酸浸”需适宜的酸浓度、液固比、酸浸温度、氧流量等,其中酸浸温度对铁浸取率的影响如图所示:

①加热条件下酸浸时,Fe3O4与硫酸反应的化学方程式为___________ 。
②酸浸时,通入O2的目的是___________ ,该反应的离子方程式为___________ 。
③当酸浸温度超过100℃时,铁浸取率反而减小,其原因是___________ 。
(3)滤渣的主要成分为___________ (填化学式)。
(4)“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+;在酸性条件下,再用K2Cr2O7标准溶液滴定Fe2+( 被还原为Cr3+),该滴定反应的离子方程式为
被还原为Cr3+),该滴定反应的离子方程式为___________ 。

(1)为了提高废铁渣的浸出率,应该采用
(2)“酸浸”需适宜的酸浓度、液固比、酸浸温度、氧流量等,其中酸浸温度对铁浸取率的影响如图所示:

①加热条件下酸浸时,Fe3O4与硫酸反应的化学方程式为
②酸浸时,通入O2的目的是
③当酸浸温度超过100℃时,铁浸取率反而减小,其原因是
(3)滤渣的主要成分为
(4)“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+;在酸性条件下,再用K2Cr2O7标准溶液滴定Fe2+(
 被还原为Cr3+),该滴定反应的离子方程式为
被还原为Cr3+),该滴定反应的离子方程式为
您最近一年使用:0次
名校
3 . 由下列实验操作和现象所得结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向Na2CO3溶液中滴加2滴酚酞试液,再加热该溶液 | 溶液显红色、加热后颜色变深 |  能水解且水解过程吸热 能水解且水解过程吸热 |
| B | 在圆底烧瓶中加入乙醇和浓硫酸的混合液及适量沸石。迅速升温至170℃并将产生的气体通入酸性KMnO4溶液中 | KMnO4溶液褪色 | 有乙烯生成 |
| C | 向KI-淀粉溶液中滴加过量饱和氯水后再滴入几滴淀粉溶液 | 溶液先变蓝色后褪色,最终仍无色 | 氯水有氧化性、漂白性 |
| D | 常温下将铝条插入浓硫酸中,一段时间取出铝条 | 铝条几乎无变化 | 常温下铝条与浓硫酸不反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . I.含铜电路板可以用FeCl3溶液进行刻蚀,对刻蚀后的液体(主要含FeCl3、FeCl2、CuCl2等)进行处理,可以回收FeCl2·4H2O和CuSO4·5H2O,工艺流程如下:
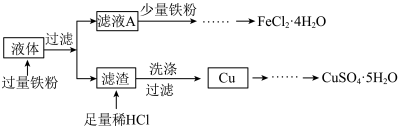
(1)从滤液A中提取FeCl2·4H2O的操作为:加入少量铁粉后,先浓缩滤液至出现___________ ,趁热过滤,取溶液,___________ ,过滤、洗涤、干燥;浓缩滤液前先加入少量铁粉的原因是___________ 。
(2)检验从滤渣中提取出的Cu上Cl—已洗净的操作为:___________ ;制备CuSO4·5H2O时,将Cu溶解于H2SO4、HNO3的混酸中,若该过程中产生的气体只有NO,且反应后溶质只有CuSO4,则混酸中H2SO4、HNO3的浓度之比为___________ 。
II.利用滴定法可以测定CuSO4·5H2O的纯度,操作如下:
①取agCuSO4·5H2O样品,加入足量NH4F—HF混合溶液溶解 (其中F—防止Fe3+干扰检验:Fe3++6F—=[FeF6]3—)。
②滴加足量KI溶液,发生反应:2Cu2++4I—=2CuI↓+I2。
③用cmol·L-1Na2S2O3标准溶液滴定,以淀粉溶液为指示剂,到达滴定终点时消耗Na2S2O3标准液VmL,发生的反应为:I2+2 =
= +2I—。
+2I—。
(3)已知NH4F溶液呈酸性,则水解程度:
___________ F—(选填“>”“<”或“=”),加水稀释,溶液中
___________ (选填“变大”“变小”或“不变”)。
(4)已知CuI沉淀能够大量吸附I2,因此在接近滴定终点时向溶液中滴加KSCN溶液,CuI转化为CuSCN,通过平衡移动的原理解释沉淀转化的原因:___________ 。
(5)CuSO4·5H2O的质量分数为___________ (用含a,c,V的代数式表示)。若步骤①使用蒸馏水溶解样品,则测得CuSO4·5H2O的质量分数将___________ ;若步骤③不滴加KSCN溶液,则测得CuSO4·5H2O的质量分数将___________ (均选填“偏高”“偏低”或“不变”)。

(1)从滤液A中提取FeCl2·4H2O的操作为:加入少量铁粉后,先浓缩滤液至出现
(2)检验从滤渣中提取出的Cu上Cl—已洗净的操作为:
II.利用滴定法可以测定CuSO4·5H2O的纯度,操作如下:
①取agCuSO4·5H2O样品,加入足量NH4F—HF混合溶液溶解 (其中F—防止Fe3+干扰检验:Fe3++6F—=[FeF6]3—)。
②滴加足量KI溶液,发生反应:2Cu2++4I—=2CuI↓+I2。
③用cmol·L-1Na2S2O3标准溶液滴定,以淀粉溶液为指示剂,到达滴定终点时消耗Na2S2O3标准液VmL,发生的反应为:I2+2
 =
= +2I—。
+2I—。(3)已知NH4F溶液呈酸性,则水解程度:


(4)已知CuI沉淀能够大量吸附I2,因此在接近滴定终点时向溶液中滴加KSCN溶液,CuI转化为CuSCN,通过平衡移动的原理解释沉淀转化的原因:
(5)CuSO4·5H2O的质量分数为
您最近一年使用:0次
5 . 氨是重要的工业原料,在农业、医药,国防和化工等领域有重要应用。
I.某温度下水的离子积常数为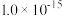 ,向
,向 的氨水中逐滴加入
的氨水中逐滴加入 的盐酸,所得溶液的
的盐酸,所得溶液的 ,溶液中
,溶液中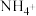 和
和 物质的量分数与加入盐酸的体积的关系如图所示,根据图象回答下列问题。
物质的量分数与加入盐酸的体积的关系如图所示,根据图象回答下列问题。
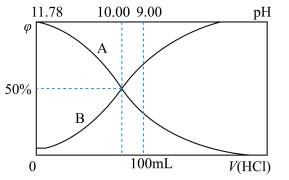
(1)表示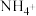 物质的量分数变化的曲线是
物质的量分数变化的曲线是___________ (填“A”或“B”)。
(2)该温度下, 的电离平衡常数为
的电离平衡常数为___________ 。
(3)当加入盐酸体积为 时,溶液中
时,溶液中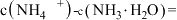
_______  (用数字表示精确值)。
(用数字表示精确值)。
Ⅱ.铵盐在日常生活中用处广泛, 常作食品加工中的食品添加剂,用于焙烤食品。请回答下列问题:
常作食品加工中的食品添加剂,用于焙烤食品。请回答下列问题:
(4) 可作净水剂,其原理是
可作净水剂,其原理是_________________________________ (用离子方程式说明)。
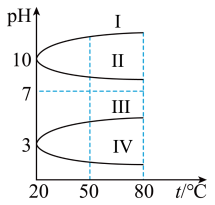
(5)下列图像为 的几种电解质溶液的pH随温度变化的曲线。
的几种电解质溶液的pH随温度变化的曲线。
其中符合 溶液的pH随温度变化的曲线是
溶液的pH随温度变化的曲线是___________ (填罗马数字), 溶液的pH随温度变化的原因是
溶液的pH随温度变化的原因是_________________________________ 。
(6)相同条件下,下列五种溶液中 由到小的大顺序是
由到小的大顺序是___________ (填序号)。
①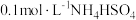 溶液
溶液
② 溶液
溶液
③ 溶液
溶液
④ 溶液
溶液
⑤ 氨水
氨水
I.某温度下水的离子积常数为
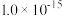 ,向
,向 的氨水中逐滴加入
的氨水中逐滴加入 的盐酸,所得溶液的
的盐酸,所得溶液的 ,溶液中
,溶液中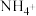 和
和 物质的量分数与加入盐酸的体积的关系如图所示,根据图象回答下列问题。
物质的量分数与加入盐酸的体积的关系如图所示,根据图象回答下列问题。
(1)表示
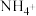 物质的量分数变化的曲线是
物质的量分数变化的曲线是(2)该温度下,
 的电离平衡常数为
的电离平衡常数为(3)当加入盐酸体积为
 时,溶液中
时,溶液中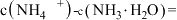
 (用数字表示精确值)。
(用数字表示精确值)。Ⅱ.铵盐在日常生活中用处广泛,
 常作食品加工中的食品添加剂,用于焙烤食品。请回答下列问题:
常作食品加工中的食品添加剂,用于焙烤食品。请回答下列问题:(4)
 可作净水剂,其原理是
可作净水剂,其原理是(5)下列图像为
 的几种电解质溶液的pH随温度变化的曲线。
的几种电解质溶液的pH随温度变化的曲线。其中符合
 溶液的pH随温度变化的曲线是
溶液的pH随温度变化的曲线是 溶液的pH随温度变化的原因是
溶液的pH随温度变化的原因是
(6)相同条件下,下列五种溶液中
 由到小的大顺序是
由到小的大顺序是①
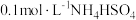 溶液
溶液②
 溶液
溶液③
 溶液
溶液④
 溶液
溶液⑤
 氨水
氨水
您最近一年使用:0次
2023高三·全国·专题练习
名校
6 . 已知K2Cr2O7溶液中存在平衡:Cr2O +H2O
+H2O 2CrO
2CrO +2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
+2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
 +H2O
+H2O 2CrO
2CrO +2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
+2H+。分别在T1℃、T2℃恒温条件下,向100mL0.100mol·L-1的K2Cr2O7溶液中加入一定量K2Cr2O7固体,持续搅拌下用pH传感器连续测量溶液的pH,得到如图图象,下列说法正确的是
| A.图中T1℃>T2℃ |
B.t1后溶液中有2c(Cr2O )+c(CrO )+c(CrO )=c(K+) )=c(K+) |
| C.T2℃时,上述反应的平衡常数的数量级是10-12 |
D.T1℃下,加入一定量K2Cr2O7固体后达到新平衡时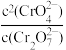 的值增大 的值增大 |
您最近一年使用:0次
2023-12-16更新
|
197次组卷
|
3卷引用:盐类的水解
名校
解题方法
7 . 下列说法正确的是
| A.AlCl3溶液和Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分不同 |
| B.配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度 |
| C.实验室制备的NaF溶液应保存在玻璃试剂瓶中 |
| D.BaCO3可用于胃肠X射线造影检查 |
您最近一年使用:0次
名校
8 . 下列事实不能用勒夏特列原理解释的是
A.用热的 溶液清洗带有油污的餐具 溶液清洗带有油污的餐具 |
| B.把食品存放在冰箱里可延长保质期 |
| C.工业合成氨常采用20MPa的高压 |
D.配制 溶液,常将 溶液,常将 晶体溶于较浓的盐酸中 晶体溶于较浓的盐酸中 |
您最近一年使用:0次
名校
解题方法
9 . 关于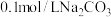 溶液,下列判断不正确的是
溶液,下列判断不正确的是
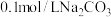 溶液,下列判断不正确的是
溶液,下列判断不正确的是| A.存在盐的电离平衡和水解平衡 |
B.升高温度, 增大 增大 |
C.加入 溶液, 溶液, 减小 减小 |
D. |
您最近一年使用:0次
2023-12-08更新
|
125次组卷
|
3卷引用:北京市清华大学附属中学2023-2024学年高二上学期第三单元化学统练
名校
解题方法
10 . 中科院化学所研制的唱体材料——纳米四氧化三铁,在核磁共振造影及医药上有广泛用途,其生产过程的部分流程如图所示: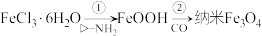 ,下列有关说法正确的是
,下列有关说法正确的是
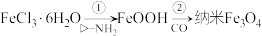 ,下列有关说法正确的是
,下列有关说法正确的是A.可用稀硫酸和 鉴别Fe3O4和FeO 鉴别Fe3O4和FeO |
B.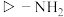 在反应①中的作用是促进氯化铁水解 在反应①中的作用是促进氯化铁水解 |
| C.将制得的纳米Fe3O4均匀分散在水中不会产生丁达尔效应 |
D.反应②发生的化学方程式为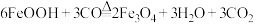 |
您最近一年使用:0次
2023-12-08更新
|
103次组卷
|
2卷引用:天津市第一中学2023-2024学年高三上学期第二次月考化学试题



