1 . (1)已知25℃时,醋酸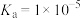 ,0.1mol/L的醋酸溶液的pH=
,0.1mol/L的醋酸溶液的pH=___________ 。
(2)相同物质的量浓度的五种溶液:①(NH4)2SO4 ②氨水③NH4HSO4 ④NH4Cl⑤(NH4)2Fe(SO4)2,c(NH4+)由大到小顺序是___________ (用序号表示)。
(3)可溶性铝盐常用作净水剂的原因:___________ (用离子方程式表示)。
(4)将等体积等物质的量浓度的CH3COONa和NaF溶液混合:c(CH3COOH)+c(HF)___________ c(OH-)-c(H+)(填 > 或 < 或 =)
(5)某温度下,测得的0.001mol/LHCl溶液中,由水电离出来的 。求此温度下,水离子积常数为
。求此温度下,水离子积常数为___________ 。在此温度下,将 的HCl溶液和
的HCl溶液和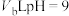 的
的 溶液混合均匀,测得溶液的pH=7,则
溶液混合均匀,测得溶液的pH=7,则
___________ 。
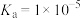 ,0.1mol/L的醋酸溶液的pH=
,0.1mol/L的醋酸溶液的pH=(2)相同物质的量浓度的五种溶液:①(NH4)2SO4 ②氨水③NH4HSO4 ④NH4Cl⑤(NH4)2Fe(SO4)2,c(NH4+)由大到小顺序是
(3)可溶性铝盐常用作净水剂的原因:
(4)将等体积等物质的量浓度的CH3COONa和NaF溶液混合:c(CH3COOH)+c(HF)
(5)某温度下,测得的0.001mol/LHCl溶液中,由水电离出来的
 。求此温度下,水离子积常数为
。求此温度下,水离子积常数为 的HCl溶液和
的HCl溶液和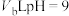 的
的 溶液混合均匀,测得溶液的pH=7,则
溶液混合均匀,测得溶液的pH=7,则
您最近一年使用:0次
名校
解题方法
2 . 镍及其化合物用途广泛。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,以下是从该矿渣中回收NiSO4的工艺路线:
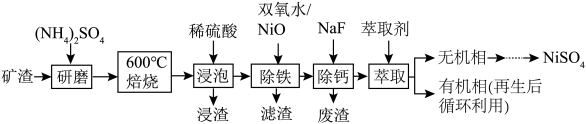
已知:①(NH4)2SO4在350℃以上会分解生成NH3和H2SO4,NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3。②铁元素以针铁矿(FeOOH)形式沉淀,铁渣易过滤。
请回答下列问题:
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是______ ,写出焙烧过程中铁酸镍发生的化学反应方程式______ 。
(2)“浸渣”的主要成分为______ (填化学式)。
(3)溶液pH对铁去除率的影响实验结果如图所示:
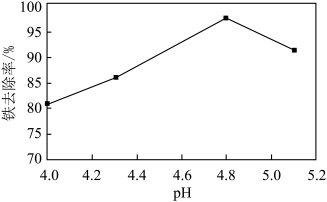
①从图中数据来看,沉铁的最佳pH为______ 。
②结合图中数据,解释pH偏小或偏大都不利于沉铁的原因是______ 、______ 。
③检验“除铁”后溶液中是否还有Fe3+的操作是______ 。
(4)若溶液中c(Ca2+)=1.0×10-3mol•L-1,当除钙率达到99%时,溶液中c(F—)=_____ mol•L-1。[已知Ksp(CaF2)= 4.0×10-11]

已知:①(NH4)2SO4在350℃以上会分解生成NH3和H2SO4,NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3。②铁元素以针铁矿(FeOOH)形式沉淀,铁渣易过滤。
请回答下列问题:
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是
(2)“浸渣”的主要成分为
(3)溶液pH对铁去除率的影响实验结果如图所示:

①从图中数据来看,沉铁的最佳pH为
②结合图中数据,解释pH偏小或偏大都不利于沉铁的原因是
③检验“除铁”后溶液中是否还有Fe3+的操作是
(4)若溶液中c(Ca2+)=1.0×10-3mol•L-1,当除钙率达到99%时,溶液中c(F—)=
您最近一年使用:0次
名校
3 . 在日常生产生活中,经常涉及化学反应原理,下列过程或现象与盐类水解无关的是
| A.加热氯化铁溶液,颜色变深 |
B. 与 与 溶液可用作焊接金属时的除锈剂 溶液可用作焊接金属时的除锈剂 |
| C.氯化钙溶液中滴加甲基橙,溶液显黄色 |
D.实验室中盛放 溶液的试剂瓶不能用磨口玻璃塞 溶液的试剂瓶不能用磨口玻璃塞 |
您最近一年使用:0次
2024-03-09更新
|
185次组卷
|
2卷引用:安徽省合肥市第一中学2023-2024学年高二上学期期末考试化学试题
23-24高二上·广东深圳·期末
名校
解题方法
4 . 下列颜色变化,与勒夏特列原理无关的是
| A.红棕色的NO2体系加压后,颜色先变深后逐渐变浅 |
| B.将0.01mol/LFeCl3溶液加热,溶液的颜色加深 |
| C.H2、I2、HI平衡混合气加压后颜色变深 |
| D.新制的氯水在光照下颜色变浅 |
您最近一年使用:0次
名校
5 . 石油天然气开采和炼制过程中会产生大量含硫废水(其中S元素主要化合价是-2价),对设备、环境等造成严重危害。已知:H2S有剧毒;常温下溶解度为1:2.6(体积)。
(1)如图为常温下H2S、HS—、S2—在水溶液中的物质的量分数随pH变化的分布曲线,回答下列问题:

①当pH≈8时,含硫废水中最主要的含硫微粒为___________ 。
②NaHS溶液呈___________ (填“酸性”、“碱性”或“中性”),NaHS水解的离子方程式为:___________ 。
③由图判断,NaHS在常温下发生水解的平衡常数Kh=___________ 。
(2)沉淀法处理含硫废水:向pH≈8的含硫废水中加入适量Cu2+的溶液,产生黑色沉淀且溶液的pH降低,用化学平衡移动的原理解释溶液pH降低的原因:___________ 。
(3)氧化还原法处理含硫废水:向pH≈8的含硫废水中加入一定浓度的Na2SO3溶液,加适量酸,溶液产生淡黄色沉淀。不同pH时,硫化物去除率随时间的变化曲线如图所示,试分析本工艺选择控制体系的pH≈6,而不是去除率更高的pH=3的主要原因:___________ 。

(4)已知:Ksp(AgI)=8.5×10-17、Ksp(AgCl)=1.8×10-10,向浓度均为0.1mol•L-1的NaCl和NaI的混合液中逐渐加入AgNO3粉末,当溶液中I—浓度下降到___________ mol•L-1时(保留一位小数),AgCl开始沉淀。
(1)如图为常温下H2S、HS—、S2—在水溶液中的物质的量分数随pH变化的分布曲线,回答下列问题:

①当pH≈8时,含硫废水中最主要的含硫微粒为
②NaHS溶液呈
③由图判断,NaHS在常温下发生水解的平衡常数Kh=
(2)沉淀法处理含硫废水:向pH≈8的含硫废水中加入适量Cu2+的溶液,产生黑色沉淀且溶液的pH降低,用化学平衡移动的原理解释溶液pH降低的原因:
(3)氧化还原法处理含硫废水:向pH≈8的含硫废水中加入一定浓度的Na2SO3溶液,加适量酸,溶液产生淡黄色沉淀。不同pH时,硫化物去除率随时间的变化曲线如图所示,试分析本工艺选择控制体系的pH≈6,而不是去除率更高的pH=3的主要原因:

(4)已知:Ksp(AgI)=8.5×10-17、Ksp(AgCl)=1.8×10-10,向浓度均为0.1mol•L-1的NaCl和NaI的混合液中逐渐加入AgNO3粉末,当溶液中I—浓度下降到
您最近一年使用:0次
名校
解题方法
6 . 下列操作能达到相应实验目的的是
| 实验操作 | 实验目的 | |
| A | 向等体积、等pH的两种酸溶液HA和HB中分别加入足量锌粉,充分反应后,HA溶液产生更多的氢气 | 说明Ka(HA)>Ka(HB) |
| B | 向5mL0.1mol/LCuSO4溶液中先加入2mL0.4mol/LNaOH溶液,再加入1mL0.1mol/LNa2S溶液 | 探究常温下Ksp[Cu(OH)2]>Ksp(CuS) |
| C | 向滴有酚酞的碳酸钠溶液中加入适量BaCl2固体,溶液颜色变浅 | 说明碳酸钠溶液中存在水解平衡 |
| D | 向2支盛有5mL不同浓度NaHSO3溶液的试管中,同时加入2mL5%H2O2溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-27更新
|
381次组卷
|
2卷引用:辽宁省五校联考2023-2024学年高二上学期期末考试化学试题
解题方法
7 . 实验测得 溶液、
溶液、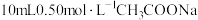 溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃时
溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃时 和
和 电离常数均为
电离常数均为 ,下列说法正确的是
,下列说法正确的是
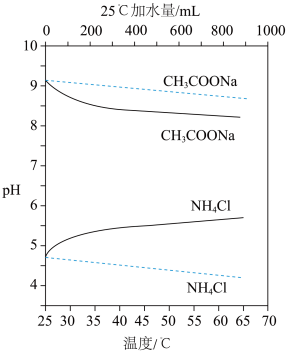
 溶液、
溶液、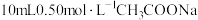 溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃时
溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃时 和
和 电离常数均为
电离常数均为 ,下列说法正确的是
,下列说法正确的是
| A.图中 |
B.将 溶液加水稀释至浓度 溶液加水稀释至浓度 ,溶液pH变化值小于 ,溶液pH变化值小于 |
C.随温度升高, 增大, 增大, 溶液中 溶液中 减小, 减小, 增大,pH减小 增大,pH减小 |
D.25℃时稀释相同倍数的 溶液与 溶液与 溶液中: 溶液中: |
您最近一年使用:0次
名校
解题方法
8 . 已知 、
、 、
、 、
、 、
、 分别表示弱酸的电离平衡常数、弱碱的电离平衡常数,水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为
分别表示弱酸的电离平衡常数、弱碱的电离平衡常数,水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为 时以下数据:
时以下数据: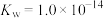 ,
, ,
,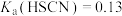 ,
, ,
,
(1)有关上述常数的说法正确的是___________ 。
a.它们都能反映一定条件下对应变化进行的程度
b.所有弱电解质的电离常数和难溶电解质的 都随温度的升高而增大
都随温度的升高而增大
c.常温下, 在水中的
在水中的 大于在饱和
大于在饱和 溶液中的
溶液中的
d.一定温度下,在 溶液中,
溶液中,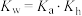
(2) 时,将浓度相等的
时,将浓度相等的 与
与 溶液等体积混合,判断溶液呈
溶液等体积混合,判断溶液呈___________ (填“酸”、“碱”或“中”)性。
(3)已知 溶液为中性,又知
溶液为中性,又知 溶液加到
溶液加到 溶液中有气体放出,现有
溶液中有气体放出,现有 时等浓度的四种溶液:A.
时等浓度的四种溶液:A.  ,B.
,B. ,C.
,C. ,D.
,D. 。
。
回答下列问题:
①试推断 溶液的
溶液的
___________ 7(填“>”、“<”或“=”)
②将四种溶液按 浓度由大到小的顺序排列是:
浓度由大到小的顺序排列是:___________ (用字母排序)。
(4)为探究 在酸中的溶解性,利用以上数据可以计算出反应:
在酸中的溶解性,利用以上数据可以计算出反应: 在
在 时的平衡常数
时的平衡常数
___________ ,并据此推断 是否能溶解于醋酸,并简要说明原因。(已知
是否能溶解于醋酸,并简要说明原因。(已知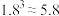 )
)___________ 。
 、
、 、
、 、
、 、
、 分别表示弱酸的电离平衡常数、弱碱的电离平衡常数,水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为
分别表示弱酸的电离平衡常数、弱碱的电离平衡常数,水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为 时以下数据:
时以下数据: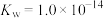 ,
, ,
,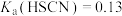 ,
, ,
,
(1)有关上述常数的说法正确的是
a.它们都能反映一定条件下对应变化进行的程度
b.所有弱电解质的电离常数和难溶电解质的
 都随温度的升高而增大
都随温度的升高而增大c.常温下,
 在水中的
在水中的 大于在饱和
大于在饱和 溶液中的
溶液中的
d.一定温度下,在
 溶液中,
溶液中,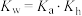
(2)
 时,将浓度相等的
时,将浓度相等的 与
与 溶液等体积混合,判断溶液呈
溶液等体积混合,判断溶液呈(3)已知
 溶液为中性,又知
溶液为中性,又知 溶液加到
溶液加到 溶液中有气体放出,现有
溶液中有气体放出,现有 时等浓度的四种溶液:A.
时等浓度的四种溶液:A.  ,B.
,B. ,C.
,C. ,D.
,D. 。
。回答下列问题:
①试推断
 溶液的
溶液的
②将四种溶液按
 浓度由大到小的顺序排列是:
浓度由大到小的顺序排列是:(4)为探究
 在酸中的溶解性,利用以上数据可以计算出反应:
在酸中的溶解性,利用以上数据可以计算出反应: 在
在 时的平衡常数
时的平衡常数
 是否能溶解于醋酸,并简要说明原因。(已知
是否能溶解于醋酸,并简要说明原因。(已知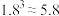 )
)
您最近一年使用:0次
9 . 下列实验过程中的相关操作正确的是
| 选项 | 实验 | 操作 |
| A | 验证: | 向 溶液中先加入 溶液中先加入 滴 滴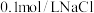 溶液,再滴加 溶液,再滴加 滴 滴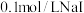 溶液 溶液 |
| B | 探究浓度对反应速率的影响 | 向2支盛有 不同浓度的 不同浓度的 溶液的试管中同时加入 溶液的试管中同时加入 硫酸,记录出现浑浊的时间 硫酸,记录出现浑浊的时间 |
| C | 由 溶液制备无水 溶液制备无水 | 将 溶液加热蒸干 溶液加热蒸干 |
| D | 验证 是弱酸 是弱酸 | 室温下,用 试纸测定浓度为 试纸测定浓度为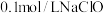 溶液的 溶液的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 .  溶液中,如果要使
溶液中,如果要使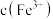 更接近于
更接近于 ,可以采取的措施是
,可以采取的措施是
 溶液中,如果要使
溶液中,如果要使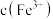 更接近于
更接近于 ,可以采取的措施是
,可以采取的措施是| A.加入适量水 | B.加入少量 溶液 溶液 | C.通入适量 气体 气体 | D.加热 |
您最近一年使用:0次



