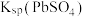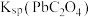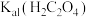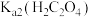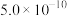1 . 以钛白副产品(含 及少量
及少量 )和
)和 为原料制备的超微细
为原料制备的超微细 ,可广泛用于新型电池材料、感光材料的生产。
,可广泛用于新型电池材料、感光材料的生产。
已知:①25℃时,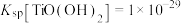 ;
;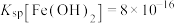 ;
;
② 不溶于水,溶于硫酸。
不溶于水,溶于硫酸。
③沉淀速度过快,沉淀的粒径会变大,包裹的杂质会变多。
(1) 的制备。将一定量的钛白副产品用热水溶解,在搅拌下加入还原铁粉,反应后pH为4~5,过滤得到
的制备。将一定量的钛白副产品用热水溶解,在搅拌下加入还原铁粉,反应后pH为4~5,过滤得到 溶液。在搅拌下先后加入氨水和草酸溶液,经
溶液。在搅拌下先后加入氨水和草酸溶液,经 调节pH、过滤、水洗、烘干后得到超微细FeC2O4·2H2O。
调节pH、过滤、水洗、烘干后得到超微细FeC2O4·2H2O。
①加入还原铁粉的作用是___________ ;
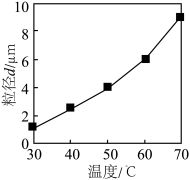
②温度对沉淀粒径的影响如图,加入氨水和草酸溶液过程需控制温度在40℃的原因是___________ ;___________ 。 的结构。
的结构。 晶体为片层结构,层内每个
晶体为片层结构,层内每个 与2个
与2个 和2个
和2个 相连,形成1个铁氧八面体。在图中补全该结构
相连,形成1个铁氧八面体。在图中补全该结构___________ 。 晶体层与层之间的作用力为
晶体层与层之间的作用力为___________ 。 的性质。将
的性质。将 在氮气的氛围中加热分解。加热过程中固体残留率[固体残留率=
在氮气的氛围中加热分解。加热过程中固体残留率[固体残留率= ]随温度的变化如图所示,B点时,固体只含有一种铁的氧化物,则AB段发生反应的化学方程式:
]随温度的变化如图所示,B点时,固体只含有一种铁的氧化物,则AB段发生反应的化学方程式:___________ 。
 及少量
及少量 )和
)和 为原料制备的超微细
为原料制备的超微细 ,可广泛用于新型电池材料、感光材料的生产。
,可广泛用于新型电池材料、感光材料的生产。已知:①25℃时,
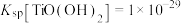 ;
;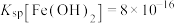 ;
;②
 不溶于水,溶于硫酸。
不溶于水,溶于硫酸。③沉淀速度过快,沉淀的粒径会变大,包裹的杂质会变多。
(1)
 的制备。将一定量的钛白副产品用热水溶解,在搅拌下加入还原铁粉,反应后pH为4~5,过滤得到
的制备。将一定量的钛白副产品用热水溶解,在搅拌下加入还原铁粉,反应后pH为4~5,过滤得到 溶液。在搅拌下先后加入氨水和草酸溶液,经
溶液。在搅拌下先后加入氨水和草酸溶液,经 调节pH、过滤、水洗、烘干后得到超微细FeC2O4·2H2O。
调节pH、过滤、水洗、烘干后得到超微细FeC2O4·2H2O。①加入还原铁粉的作用是
②温度对沉淀粒径的影响如图,加入氨水和草酸溶液过程需控制温度在40℃的原因是
 的结构。
的结构。 晶体为片层结构,层内每个
晶体为片层结构,层内每个 与2个
与2个 和2个
和2个 相连,形成1个铁氧八面体。在图中补全该结构
相连,形成1个铁氧八面体。在图中补全该结构 晶体层与层之间的作用力为
晶体层与层之间的作用力为
 的性质。将
的性质。将 在氮气的氛围中加热分解。加热过程中固体残留率[固体残留率=
在氮气的氛围中加热分解。加热过程中固体残留率[固体残留率= ]随温度的变化如图所示,B点时,固体只含有一种铁的氧化物,则AB段发生反应的化学方程式:
]随温度的变化如图所示,B点时,固体只含有一种铁的氧化物,则AB段发生反应的化学方程式: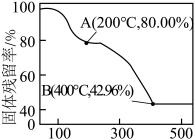
您最近一年使用:0次
名校
解题方法
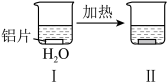
2 . 铝片与 溶液反应的探究实验如下图所示。下列说法错误的是
溶液反应的探究实验如下图所示。下列说法错误的是
 溶液反应的探究实验如下图所示。下列说法错误的是
溶液反应的探究实验如下图所示。下列说法错误的是
|
| |
无明显现象 | 铝片表面产生细小气泡 | 出现白色浑浊,产生大量气泡(经检验为 和 和 ) ) |
A. 溶液中存在水解平衡 溶液中存在水解平衡 |
B.Ⅲ中产生的细小气泡为 ,原因为 ,原因为 溶液显碱性 溶液显碱性 |
C.Ⅲ→Ⅳ的现象可说明加热可促进 的水解 的水解 |
D.Ⅳ中现象的原因为 与 与 相互促进水解产生了 相互促进水解产生了 和 和 |
您最近一年使用:0次
2024-05-27更新
|
115次组卷
|
2卷引用:天津市耀华中学2024届高三下学期第二次模拟化学试题
3 . 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 往 溶液中滴加几滴浓硫酸,溶液由橙色变为黄色 溶液中滴加几滴浓硫酸,溶液由橙色变为黄色 |  呈橙色, 呈橙色, 呈黄色 呈黄色 |
| B | 将浓硫酸加入蔗糖中形成多孔炭 | 浓硫酸具有强氧化性和脱水性 |
| C | 低温石英(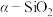 )制作石英手表 )制作石英手表 |  属于共价晶体,熔点高 属于共价晶体,熔点高 |
| D | 用钨钢钻头给混凝土墙面钻孔 | 合金硬度比其组成的纯金属低 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 下列实验装置能够达到实验目的的是
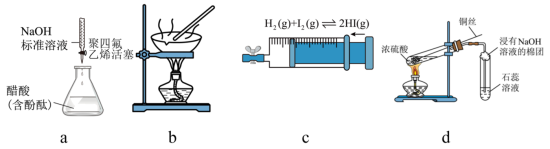
| A.图a测定醋酸的浓度 |
| B.图b由MgCl2溶液制取无水MgCl2 |
| C.图c探究压强对平衡的影响 |
| D.图d检验二氧化硫的漂白性 |
您最近一年使用:0次
2024-04-22更新
|
294次组卷
|
2卷引用:2024届海南省海南中学高三下学期第一次模拟化学试题
5 . 下列方案设计、现象和结论都正确的是
| 实验 | 目的 | 方案设计 | 现象和结论 |
| ① | 探究压强对 与 与 平衡的影响 平衡的影响 | 快速压缩装有 、 、 平衡混合气体的针筒 平衡混合气体的针筒 | 如果气体颜色变深,则增大压强,平衡向生成 的方向移动 的方向移动 |
| ② | 探究 与 与 氧化性的强弱 氧化性的强弱 | 向 和 和 的混合溶液中滴入 的混合溶液中滴入 酸化的 酸化的 溶液 溶液 | 溶液变红,说明氧化性: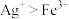 |
| ③ | 验证 溶液中存在水解平衡 溶液中存在水解平衡 | 取2  溶液于试管中,加2滴酚酞,再加入少量 溶液于试管中,加2滴酚酞,再加入少量 固体 固体 | 如果溶液红色变浅,则 溶液中存在水解平衡 溶液中存在水解平衡 |
| ④ | 相同温度下,比较 与 与 的酸性强弱 的酸性强弱 | 向等体积的水中分别通入 、 、 至饱和,再用 至饱和,再用 计测定两种溶液的 计测定两种溶液的 | 如果通 后所得溶液的 后所得溶液的 小,则 小,则 的酸性比弱 的酸性比弱 |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
2024高三下·全国·专题练习
6 . 某工厂采用辉铋矿(主要成分为 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制各
)联合焙烧法制各 和
和 ,工艺流程如下:
,工艺流程如下: 分解为
分解为 ,
, 转变为
转变为 ;
;
②金属活动性: ;
;
③相关金属离子形成氢氧化物的 范围如下:
范围如下:
“酸浸”中过量浓盐酸的作用为:①充分浸出 和
和 ;②
;②_______ 。
 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制各
)联合焙烧法制各 和
和 ,工艺流程如下:
,工艺流程如下: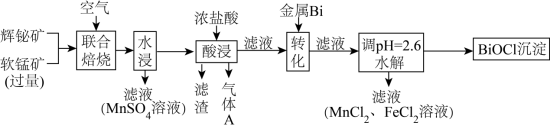
 分解为
分解为 ,
, 转变为
转变为 ;
;②金属活动性:
 ;
;③相关金属离子形成氢氧化物的
 范围如下:
范围如下:开始沉淀 | 完全沉淀 | |
 | 6.5 | 8.3 |
 | 1.6 | 2.8 |
 | 8.1 | 10.1 |
 和
和 ;②
;②
您最近一年使用:0次
7 . 为了探究温度对水解平衡的影响,用手持技术测定一定浓度 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是
 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是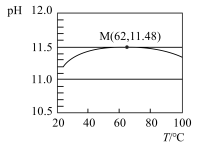
| A.该实验能证明升温促进水解 | B.点M之后 水解放热 水解放热 |
C.点M处溶液中 略大于 略大于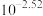 mol/L mol/L | D.点M后pH下降是因为升温对 的影响更大 的影响更大 |
您最近一年使用:0次
8 . 稀土在电子、激光、核工业、超导等诸多高科技领域有广泛的应用。钪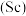 是一种稀土金属,钛尾矿经一系列处理后得到固体
是一种稀土金属,钛尾矿经一系列处理后得到固体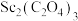 和主要成分是
和主要成分是 的废水,利用钛尾矿回收金属钪和草酸的工艺流程如图所示。回答下列问题:
的废水,利用钛尾矿回收金属钪和草酸的工艺流程如图所示。回答下列问题: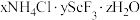 是“沉钪”过程中
是“沉钪”过程中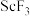 与氯化物形成的复盐沉淀,在强酸中部分溶解。
与氯化物形成的复盐沉淀,在强酸中部分溶解。
②“脱水除铵”是复盐沉淀的热分解过程。
③ 时,部分物质的相关信息如表所示:
时,部分物质的相关信息如表所示:
(1)“焙烧”时将固体粉碎的目的为________________ 。
(2)“焙烧”过程中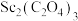 生成
生成 的化学方程式为
的化学方程式为_________________ 。
(3)“脱水除铵”过程中固体质量与温度的关系如图所示,其中在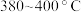 过程中会有白烟冒出,保温至无烟气产生,由图中数据可得
过程中会有白烟冒出,保温至无烟气产生,由图中数据可得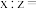
_______ 。

(4)传统制备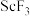 的方法是先得到
的方法是先得到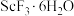 沉淀,再高温脱水得
沉淀,再高温脱水得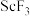 ,但通常含有
,但通常含有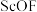 杂质,原因是
杂质,原因是_______________ (用化学方程式表示)。流程中“沉钪”后“脱水除铵”可制得纯度很高的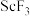 ,其原因是
,其原因是____________ 。
(5)将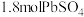 加到
加到 含有
含有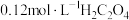 的废水中,发生的离子反应为
的废水中,发生的离子反应为 ,该反应的平衡常数的值
,该反应的平衡常数的值
________ 。
(6)滤饼经较浓硫酸处理后的“沉淀”是_______ (化学式)。
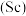 是一种稀土金属,钛尾矿经一系列处理后得到固体
是一种稀土金属,钛尾矿经一系列处理后得到固体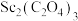 和主要成分是
和主要成分是 的废水,利用钛尾矿回收金属钪和草酸的工艺流程如图所示。回答下列问题:
的废水,利用钛尾矿回收金属钪和草酸的工艺流程如图所示。回答下列问题: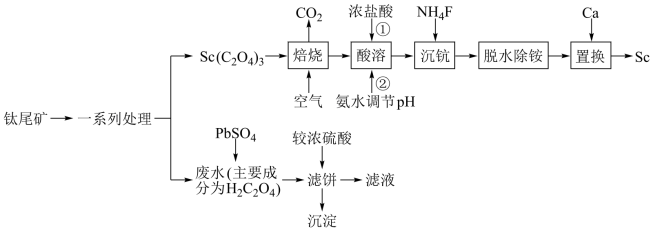
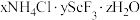 是“沉钪”过程中
是“沉钪”过程中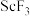 与氯化物形成的复盐沉淀,在强酸中部分溶解。
与氯化物形成的复盐沉淀,在强酸中部分溶解。②“脱水除铵”是复盐沉淀的热分解过程。
③
 时,部分物质的相关信息如表所示:
时,部分物质的相关信息如表所示:
|
|
|
|
|
|
|
|
(1)“焙烧”时将固体粉碎的目的为
(2)“焙烧”过程中
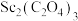 生成
生成 的化学方程式为
的化学方程式为(3)“脱水除铵”过程中固体质量与温度的关系如图所示,其中在
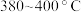 过程中会有白烟冒出,保温至无烟气产生,由图中数据可得
过程中会有白烟冒出,保温至无烟气产生,由图中数据可得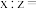

(4)传统制备
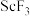 的方法是先得到
的方法是先得到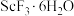 沉淀,再高温脱水得
沉淀,再高温脱水得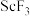 ,但通常含有
,但通常含有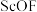 杂质,原因是
杂质,原因是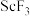 ,其原因是
,其原因是(5)将
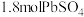 加到
加到 含有
含有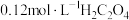 的废水中,发生的离子反应为
的废水中,发生的离子反应为 ,该反应的平衡常数的值
,该反应的平衡常数的值
(6)滤饼经较浓硫酸处理后的“沉淀”是
您最近一年使用:0次
名校
9 . 由下列实验操作及现象所得结论正确的是
| 实验操作及现象 | 结论 | |
| A | 向 粉末中滴加1 粉末中滴加1 盐酸,将产生的气体通入苯酚钠溶液,溶液变浑浊 盐酸,将产生的气体通入苯酚钠溶液,溶液变浑浊 | 酸性: 苯酚 苯酚 |
| B | 向0.1 HI溶液中滴加几滴淀粉溶液,再滴加几滴0.1 HI溶液中滴加几滴淀粉溶液,再滴加几滴0.1  溶液,溶液变蓝 溶液,溶液变蓝 | 氧化性: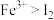 |
| C | 分别向浓度均为0.1 的 的 和 和 溶液中通入 溶液中通入 至饱和,前者无明显现象,后者生成沉淀 至饱和,前者无明显现象,后者生成沉淀 | 溶度积常数: |
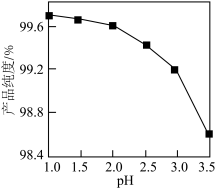
| D | 在20℃和40℃时,用pH计测得0.1  溶液的pH分别为9.66和9.37 溶液的pH分别为9.66和9.37 |  的水解常数: 的水解常数: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-29更新
|
764次组卷
|
3卷引用:山东省烟台市2024届高三一模化学试题
名校
10 . 钛酸钡( )具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。
 )具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微
)具有高介电常数和低介电损耗,是电子陶瓷中使用最广泛的材料之一,被誉为“电子陶瓷工业的支柱”。一种超细微 粉末的制备方法如下。
粉末的制备方法如下。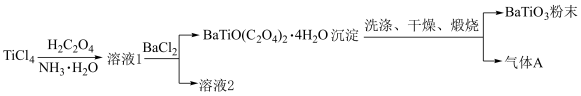
A.可用硝酸酸化的 溶液检验洗涤是否完全 溶液检验洗涤是否完全 |
| B.用溶液2提取的一种副产物可作肥料 |
| C.流程中的三步反应均为非氧化还原反应 |
D.向 中先加入 中先加入 后加入 后加入 的目的是防止 的目的是防止 水解 水解 |
您最近一年使用:0次