1 . 能促进水的电离,且水溶液呈酸性的是
A. | B.HClO | C. | D.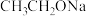 |
您最近一年使用:0次
名校
解题方法
2 . 钼是电子工业的重要材料,制备它的原料之一是钼铅矿(主要成分是PbMoO4,模拟部分工艺流如图:

已知:Mo有多种化合价,常见化合价有+2、+3、+4、+6;
(1)浸渣的主要成分是________ (填化学式)。
(2)写出流程中用热还原法制单质钼的化学方程式________ 。
(3)铵化时,加HNO3的作用是________ 。
(4)检验(NH4)2MoO4晶体洗净的方法是________ 。
(5)可循环利用的物质有________ (填化学式)。
(6)钼基硫化合物Cu2Mo6S8常用作锂离子电池正极材料,具有较高的功率密度和能量密度,该电池放电时的总反应为xLi+Cu2Mo6S8=LixCu2Mo6S8,写出该电池充电时阳极的电极反应式:________ 。

已知:Mo有多种化合价,常见化合价有+2、+3、+4、+6;
(1)浸渣的主要成分是
(2)写出流程中用热还原法制单质钼的化学方程式
(3)铵化时,加HNO3的作用是
(4)检验(NH4)2MoO4晶体洗净的方法是
(5)可循环利用的物质有
(6)钼基硫化合物Cu2Mo6S8常用作锂离子电池正极材料,具有较高的功率密度和能量密度,该电池放电时的总反应为xLi+Cu2Mo6S8=LixCu2Mo6S8,写出该电池充电时阳极的电极反应式:
您最近一年使用:0次
名校
3 . 利用下列装置进行实验,能达到实验目的的是


A.用甲制备并收集纯净的 |
| B.用乙比较碳元素与硫元素的非金属性强弱 |
| C.用丙提取溴水中的溴单质 |
D.用丁蒸发 溶液制备 溶液制备 |
您最近一年使用:0次
4 . 下列实验操作正确且能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 由 制备无水 制备无水 | 将 在HCl气流中加热 在HCl气流中加热 |
| B | 除去 中的 中的 气体 气体 | 依次通过盛有酸性 溶液和浓硫酸的洗气瓶 溶液和浓硫酸的洗气瓶 |
| C | 比较HClO和 的酸性强弱 的酸性强弱 | 室温下,用pH试纸测定同浓度的HClO和 溶液的pH 溶液的pH |
| D | 检验铝热反应(Al和 )反应后固体中是否含 )反应后固体中是否含 | 取反应后固体,溶于足量稀硫酸,滴加KSCN溶液,溶液不变红,说明不含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 碳酸亚铁(白色固体,难溶于水)是一种重要的工业原料,可用于制备补血剂乳酸亚铁。某研究小组通过下列实验,寻找利用复分解反应制备FeCO3的最佳方案:
(1)实验Ⅰ中红褐色沉淀产生的原因可用如下反应表示,请补全反应:_____ 。
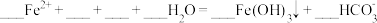 。
。
(2)实验Ⅱ中产生FeCO3的离子方程式为_____ 。
(3)为了探究实验Ⅲ中 起的作用,甲同学设计了实验Ⅳ进行探究:
起的作用,甲同学设计了实验Ⅳ进行探究:
对比实验Ⅱ、Ⅲ、Ⅳ,甲同学得出结论: 水解产生
水解产生 ,降低溶液pH,减少了副产物Fe(OH)2的产生。
,降低溶液pH,减少了副产物Fe(OH)2的产生。
乙同学认为该实验方案不够严谨,应补充的对比实验操作是:_____ ,再取该溶液一滴管,与2mL1mol/LNaHCO3溶液混合。
(4)小组同学进一步讨论认为,定性实验现象并不能直接证明实验Ⅲ中FeCO3的纯度最高,需要利用如图所示的装置进行定量测定。分别将实验Ⅰ、Ⅱ、Ⅲ中的沉淀进行过滤、洗涤、干燥后称量,然后转移至A处的广口瓶中。
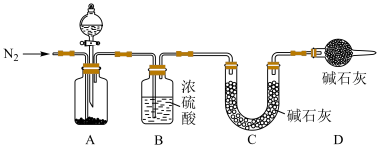
①A中分液漏斗中的试剂为_____ 。
②为测定FeCO3的纯度,除样品总质量外,还需测定的物理量是_____ 。
(5)实验反思:经测定,实验Ⅲ中的FeCO3纯度高于实验Ⅰ和实验Ⅱ.通过以上实验分析,制备FeCO3实验成功的关键因素是_____ 。
| 实验 | 试剂 | 现象 | |
| 滴管 | 试管 | ||
 | 0.8mol/LFeSO4溶液(pH=4.5) | 1mol/LNa2CO3溶液(pH=11.9) | 实验Ⅰ:立即产生灰绿色沉淀,5min后出现明显的红褐色 |
| 0.8mol/LFeSO4溶液(pH=4.5) | 1mol/LNaHCO3溶液(pH=8.6) | 实验Ⅱ:产生白色沉淀及少量无色气泡,2min后出现明显的灰绿色。 | |
| 0.8mol/L(NH4)2Fe(SO4)2溶液(pH=4.0) | 1mol/LNaHCO3溶液(pH=8.6) | 实验Ⅲ:产生白色沉淀及无色气泡,较长时间保持白色 | |
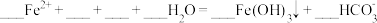 。
。(2)实验Ⅱ中产生FeCO3的离子方程式为
(3)为了探究实验Ⅲ中
 起的作用,甲同学设计了实验Ⅳ进行探究:
起的作用,甲同学设计了实验Ⅳ进行探究:| 操作 | 现象 | |
| 实验Ⅳ | 向0.8mol/LFeSO4溶液中加入 的混合溶液(已知 的混合溶液(已知 对实验无影响)。再取该溶液一滴管与2mL1mol/LNaHCO3溶液混合。 对实验无影响)。再取该溶液一滴管与2mL1mol/LNaHCO3溶液混合。 | 与实验Ⅲ现象相同 |
 水解产生
水解产生 ,降低溶液pH,减少了副产物Fe(OH)2的产生。
,降低溶液pH,减少了副产物Fe(OH)2的产生。乙同学认为该实验方案不够严谨,应补充的对比实验操作是:
(4)小组同学进一步讨论认为,定性实验现象并不能直接证明实验Ⅲ中FeCO3的纯度最高,需要利用如图所示的装置进行定量测定。分别将实验Ⅰ、Ⅱ、Ⅲ中的沉淀进行过滤、洗涤、干燥后称量,然后转移至A处的广口瓶中。

①A中分液漏斗中的试剂为
②为测定FeCO3的纯度,除样品总质量外,还需测定的物理量是
(5)实验反思:经测定,实验Ⅲ中的FeCO3纯度高于实验Ⅰ和实验Ⅱ.通过以上实验分析,制备FeCO3实验成功的关键因素是
您最近一年使用:0次
名校
6 . 室温时,用 稀盐酸滴定
稀盐酸滴定 溶液,已知:
溶液,已知: 溶液中水的电离程度随所加稀盐酸的体积变化如图所示,则下列有关说法正确的是
溶液中水的电离程度随所加稀盐酸的体积变化如图所示,则下列有关说法正确的是

 稀盐酸滴定
稀盐酸滴定 溶液,已知:
溶液,已知: 溶液中水的电离程度随所加稀盐酸的体积变化如图所示,则下列有关说法正确的是
溶液中水的电离程度随所加稀盐酸的体积变化如图所示,则下列有关说法正确的是
| A.可选取酚酞作为滴定指示剂 |
| B.M点溶液的pH>7 |
| C.图中Q点水的电离程度最大 |
D.M点, |
您最近一年使用:0次
名校
7 . 关于海水综合利用,下列说法正确的是
A.粗盐提纯所加沉淀剂可依次为 溶液、 溶液、 溶液、 溶液、 溶液 溶液 |
B.海水提镁过程中将 直接灼烧即可制得无水 直接灼烧即可制得无水 |
C.海水提溴过程中每获得 共需要消耗标准状况下 共需要消耗标准状况下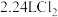 |
| D.海水淡化常用的主要方法有蒸馏法、电渗析法和离子交换法 |
您最近一年使用:0次
2023-05-14更新
|
186次组卷
|
3卷引用:湖南省株洲市第一中学2021届高三第一次模拟检测化学试题
8 . 尖晶石矿的主要成分为 (含
(含 杂质)。已知:
杂质)。已知: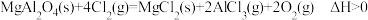 。该反应难以发生,但采用“加炭氯化法”可以制备
。该反应难以发生,但采用“加炭氯化法”可以制备 和
和 ,同时还可得到副产物
,同时还可得到副产物 (
( 沸点为
沸点为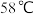 ,
, 在
在 升华):
升华):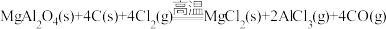 。下列说法
。下列说法不正确 的是
 (含
(含 杂质)。已知:
杂质)。已知: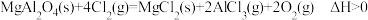 。该反应难以发生,但采用“加炭氯化法”可以制备
。该反应难以发生,但采用“加炭氯化法”可以制备 和
和 ,同时还可得到副产物
,同时还可得到副产物 (
( 沸点为
沸点为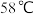 ,
, 在
在 升华):
升华):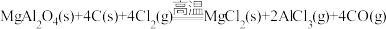 。下列说法
。下列说法| A.制备时要保持无水环境 |
B.输送气态产物的管道温度要保持在 以上 以上 |
| C.氯化时加炭,既增大了反应的趋势,又为氯化提供了能量 |
D.为避免产生大量 ,反应过程中需保持炭过量 ,反应过程中需保持炭过量 |
您最近一年使用:0次
2022-06-14更新
|
4572次组卷
|
10卷引用:湖南省株洲市第二中学2021届高三下学期第三次模拟考试化学试卷
湖南省株洲市第二中学2021届高三下学期第三次模拟考试化学试卷2022年6月浙江省普通高校招生选考化学试题(已下线)2022年浙江省6月高考真题变式题21-25(已下线)考点15 铝及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第14练 无机非金属材料-2023年高考化学一轮复习小题多维练(全国通用)浙江省浙里卷天下2022-2023学年高三上学期10月联考化学试题(已下线)易错点33 物质的制备-备战2023年高考化学考试易错题(已下线)专题卷11 化学反应速率与化学平衡归因分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)考点15 铝及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
解题方法
9 . 宏观辨识与微观探析是化学学科核心素养之一,下列指定反应的离子方程式书写正确的是
A.向 溶液中滴加少量 溶液中滴加少量 溶液: 溶液: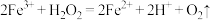 |
B.向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解: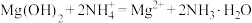 |
C. 溶液与过量 溶液与过量 溶液反应: 溶液反应: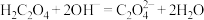 |
D.将 溶液与 溶液与 溶液混合: 溶液混合: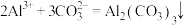 |
您最近一年使用:0次
名校
解题方法
10 . 《本草纲目》中有“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”记载。有关说法错误的是
| A.薪柴之灰可做钾肥 | B.取碱浇衣存在水解反应 |
| C.碱浣衣与肥皂浣衣原理不同 | D.上述过程涉及溶解、过滤、蒸馏操作 |
您最近一年使用:0次
2022-05-07更新
|
267次组卷
|
4卷引用:湖南省株洲市第一中学2021届高三下学期第三次模拟检测化学试题



