名校
解题方法
1 . 以废旧锂离子电池(主要成分为 )为原料制备棒状草酸钴晶体(
)为原料制备棒状草酸钴晶体( ,微溶于水,溶解度随温度升高而逐渐增大)的一种方法如下图所示,该法经济可行,为工业化回收废旧锂电池中有色金属提供了依据。
,微溶于水,溶解度随温度升高而逐渐增大)的一种方法如下图所示,该法经济可行,为工业化回收废旧锂电池中有色金属提供了依据。 外,还含
外,还含 、
、 ,
, ,
, ,
, ,
, 等离子;
等离子;
② ,
,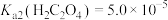 ;
;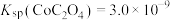 。
。
回答下列问题:
(1)“浸出”时, 与
与 、稀硫酸反应中氧化剂与还原剂的物质的量之比为
、稀硫酸反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)“水解沉淀铝铜”时,沉淀铝反应的离子方程式为___________ 。
(3)沉淀2的成分为 和
和___________ ,“氧化沉淀铁锰”时,生成 的离子方程式为
的离子方程式为___________ 。
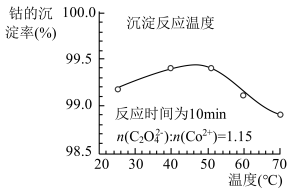
(4)“沉钴”时,温度与钴的沉淀率的关系如图所示,沉淀反应时间为10 min,反应温度为50℃以上时,温度升高,而钴的沉淀率下降,可能原因为___________ 。 溶液代替
溶液代替 ,反应为
,反应为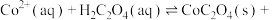
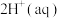 ,则该反应的平衡常数为
,则该反应的平衡常数为___________ ,若平衡时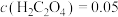 mol⋅L-1,
mol⋅L-1, ,则此时Co2+是否沉淀完全?
,则此时Co2+是否沉淀完全?___________ (填“是”或“否”,离子浓度≤10-5 mol⋅L-1即可认为沉淀完全)。
 )为原料制备棒状草酸钴晶体(
)为原料制备棒状草酸钴晶体( ,微溶于水,溶解度随温度升高而逐渐增大)的一种方法如下图所示,该法经济可行,为工业化回收废旧锂电池中有色金属提供了依据。
,微溶于水,溶解度随温度升高而逐渐增大)的一种方法如下图所示,该法经济可行,为工业化回收废旧锂电池中有色金属提供了依据。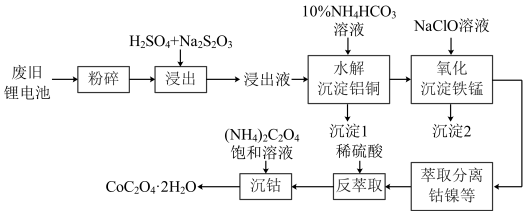
 外,还含
外,还含 、
、 ,
, ,
, ,
, ,
, 等离子;
等离子;②
 ,
,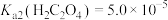 ;
;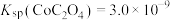 。
。回答下列问题:
(1)“浸出”时,
 与
与 、稀硫酸反应中氧化剂与还原剂的物质的量之比为
、稀硫酸反应中氧化剂与还原剂的物质的量之比为(2)“水解沉淀铝铜”时,沉淀铝反应的离子方程式为
(3)沉淀2的成分为
 和
和 的离子方程式为
的离子方程式为(4)“沉钴”时,温度与钴的沉淀率的关系如图所示,沉淀反应时间为10 min,反应温度为50℃以上时,温度升高,而钴的沉淀率下降,可能原因为
 溶液代替
溶液代替 ,反应为
,反应为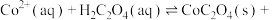
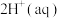 ,则该反应的平衡常数为
,则该反应的平衡常数为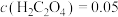 mol⋅L-1,
mol⋅L-1, ,则此时Co2+是否沉淀完全?
,则此时Co2+是否沉淀完全?
您最近一年使用:0次
2024-02-01更新
|
336次组卷
|
2卷引用:山西省忻州市2023-2024学年高三上学期1月期末理综试题-高中化学
名校
解题方法
2 . 根据下列事实得出的相应结论错误的是
| 选项 | 事实 | 结论 |
| A | 25℃时分别测定浓度均为0.1mol·L-1的NaCl溶液和CH3COONH4溶液的pH,pH都等于7 | 两溶液中水的电离程度相等 |
| B | t ℃时,反应①:Br2(g)+ H2(g)  2HBr(g) K=5. 6×107;反应②:I2(g)+ H2(g) 2HBr(g) K=5. 6×107;反应②:I2(g)+ H2(g)  2HI(g) K=43 2HI(g) K=43 | 相同条件下。平衡体系中卤化氢所占的比例:反应①>反应② |
| C | 向漂白粉溶液中通入足量SO2气体,产生白色沉淀 | 还原性:SO2>Cl- |
| D | 常温下,将50mL苯与50mLCH3COOH混合,所得混合液的体积为101 mL | 混合过程中削弱了CH3COOH分子间的氢键。且苯与CH3COOH分子间的范德华力弱于CH3COOH分子间的氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-22更新
|
90次组卷
|
2卷引用:山西省大同市2023届高三下学期三模理科综合化学试题
3 . 以电解铝废渣(主要含AlF3、NaF、LiF、CaO)为原料,制备电池级碳酸锂的工艺流程如下:
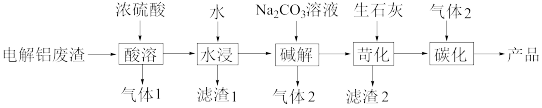
已知: AlF3、LiF难溶于水,LiOH溶于水,Li2CO3微溶于水,Ksp(Li2CO3)
 2.5×10-2、Ksp( CaCO3) = 2.8×10-9。回答下列问题:
2.5×10-2、Ksp( CaCO3) = 2.8×10-9。回答下列问题:
(1)①电解氧化铝生成铝的化学方程式为___________ ,无碳电解铝技术是利用陶瓷材料替代碳作阳极,该技术的优点之一是___________ 。
②已知AlCl3可形成共价分子, AlF3为离子晶体,从电负性的角度解释其原因:_____________ 。
(2)“气体1”是___________ ( 填化学式,下同),“滤渣1”的主要成分是___________ 。
(3)已知“碱解”同时生成白色沉淀,写出生成“气体2”的离子方程式___________ 。
(4)“苛化”中存在如下反应:Li2CO3(s)+Ca2+(aq) 2Li+(aq)+ CaCO3(s)。通过计算解释生石灰能使Li2CO3完全转化的原因:
2Li+(aq)+ CaCO3(s)。通过计算解释生石灰能使Li2CO3完全转化的原因:______________ 。
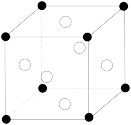
(5)Al-Li合金具有低密度、耐腐蚀等特点,已成为航天器的重要结构材料。一种Al3Li合金的晶胞如图所示,其中白球代表的是___________ ;若其晶胞参数为apm,则该合金的晶体密度为___________ g·cm-3 (列出计算式,阿伏加德罗常数用NA表示)。

已知: AlF3、LiF难溶于水,LiOH溶于水,Li2CO3微溶于水,Ksp(Li2CO3)

 2.5×10-2、Ksp( CaCO3) = 2.8×10-9。回答下列问题:
2.5×10-2、Ksp( CaCO3) = 2.8×10-9。回答下列问题:(1)①电解氧化铝生成铝的化学方程式为
②已知AlCl3可形成共价分子, AlF3为离子晶体,从电负性的角度解释其原因:
(2)“气体1”是
(3)已知“碱解”同时生成白色沉淀,写出生成“气体2”的离子方程式
(4)“苛化”中存在如下反应:Li2CO3(s)+Ca2+(aq)
 2Li+(aq)+ CaCO3(s)。通过计算解释生石灰能使Li2CO3完全转化的原因:
2Li+(aq)+ CaCO3(s)。通过计算解释生石灰能使Li2CO3完全转化的原因:(5)Al-Li合金具有低密度、耐腐蚀等特点,已成为航天器的重要结构材料。一种Al3Li合金的晶胞如图所示,其中白球代表的是

您最近一年使用:0次
4 . 某小组同学利用图示装置进行实验,试管中实验现象正确的是
| a | b | c | 试管中的现象 | 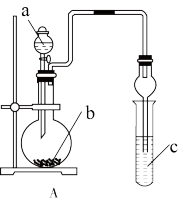 | |
| A | 稀硫酸 | 碳酸钠 | 饱和食盐水 | 产生大量沉淀 | |
| B | 浓氨水 | 氧化钙 | 硫酸铝溶液 | 先产生白色沉淀,后沉淀消失 | |
| C | 浓盐酸 | 高锰酸钾 | 品红溶液 | 溶液褪色,加热后红色复现 | |
| D | AlCl3 溶液 | Na2S溶液 | 滴有 K3[Fe(CN)6]的FeCl3溶液 | 溶液颜色变浅,且有蓝色沉淀生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 根据下列实验现象能得出相应实验结论的是
| 选项 | 实验现象 | 实验结论 |
| A | 用锌与稀硫酸反应制氢气时,滴入几滴硫酸铜溶液,反应速率加快 | Cu2+具有催化作用 |
| B | 向含有酚酞的Na2CO3溶液中加入溶液M,红色褪去 | 溶液M一定呈酸性 |
| C | 向铁片上滴1滴含有酚酞的食盐水,一段时间后溶液边缘变红 | 铁发生了吸氧腐蚀 |
| D | 向Al2(SO4)3溶液中滴加Na2S溶液,有白色沉淀产生 | 白色沉淀是Al2S3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-18更新
|
107次组卷
|
2卷引用:山西省大同市2021-2022学年高二上学期期末质量检测化学试题



