名校
1 . 铁、铜及其化合物在日常生活及工业生产中有着非常广泛的用途。回答下列问题:
I.FeCl3是常用的金属蚀刻剂和净水剂。
(1)FeCl3在溶液中分三步水解:
Fe3++H2O Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O
 +H+ K2
+H+ K2
 +H2O
+H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是_______ 。
(2)配制FeCl3溶液时,常将FeCl3晶体溶于浓盐酸中,使用时加蒸馏水稀释至指定浓度。某同学误将FeCl3直接放入自来水(含有Mg2+、Ca2+、 、Cl-等杂质离子)中,看到红褐色沉淀和大量气泡,试解释出现该现象的原因
、Cl-等杂质离子)中,看到红褐色沉淀和大量气泡,试解释出现该现象的原因_______ (用离子方程式表示)。
II. CuCl2 常用作电镀添加剂、催化剂及饲料添加剂。
(3)①25℃时Fe(OH)2、Fe(OH)3、Cu(OH)2的Ksp如表格所示,计算当溶液中Fe2+、Cu2+离子浓度均为0.1 mol/L时,Fe(OH)2沉淀完全及Cu(OH)2开始沉淀时的pH值(已知lg2=0.3)
②在CuCl2溶液中含有少量FeCl2杂质时 _______ (填“能"、“不能”)通过调节溶液pH的方法来除去,理由是_______ 。
③为了除去CuCl2溶液中含有的少量FeCl2,可以用_______ (填化学式,写出一种即可) 将FeCl2氧化为FeCl3,然后通过加入_______ (填化学式,出一种即可)调控溶液pH值,使_______ <pH<_______ ,将FeCl3转化为Fe(OH)3除去。
I.FeCl3是常用的金属蚀刻剂和净水剂。
(1)FeCl3在溶液中分三步水解:
Fe3++H2O
 Fe(OH)2++H+ K1
Fe(OH)2++H+ K1Fe(OH)2++H2O

 +H+ K2
+H+ K2 +H2O
+H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3以上水解反应的平衡常数K1、K2、K3由大到小的顺序是
(2)配制FeCl3溶液时,常将FeCl3晶体溶于浓盐酸中,使用时加蒸馏水稀释至指定浓度。某同学误将FeCl3直接放入自来水(含有Mg2+、Ca2+、
 、Cl-等杂质离子)中,看到红褐色沉淀和大量气泡,试解释出现该现象的原因
、Cl-等杂质离子)中,看到红褐色沉淀和大量气泡,试解释出现该现象的原因II. CuCl2 常用作电镀添加剂、催化剂及饲料添加剂。
(3)①25℃时Fe(OH)2、Fe(OH)3、Cu(OH)2的Ksp如表格所示,计算当溶液中Fe2+、Cu2+离子浓度均为0.1 mol/L时,Fe(OH)2沉淀完全及Cu(OH)2开始沉淀时的pH值(已知lg2=0.3)
| 分子式 | Ksp | 开始沉淀时的pH值 | 沉淀完全时的pH值 |
| Fe(OH)2 | 4.0×10-17 | 6.3 | a= |
| Fe(OH)3 | 2.79×10-39 | 1.5 | 2.8 |
| Cu(OH)2 | 1.6×10-20 | b= | 6.6 |
③为了除去CuCl2溶液中含有的少量FeCl2,可以用
您最近一年使用:0次
2023-01-06更新
|
799次组卷
|
2卷引用:辽宁省东北育才学校高中部2022-2023学年高二上学期期末考试化学试题
2 . 以镁铝复合氧化物(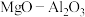 )为载体的负载型镍铜双金属催化剂(Ni-Cu/
)为载体的负载型镍铜双金属催化剂(Ni-Cu/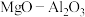 )是一种新型的高效加氢或脱氢催化剂,其制备流程如下:
)是一种新型的高效加氢或脱氢催化剂,其制备流程如下:
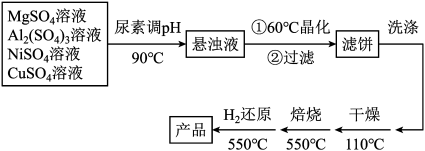
已知:常温下, ,
,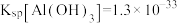 。回答下列问题:
。回答下列问题:
(1)在元素周期表中,Ni在______ (填“s”“p”“d”“f”或“ds”)区,基态铜原子的价电子排布式为____________ 。
(2)在加热条件下,尿素 在水中发生水解反应,放出
在水中发生水解反应,放出_________ 和_________ (填化学式)两种气体。
(3)“晶化”过程中,需保持恒温60℃,可采用的加热方式为___________ 。
(4)常温下,若“悬浊液”中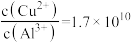 ,则溶液的
,则溶液的
_______ 。
(5) 在消防工业中常用于与小苏打、发泡剂组成泡沫灭火剂,请写出其灭火原理
在消防工业中常用于与小苏打、发泡剂组成泡沫灭火剂,请写出其灭火原理____________________________________ (用离子方程式表示)。
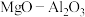 )为载体的负载型镍铜双金属催化剂(Ni-Cu/
)为载体的负载型镍铜双金属催化剂(Ni-Cu/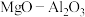 )是一种新型的高效加氢或脱氢催化剂,其制备流程如下:
)是一种新型的高效加氢或脱氢催化剂,其制备流程如下:
已知:常温下,
 ,
,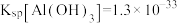 。回答下列问题:
。回答下列问题:(1)在元素周期表中,Ni在
(2)在加热条件下,尿素
 在水中发生水解反应,放出
在水中发生水解反应,放出(3)“晶化”过程中,需保持恒温60℃,可采用的加热方式为
(4)常温下,若“悬浊液”中
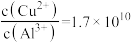 ,则溶液的
,则溶液的
(5)
 在消防工业中常用于与小苏打、发泡剂组成泡沫灭火剂,请写出其灭火原理
在消防工业中常用于与小苏打、发泡剂组成泡沫灭火剂,请写出其灭火原理
您最近一年使用:0次
名校
解题方法
3 . 常温下pH=1的某溶液A中含有 、K+、Na+、Fe3+、Al3+、Fe2+、
、K+、Na+、Fe3+、Al3+、Fe2+、 、
、 、Cl-、I-、
、Cl-、I-、 中的几种,且溶液中各离子的物质的量浓度均为0.1moL/L,现取该溶液进行有关实验,实验结果如图所示:下列有关说法正确的是
中的几种,且溶液中各离子的物质的量浓度均为0.1moL/L,现取该溶液进行有关实验,实验结果如图所示:下列有关说法正确的是

 、K+、Na+、Fe3+、Al3+、Fe2+、
、K+、Na+、Fe3+、Al3+、Fe2+、 、
、 、Cl-、I-、
、Cl-、I-、 中的几种,且溶液中各离子的物质的量浓度均为0.1moL/L,现取该溶液进行有关实验,实验结果如图所示:下列有关说法正确的是
中的几种,且溶液中各离子的物质的量浓度均为0.1moL/L,现取该溶液进行有关实验,实验结果如图所示:下列有关说法正确的是
A.该溶液中一定有上述离子中的 、Al3+、 、Al3+、 、Cl-四种离子 、Cl-四种离子 |
| B.实验消耗Cu14.4g,则生成气体丁的体积为3.36L |
| C.可用焰色试验确定原溶液中是否含有Na+,若含有Na+灼烧时火焰呈黄色,是因为基态的电子跃迁激发态若未见黄色火焰则无Na+ |
| D.一定没有Fe3+,但是无法确定是否含有I- |
您最近一年使用:0次
名校
解题方法
4 . 下列离子因发生相互促进的水解反应而不能大量共存的是
A.K+、S2-、Al3+、AlO | B.MnO 、Na+、SO 、Na+、SO 、K+ 、K+ |
C.SO 、Fe3+、S2-、K+ 、Fe3+、S2-、K+ | D.Fe2+、Cl-、H+、NO |
您最近一年使用:0次
2022-11-22更新
|
363次组卷
|
6卷引用:辽宁省重点高中沈阳市郊联体2022-2023学年高二上学期期中考试化学试题
5 . 下列实验操作、实验现象及解释或结论都正确且有因果关系的是
实验操作 | 实验现象 | 解释或结论 | |
A | 向饱和硼酸溶液中加入少量 | 无气泡冒出 | 酸性:碳酸>硼酸 |
B | 将等物质的量的 | 有白色沉淀和气体生成 | 二者水解相互促进生成氢氧化铝沉淀 |
C | 向 | 先生成白色沉淀,后有黄色沉淀生成 |
|
D | 常温下,用玻璃棒蘸取某浓度 |
| 该 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-19更新
|
282次组卷
|
2卷引用:辽宁省沈阳市五校协作体2022-2023学年高二上学期期中考试化学试题
名校
解题方法
6 . 室温下,下列各组离子在指定溶液中一定能大量共存的是
A.常温下 =10-12的溶液:K+、Ba2+、Cl-、Br- =10-12的溶液:K+、Ba2+、Cl-、Br- |
B.在含有大量Al3+溶液中: 、Na+、Cl-、 、Na+、Cl-、 |
C.常温下pH=7的溶液中:Na+、Cl-、 、Fe3+ 、Fe3+ |
D.常温下由水电离产生的c(OH-)=10-12mol•L-1的溶液:K+、Al3+、Cl-、 |
您最近一年使用:0次
2022-11-18更新
|
429次组卷
|
3卷引用:辽宁省六校协作体2022-2023学年高二上学期期中考试化学试题
名校
7 . 室温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1mol/LNaHCO3溶液:K+、Al3+、Cl―、SO |
B.使甲基橙变红的溶液:Mg2+、Na+、SO 、NO 、NO |
C.pH=1的溶液:K+、Fe2+、Cl―、NO |
D.与铝反应能产生大量氢气的溶液:Na+、NH 、Cl―、NO 、Cl―、NO |
您最近一年使用:0次
名校
解题方法
8 . 室温下,下列各组离子在指定溶液中能大量共存的是
A.含有FeCl3的溶液:NH 、SCN-、OH-、Mg2+ 、SCN-、OH-、Mg2+ |
B.含有NaHCO3的溶液:Cl-、NO 、Al3+、Ba2+ 、Al3+、Ba2+ |
C.澄清透明溶液中: SO 、K+、 、K+、 |
D.含有K2Cr2O7的溶液: 、SO 、SO 、K+、 、K+、 |
您最近一年使用:0次
2022-11-01更新
|
205次组卷
|
2卷引用:辽宁省沈阳市东北育才学校高中部2022-2023学年高二上学期第二次月考化学试题
解题方法
9 . 下列离子方程式正确的是
A.泡沫灭火器的原理: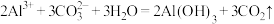 |
B. 与 与 反应制备 反应制备 |
C.向 溶液中滴加过量 溶液中滴加过量 溶液: 溶液: |
D.硫酸酸化的 溶液与双氧水反应后溶液褪色: 溶液与双氧水反应后溶液褪色: |
您最近一年使用:0次
10 . 锂电池具有广泛应用。用废铝渣(含金属铝、锂盐等)获得电池级 的一种工艺流程如图(部分物质已略去):
的一种工艺流程如图(部分物质已略去):

下列说法不正确 的是
 的一种工艺流程如图(部分物质已略去):
的一种工艺流程如图(部分物质已略去):
下列说法
A.用焰色试验检验①加热后得到滤液中的 ,是因为电子从激发态跃迁至基态或较低能级时以光的形式释放能量 ,是因为电子从激发态跃迁至基态或较低能级时以光的形式释放能量 |
B.②中生成 的离子方程式: 的离子方程式: |
C.由③推测溶解度: |
D.依据对角线规则, 微溶于水可以推测 微溶于水可以推测 在水中溶解度不大 在水中溶解度不大 |
您最近一年使用:0次
2022-08-03更新
|
375次组卷
|
4卷引用:辽宁省抚顺市2021-2022学年高二上学期期末考试化学试题
辽宁省抚顺市2021-2022学年高二上学期期末考试化学试题辽宁省沈阳市同泽中学2022-2023学年高二12月月考化学试题(已下线)3.4.2 沉淀溶解平衡的应用-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)湖北省重点高中智学联盟2022-2023学年高二上学期期末考试化学试题

 粉末
粉末 溶液与
溶液与 溶液滴加
溶液滴加 溶液,再向其中滴加
溶液,再向其中滴加 溶液
溶液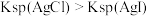
 试纸中央,与标准比色卡对比
试纸中央,与标准比色卡对比


