1 . 绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和 内循环。工艺流程如下:
内循环。工艺流程如下:
(1)Al在元素周期表中的位置为___________ ;“高温连续氧化”过程中发生的氧化还原反应的化学方程式是___________ 。
(2)“固体III”的主要成分是___________ (填化学式)。
(3)已知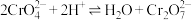 ,则“工序③”中通入
,则“工序③”中通入___________ (填“足量”或“少量”)的气体A更有利于得到重铬酸盐;流程中可以循环使用的物质除气体A外还有___________ (填化学式)。
(4)“工序④”中发生反应的离子方程式为___________ ;常温常压下,“工序④”的溶液中铝元素恰好完全转化为沉淀的pH为8.37,则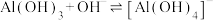

___________ 。(通常认为溶液中离子浓度小于 时沉淀完全)
时沉淀完全)
 内循环。工艺流程如下:
内循环。工艺流程如下: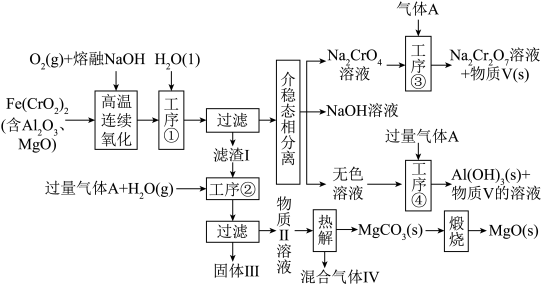
(1)Al在元素周期表中的位置为
(2)“固体III”的主要成分是
(3)已知
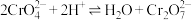 ,则“工序③”中通入
,则“工序③”中通入(4)“工序④”中发生反应的离子方程式为
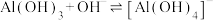

 时沉淀完全)
时沉淀完全)
您最近一年使用:0次
名校
2 . 室温下,下列实验方案能达到探究目的的是
| 选项 | 探究目的 | 探究方案 |
| A | 证明丁烯醛中含碳碳双键 | 向丁烯醛 中加入 中加入酸性高锰酸钾溶液,观察溶液颜色变化 |
| B | 比较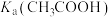 和 和 的大小 的大小 | 向 溶液中滴加 溶液中滴加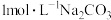 溶液,观察是否产生气泡 溶液,观察是否产生气泡 |
| C | 比较 与 与 氧化性强弱 氧化性强弱 | 向 溶液中滴入硫酸酸化的 溶液中滴入硫酸酸化的 溶液,观察溶液颜色变化 |
| D | 探究浓度对 溶液水解程度的影响 溶液水解程度的影响 | 向 的 的 溶液中滴加酚酞溶液 溶液中滴加酚酞溶液观察现象,再加入少量  固体,观察颜色变化 固体,观察颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 往 溶液中滴加几滴浓硫酸,溶液由橙色变为黄色 溶液中滴加几滴浓硫酸,溶液由橙色变为黄色 |  呈橙色, 呈橙色, 呈黄色 呈黄色 |
| B | 将浓硫酸加入蔗糖中形成多孔炭 | 浓硫酸具有强氧化性和脱水性 |
| C | 低温石英(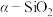 )制作石英手表 )制作石英手表 |  属于共价晶体,熔点高 属于共价晶体,熔点高 |
| D | 用钨钢钻头给混凝土墙面钻孔 | 合金硬度比其组成的纯金属低 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 乙氨酸( )是一种两性有机物,可与盐酸反应生成盐酸盐(
)是一种两性有机物,可与盐酸反应生成盐酸盐( )。已知
)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是
 )是一种两性有机物,可与盐酸反应生成盐酸盐(
)是一种两性有机物,可与盐酸反应生成盐酸盐( )。已知
)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是A.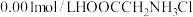 水溶液的pH=3 水溶液的pH=3 |
B.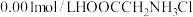 水溶液加水稀释,pH升高 水溶液加水稀释,pH升高 |
C. 在水中的电离方程式为: 在水中的电离方程式为: |
D. 水溶液中: 水溶液中: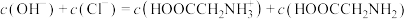 |
您最近一年使用:0次
5 . 25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)_______ 。(单项)
A.氨水与氯化铵发生化学反应
B.氯化铵溶液水解显酸性,增加了c(H+)
C.铵根离子浓度增大,抑制了氨水的电离,使c(OH-)减小
A.氨水与氯化铵发生化学反应
B.氯化铵溶液水解显酸性,增加了c(H+)
C.铵根离子浓度增大,抑制了氨水的电离,使c(OH-)减小
您最近一年使用:0次
6 . 下列方案设计、现象和结论都正确的是
| 实验 | 目的 | 方案设计 | 现象和结论 |
| ① | 探究压强对 与 与 平衡的影响 平衡的影响 | 快速压缩装有 、 、 平衡混合气体的针筒 平衡混合气体的针筒 | 如果气体颜色变深,则增大压强,平衡向生成 的方向移动 的方向移动 |
| ② | 探究 与 与 氧化性的强弱 氧化性的强弱 | 向 和 和 的混合溶液中滴入 的混合溶液中滴入 酸化的 酸化的 溶液 溶液 | 溶液变红,说明氧化性: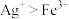 |
| ③ | 验证 溶液中存在水解平衡 溶液中存在水解平衡 | 取2  溶液于试管中,加2滴酚酞,再加入少量 溶液于试管中,加2滴酚酞,再加入少量 固体 固体 | 如果溶液红色变浅,则 溶液中存在水解平衡 溶液中存在水解平衡 |
| ④ | 相同温度下,比较 与 与 的酸性强弱 的酸性强弱 | 向等体积的水中分别通入 、 、 至饱和,再用 至饱和,再用 计测定两种溶液的 计测定两种溶液的 | 如果通 后所得溶液的 后所得溶液的 小,则 小,则 的酸性比弱 的酸性比弱 |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
7 . 安息香酸(HR)是最简单的一元芳香酸,其钠盐(用NaR表示)的水溶液呈碱性。已知常温下,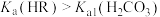 。下列说法正确的是
。下列说法正确的是
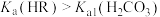 。下列说法正确的是
。下列说法正确的是A.常温下, HR水溶液的 HR水溶液的 |
| B.向NaR水溶液中加水稀释,溶液的pH升高 |
C.NaR水溶液中,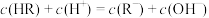 |
D.常温下,NaR溶液的碱性比同浓度的 溶液弱 溶液弱 |
您最近一年使用:0次
2024高三下·全国·专题练习
8 . 某工厂采用辉铋矿(主要成分为 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制各
)联合焙烧法制各 和
和 ,工艺流程如下:
,工艺流程如下: 分解为
分解为 ,
, 转变为
转变为 ;
;
②金属活动性: ;
;
③相关金属离子形成氢氧化物的 范围如下:
范围如下:
“酸浸”中过量浓盐酸的作用为:①充分浸出 和
和 ;②
;②_______ 。
 ,含有
,含有 、
、 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )联合焙烧法制各
)联合焙烧法制各 和
和 ,工艺流程如下:
,工艺流程如下: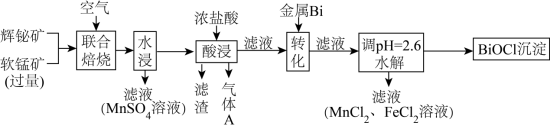
 分解为
分解为 ,
, 转变为
转变为 ;
;②金属活动性:
 ;
;③相关金属离子形成氢氧化物的
 范围如下:
范围如下:开始沉淀 | 完全沉淀 | |
 | 6.5 | 8.3 |
 | 1.6 | 2.8 |
 | 8.1 | 10.1 |
 和
和 ;②
;②
您最近一年使用:0次
9 . 下列对实验设计的评价错误的是
| 选项 | 实验设计 | 实验评价 |
| A. | 将含有二氧化硫的气体通入酸性高锰酸钾中,然后加入足量氯化钡溶液。通过测定白色沉淀的质量,可推算二氧化硫的物质的量 | 不合理,酸性高锰酸钾中的稀硫酸会与氯化钡产生沉淀 |
| B. | 实验室用浓硫酸和乙醇制取乙烯时,若要检验所得气体含有CH2=CH2,可将混合气体干燥后,通入溴的四氯化碳溶液中。若溶液褪色,则证明有乙烯 | 合理,混合气体中,只有乙烯可使溴的四氯化碳溶液褪色 |
| C. | 常温下,用pH计分别测定等体积 CH3COONH4溶液和 CH3COONH4溶液和 CH3COONH4溶液的pH.通过比较pH值,探究浓度对水的电离程度的影响 CH3COONH4溶液的pH.通过比较pH值,探究浓度对水的电离程度的影响 | 合理 |
| D. | 探究浓度对反应速率的影响,向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL5%H2O2溶液。通过观察现象,探究浓度对反应速率的影响 | 不合理,该实验无明显现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-16更新
|
420次组卷
|
3卷引用:2024年辽宁省抚顺市普通高中高三下学期模拟考试化学试卷
10 . 一种利用配合物消除氮氧化物污染的反应为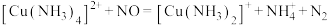
 。设
。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
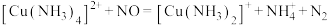
 。设
。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.键角: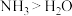 |
B.1mol 中含有 中含有 键的数目为 键的数目为 |
C.同温下 的数目:1L0.5mol/L 的数目:1L0.5mol/L 溶液>2L0.25mol/L 溶液>2L0.25mol/L 溶液 溶液 |
D.标准状况下,每生成22.4L ,该反应转移电子数为 ,该反应转移电子数为 |
您最近一年使用:0次



