1 . 已知:Mg(OH)2(s) Mg2+(aq)+2OH-(aq) ∆H>0;Fe(OH)3的溶解度小于Mg(OH)2。改变含大量Mg(OH)2固体的浊液一个条件,下列判断错误的是
Mg2+(aq)+2OH-(aq) ∆H>0;Fe(OH)3的溶解度小于Mg(OH)2。改变含大量Mg(OH)2固体的浊液一个条件,下列判断错误的是
 Mg2+(aq)+2OH-(aq) ∆H>0;Fe(OH)3的溶解度小于Mg(OH)2。改变含大量Mg(OH)2固体的浊液一个条件,下列判断错误的是
Mg2+(aq)+2OH-(aq) ∆H>0;Fe(OH)3的溶解度小于Mg(OH)2。改变含大量Mg(OH)2固体的浊液一个条件,下列判断错误的是| A.加热,Ksp增大 | B.加少量水,c(Mg2+)减小 |
| C.加少量FeCl3,pH降低 | D.加少量NaOH,c(OH-)增大 |
您最近一年使用:0次
2 . 为探究Fe3+能去否除银镜反应后试管壁上银镜进行了如下实验。
(常温下溶解度:AgCl :1.9×10-4g;Ag2SO4:0.796g)
下列说法不正确的是
序号 | 操作 | 现象 |
实验① | 将2mL 2mo/L Fe(NO3)3溶液(pH=1)加入有银镜的试管中 | 银镜消失 |
实验② | 将2mL 1mol/LFe2(SO4)3溶液(pH=1)加入有银镜的试管中 | 银镜减少,未消失 |
实验③ | 将2mL 2mol/L FeCl3溶液(pH=1)加入有银镜的试管中 | 银镜消失 |
下列说法不正确的是
| A.①中可能发生反应:Fe3++Ag=Fe2++Ag+ |
| B.实验①可以证明本条件下氧化性Fe3+>Ag+ |
| C.实验②和③的试管中可能有白色沉淀生成 |
D.实验②和③现象的差异与溶液中Cl-和 有关 有关 |
您最近一年使用:0次
3 . 0.1 mol·L-1的银氨溶液中存在如下平衡:Ag(NH3) +2H2O⇌Ag++2NH3·H2O,下列说法正确的是
+2H2O⇌Ag++2NH3·H2O,下列说法正确的是
 +2H2O⇌Ag++2NH3·H2O,下列说法正确的是
+2H2O⇌Ag++2NH3·H2O,下列说法正确的是| A.向溶液中加一定浓度的氨水,该平衡可能正向移动 |
| B.该反应是一个水解反应 |
| C.向溶液中逐滴加入稀盐酸至过量,产生白色沉淀,再加入氢氧化钠沉淀至过量沉淀减少 |
| D.温度升高有利于该反应平衡正向移动,是由于促进了NH3·H2O电离降低了溶液中NH3·H2O浓度 |
您最近一年使用:0次
名校
解题方法
4 . MSO4和MCO3是两种难溶性盐。常温时两种物质的溶解度曲线如图所示,下列叙述错误的是
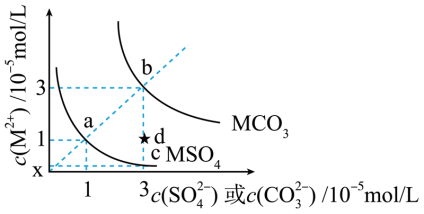
| A.Ksp(MCO3)=9.0×10−10 |
| B.c点的纵坐标0.33 |
| C.在饱和的MCO3澄清溶液里加入适量的Na2SO4固体,可使b点变为d点 |
| D.使1L含1molMSO4的悬浊液中的分散质完全转化为MCO3,需要加1molNa2CO3固体 |
您最近一年使用:0次
2021-03-03更新
|
904次组卷
|
7卷引用:新疆维吾尔自治区2021届高三第二次联考理科综合能力测试化学试卷
新疆维吾尔自治区2021届高三第二次联考理科综合能力测试化学试卷(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)小题22 难溶电解质的溶解平衡——备战2021年高考化学经典小题考前必刷(全国通用)江西省吉安市第一中学2021-2022学年高二上学期期中考试(理科)化学试题(已下线)题型27 沉淀溶解平衡常数及其应用图象(已下线)T13-溶液中的离子平衡(已下线)云南省昆明市官渡区第二中学2023-2024学年高三上学期开学化学试题
名校
5 . 下列叙述中,不正确的是
| A.AgCl在水溶液中的沉淀溶解平衡方程式是AgCl(s)⇌Ag+(aq)+Cl-(aq) |
| B.HCl在水溶液中的电离方程式是HCl=H++Cl- |
| C.反应aA(g)⇌bB(g)+cC(g)达到平衡以后,增大A的物质的量浓度,A的转化率一定减小 |
| D.钢铁发生电化学腐蚀时负极反应式为Fe-2e-=Fe2+ |
您最近一年使用:0次
6 . 向氯化铁溶液中加入过量氢氧化钠溶液,振荡后静置一段时间。下列关于该体系的说法中错误的是
| A.溶液中不再存在Fe3+ |
| B.生成了氢氧化铁沉淀 |
| C.体系中存在氢氧化铁的沉淀溶解平衡 |
| D.加入少量盐酸,则溶液中Fe3+浓度会上升 |
您最近一年使用:0次
2021-02-20更新
|
191次组卷
|
4卷引用:福建省漳州市2020-2021学年高二上学期期末考试化学试题
2021高三·全国·专题练习
7 . 已知:T ℃时,Ksp(PbS)=1.3×10-24,Ksp(ZnS)=1.0×10-22;当溶液中离子浓度≤10-5 mol·L-1时,表明该离子已除尽。T℃时,下列有关ZnS和PbS的说法不正确的是
| A.ZnS的饱和溶液中,c(Zn2+)=c(S2-)=1.0×10-11 mol·L-1 |
| B.欲将某工业废水中的Pb2+除去,则加入Na2S溶液后应保证溶液中c(S2-)≥1.3×10-19mol·L-1 |
| C.向同浓度的ZnCl2和PbCl2的混合溶液中滴加Na2S溶液,PbS先析出 |
| D.向PbS悬浊液中加入ZnCl2浓溶液,PbS不可能转化为ZnS |
您最近一年使用:0次
8 . 请根据所学知识回答:
(1)CH3COONa溶液中各种离子的浓度由大到小顺序为_______ 。
(2)请分析氯化铵溶液显酸性的原因_______ 。
(3)实验室中配制FeCl3溶液时常加入_______ 溶液以抑制其水解。
(4)氯化银在水中存在沉淀溶解平衡:AgCl(s) Ag++Cl‒。现将足量氯化银分别放入:①100 mL蒸馏水中;②100 mL 0.1 mol·L‒1盐酸溶液中,充分搅拌后,相同温度下银离子浓度的大小关系是
Ag++Cl‒。现将足量氯化银分别放入:①100 mL蒸馏水中;②100 mL 0.1 mol·L‒1盐酸溶液中,充分搅拌后,相同温度下银离子浓度的大小关系是_______ (填写序号)。
(1)CH3COONa溶液中各种离子的浓度由大到小顺序为
(2)请分析氯化铵溶液显酸性的原因
(3)实验室中配制FeCl3溶液时常加入
(4)氯化银在水中存在沉淀溶解平衡:AgCl(s)
 Ag++Cl‒。现将足量氯化银分别放入:①100 mL蒸馏水中;②100 mL 0.1 mol·L‒1盐酸溶液中,充分搅拌后,相同温度下银离子浓度的大小关系是
Ag++Cl‒。现将足量氯化银分别放入:①100 mL蒸馏水中;②100 mL 0.1 mol·L‒1盐酸溶液中,充分搅拌后,相同温度下银离子浓度的大小关系是
您最近一年使用:0次
名校
9 . Ⅰ、已知常温下,AgCl的Ksp=1.8×10-10,AgBr的Ksp=4.9×10-13。
(1)现向AgCl的悬浊液中:
①加入AgNO3固体,则c(Cl-)_______ (填“变大”、“变小”或“不变”,下同);
②若改加更多的AgCl固体,则c(Ag+)_______ ;
③若改加更多的KBr固体,则c(Ag+)_______ ;
(2)有关难溶盐的溶度积及溶解度有以下叙述,其中错误的是_______ ;
A.将难溶电解质放入纯水中,溶解达到平衡时,升高温度,Ksp一定增大
B.两种难溶盐电解质,其中Ksp小的溶解度也一定小
C.难溶盐电解质的Ksp与温度有关
D.向AgCl的悬浊液中加入适量的水,使AgCl再次达到溶解平衡,AgCl的Ksp不变,其溶解度也不变
Ⅱ、最近有人制造了一种燃料电池使甲烷氧化直接产生电流,其中一个电极通入空气,另一个电极通入甲烷,电池的电解质是NaOH溶液。这个电池负极的电极反应式为_______ 。
(1)现向AgCl的悬浊液中:
①加入AgNO3固体,则c(Cl-)
②若改加更多的AgCl固体,则c(Ag+)
③若改加更多的KBr固体,则c(Ag+)
(2)有关难溶盐的溶度积及溶解度有以下叙述,其中错误的是
A.将难溶电解质放入纯水中,溶解达到平衡时,升高温度,Ksp一定增大
B.两种难溶盐电解质,其中Ksp小的溶解度也一定小
C.难溶盐电解质的Ksp与温度有关
D.向AgCl的悬浊液中加入适量的水,使AgCl再次达到溶解平衡,AgCl的Ksp不变,其溶解度也不变
Ⅱ、最近有人制造了一种燃料电池使甲烷氧化直接产生电流,其中一个电极通入空气,另一个电极通入甲烷,电池的电解质是NaOH溶液。这个电池负极的电极反应式为
您最近一年使用:0次
解题方法
10 . 硫化镉(CdS)是难溶于水的黄色颜料,其溶解为吸热过程,在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
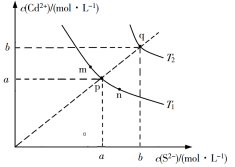
| A.在温度 T2 时,溶液中水的电离程度比 T1时大 |
| B.Ksp的关系为:Ksp(m)=Ksp(n) = Ksp(p)<Ksp(q) |
| C.温度升高时,q 点的饱和溶液的组成由 q 沿 qp 线向 p 方向移动 |
| D.向 n 点的溶液中加入少量 CdCl2固体,溶液组成由 n 沿 npm 线向 m 方向移动 |
您最近一年使用:0次
2021-01-30更新
|
140次组卷
|
2卷引用:福建省泉州市2020-2021学年高二上学期期末教学质量跟踪监测化学试题



