解题方法
1 . 弱电解质的电离平衡、盐类的水解平衡和难溶物的沉淀溶解平衡均属于化学平衡。
I.已知 在水中存在以下平衡:
在水中存在以下平衡: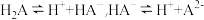 。
。
(1)常温下, 溶液的
溶液的
______ (填字母序号),原因是______ (填离子方程式)。
A.大于7 B.小于7 C.等于7 D.无法确定
(2)常温下,若向 的
的 溶液中逐滴滴加
溶液中逐滴滴加
 溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是
溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是______ (填字母序号)。
A.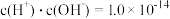 B.
B.
C.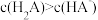 D.
D.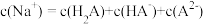
(3)常温下, 的饱和溶液中存在以下平衡:
的饱和溶液中存在以下平衡: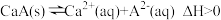 ,若要使该溶液中
,若要使该溶液中 浓度增大,可采取的措施有
浓度增大,可采取的措施有______ (填字母序号)。
A.升高温度 B.降低温度 C.加入少量蒸馏水 D.加入 固体
固体
Ⅱ.化学沉淀法是除去酸性废水中 的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液
的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液 变化的关系如图所示。向含
变化的关系如图所示。向含 的溶液中逐滴滴加
的溶液中逐滴滴加 溶液,溶液变浑浊,继续滴加
溶液,溶液变浑浊,继续滴加 溶液又变澄清。
溶液又变澄清。
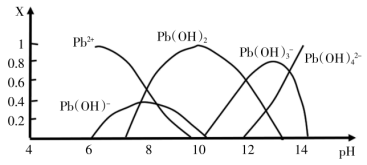
(4)若采用氢氧化物沉淀法除溶液中的 ,应将溶液的
,应将溶液的 调至约为
调至约为______ ; 时,溶液中发生的主要离子方程式为
时,溶液中发生的主要离子方程式为______ 。
(5)向酸性含铅废水中加 可将
可将 转化为
转化为 沉淀除去。若某工厂处理过的废水中
沉淀除去。若某工厂处理过的废水中 浓度为
浓度为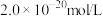 ,则
,则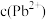 为
为______ 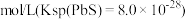 。
。
I.已知
 在水中存在以下平衡:
在水中存在以下平衡: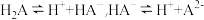 。
。(1)常温下,
 溶液的
溶液的
A.大于7 B.小于7 C.等于7 D.无法确定
(2)常温下,若向
 的
的 溶液中逐滴滴加
溶液中逐滴滴加
 溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是
溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是A.
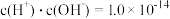 B.
B.
C.
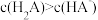 D.
D.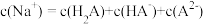
(3)常温下,
 的饱和溶液中存在以下平衡:
的饱和溶液中存在以下平衡: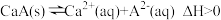 ,若要使该溶液中
,若要使该溶液中 浓度增大,可采取的措施有
浓度增大,可采取的措施有A.升高温度 B.降低温度 C.加入少量蒸馏水 D.加入
 固体
固体Ⅱ.化学沉淀法是除去酸性废水中
 的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液
的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液 变化的关系如图所示。向含
变化的关系如图所示。向含 的溶液中逐滴滴加
的溶液中逐滴滴加 溶液,溶液变浑浊,继续滴加
溶液,溶液变浑浊,继续滴加 溶液又变澄清。
溶液又变澄清。
(4)若采用氢氧化物沉淀法除溶液中的
 ,应将溶液的
,应将溶液的 调至约为
调至约为 时,溶液中发生的主要离子方程式为
时,溶液中发生的主要离子方程式为(5)向酸性含铅废水中加
 可将
可将 转化为
转化为 沉淀除去。若某工厂处理过的废水中
沉淀除去。若某工厂处理过的废水中 浓度为
浓度为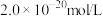 ,则
,则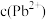 为
为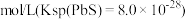 。
。
您最近一年使用:0次
2021-01-30更新
|
398次组卷
|
2卷引用:湖南省怀化市2020-2021学年高二上学期期末考试化学试题
2 . 一定温度下,某难溶电解质在水中达到沉淀溶解平衡下列说法中正确的是
| A.蒸发部分溶剂,溶质浓度增大 |
| B.沉淀的速率和溶解的速率都等于0 |
| C.再向其中加入该电解质,溶液中各种离子的浓度不变 |
| D.该难溶电解质溶解形成的阴离子的浓度等于阳离子的浓度 |
您最近一年使用:0次
3 . 25℃时,在含有大量 的饱和溶液中存在着平衡:
的饱和溶液中存在着平衡: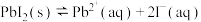 ,加入少量
,加入少量 固体,下列说法不正确的是
固体,下列说法不正确的是
 的饱和溶液中存在着平衡:
的饱和溶液中存在着平衡: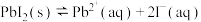 ,加入少量
,加入少量 固体,下列说法不正确的是
固体,下列说法不正确的是A.溶液中 浓度减小、 浓度减小、 浓度增大 浓度增大 | B.溶度积常数 不变 不变 |
C. 的溶解度不变 的溶解度不变 | D.沉淀溶解平衡向左移动 |
您最近一年使用:0次
2021-01-26更新
|
135次组卷
|
2卷引用:山西省怀仁市2020-2021学年高二上学期期末考试化学试题
4 . 下列方程式书写不正确的是
A. 水溶液呈碱性: 水溶液呈碱性: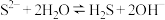 |
B. 的沉淀溶解平衡: 的沉淀溶解平衡: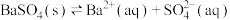 |
C.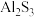 在水溶液中不存在: 在水溶液中不存在: |
D.生铁发生吸氧腐蚀和析氢腐蚀的负极反应均为: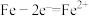 |
您最近一年使用:0次
名校
5 . 某温度下,难溶物FeR的水溶液中存在平衡FeR(s)⇌Fe2+(aq)+R2-(aq),其沉淀溶解平衡曲线如图所示。下列说法不正确的是
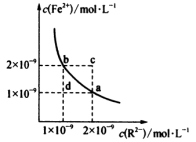

| A.该温度下,Ksp(FeR)=2×10-18 | B.c点可能有沉淀生成 |
| C.b点对应的K sp大于a点对应的K sp | D.加入FeSO4可实现由a点变到b点 |
您最近一年使用:0次
2021-01-24更新
|
501次组卷
|
5卷引用:专题11 水溶液中的离子平衡-备战2021届高考化学二轮复习题型专练
(已下线)专题11 水溶液中的离子平衡-备战2021届高考化学二轮复习题型专练山西省运城市康杰中学2021-2022学年高二上学期期中化学试题(已下线)专题27 难溶电解质的溶解平衡(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练河南省顶尖名校联盟2020-2021学年高二12月联考化学试题天津市滨海新区田家炳中学2023-2024学年高二上学期第二次月考化学试题
6 . 将CaCO3悬浊液静置后,向上层清液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是
A.c(CO ) ) | B.c(Ca2+) | C.c(H+) | D.Ksp(CaCO3) |
您最近一年使用:0次
名校
解题方法
7 . 某温度时,CaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法中,不正确 的是


A.CaSO4在水中存在沉淀溶解平衡:CaSO4 Ca2+(aq)+SO Ca2+(aq)+SO (aq) (aq) |
| B.a点表示CaSO4在水中达到沉淀溶解平衡 |
| C.b点有CaSO4沉淀生成 |
D.由图可知,含大量SO 的溶液中不存在Ca2+ 的溶液中不存在Ca2+ |
您最近一年使用:0次
2021-01-22更新
|
276次组卷
|
4卷引用:北京市大兴区2020-2021学年高二上学期期末考试化学试题
解题方法
8 . 已知:pCu=-lgc(Cu+),pX=-1gc(X-)(其中X代表Cl、Br、I)。298K时,Ksp(CuCl)=10-6,Ksp(CuBr)=10-9,Ksp(CuI)=10-12。在CuCl、CuBr、CuI的饱和溶液中阳离子和阴离子浓度关系如图所示。下列说法正确的是


| A.298K时,在CuCl的饱和溶液中加入少量NaCl固体,c(Cu+)和c(Cl-)都减小 |
| B.图中x代表CuI曲线,且P点c(Cu+)=c(I-) |
| C.升高溶液温度,M点可能移动到N点 |
D.298K时,CuBr(s)+I-(aq) CuI(s)+Br-(aq)的平衡常数K=103 CuI(s)+Br-(aq)的平衡常数K=103 |
您最近一年使用:0次
2021-01-20更新
|
185次组卷
|
2卷引用:辽宁省锦州市2020-2021学年高二上学期期末考试化学试题
9 . 下列说法正确的是
| A.升高温度,沉淀溶解平衡一定向沉淀溶解的方向移动 |
B.用 作沉淀剂,可除去废水中的 作沉淀剂,可除去废水中的 和 和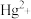 |
| C.溶解度小的沉淀不能转化为溶解度大的沉淀 |
D.向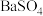 饱和溶液中加入 饱和溶液中加入 固体, 固体, 增大 增大 |
您最近一年使用:0次
10 . 下列说法不正确的是
| A.反应MgO(s)+C(s)=Mg(s)+CO(g)在室温下不能自发进行,则该反应的∆H>0 |
| B.向有AgCl固体的饱和溶液中加少许水,c(Ag+)和Ksp(AgCl)都不变 |
C.0.1 mol·L-1CH3COOH溶液加水稀释后,溶液中 的值减小 的值减小 |
| D.锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除去 |
您最近一年使用:0次



