1 . 下表是3种物质的溶解度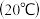 ,下列说法中正确的是
,下列说法中正确的是
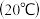 ,下列说法中正确的是
,下列说法中正确的是
| 物质 |  |  | 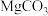 |
溶解度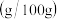 | 74 |  84 84 |  |
A.已知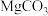 的 的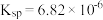 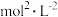 ,则所有含有固体 ,则所有含有固体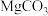 的溶液中,都有 的溶液中,都有 ,且 ,且 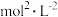 |
B.除去粗盐中含有的 杂质,最佳除杂试剂为 杂质,最佳除杂试剂为 溶液 溶液 |
| C.将表中三种物质与水混合,加热、灼烧,最终的固体产物相同 |
D.用石灰水处理含有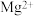 和 和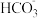 的硬水,发生的离子反应方程式为 的硬水,发生的离子反应方程式为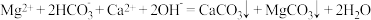 |
您最近一年使用:0次
2019-12-31更新
|
235次组卷
|
12卷引用:江西省南昌市八一中学、洪都中学等六校2019-2020学年高二上学期期末联考化学试题
江西省南昌市八一中学、洪都中学等六校2019-2020学年高二上学期期末联考化学试题2015届江西省南昌三中高三上学期第六次考试理综化学试卷(已下线)2014高考化学名师选择题专练 电解质溶液练习卷2015年湖北省荆门市高三元月调考理综化学试卷2016-2017学年湖南省娄底市双峰一中等五校高二上期中化学卷河南省洛阳市2018届高三上学期尖子生第一次联考化学试题河南省汝州市实验中学2019届高三上学期期末模拟化学试题(已下线)专题8.4 难溶电解质的溶解平衡(练)-《2020年高考一轮复习讲练测》2020届高三化学大二轮增分强化练—— 离子方程式及其应用夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——溶度积常数及相关计算2020届高三化学化学二轮复习——常考题型:浓度积及浓度积常数【精编24题】河北省石家庄市藁城区第一中学2021-2022学年高二上学期12月月考化学试题
名校
解题方法
2 . 下列实验能达到实验目的是( )
| 序号 | 实验内容 | 实验目的 |
| A | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| B | 向FeCl3+3KSCN Fe(SCN)3+3KCl的溶液平衡体系中加入少量KCl固体 Fe(SCN)3+3KCl的溶液平衡体系中加入少量KCl固体 | 说明增加生成物浓度,平衡逆向移动 |
| C | 向盛有AgCl悬浊液的试管中滴加0.1mol·L-1NaI溶液,浊液变黄 | 证明相同温度下, KSP(AgCl)>KSP(AgI) |
| D | 酸式滴定管中硫酸液面在20.00mL,将滴定管中液体全部放出 | 量取20.00mL硫酸溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-12-29更新
|
175次组卷
|
2卷引用:江西省南昌市莲塘第一中学2019-2020学年高二上学期期末质量检测化学试题
3 . 在 时,FeS的
时,FeS的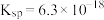 ,CuS的
,CuS的 ,ZnS的
,ZnS的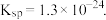 常 温时下列有关说法中正确的是
常 温时下列有关说法中正确的是
 时,FeS的
时,FeS的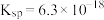 ,CuS的
,CuS的 ,ZnS的
,ZnS的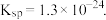 常 温时下列有关说法中正确的是
常 温时下列有关说法中正确的是| A.FeS的溶解度大于CuS的溶解度 |
B.饱和CuS溶液中 的浓度为 的浓度为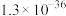  |
C.向物质的量浓度相同的 、 、 的混合液中加入少量 的混合液中加入少量 ,只有FeS沉淀生成 ,只有FeS沉淀生成 |
D.向饱和ZnS溶液中加入少量 固体,ZnS的 固体,ZnS的 变大 变大 |
您最近一年使用:0次
2019-12-26更新
|
492次组卷
|
18卷引用:江西省南昌市八一中学2022-2023学年高二上学期1月期末考试化学试题
江西省南昌市八一中学2022-2023学年高二上学期1月期末考试化学试题广东省汕头市2018-2019学年高二第二学期普通高中教学质量监测化学试题辽宁省瓦房店市高级中学2019-2020学年高二上学期期末考试化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二上学期期末考试化学试题江西省宜春市宜丰中学2023-2024学年高二上学期11月期中考试化学试题【全国百强校】四川省棠湖中学2018-2019学年高二下学期开学考试化学试题山东省淄博市实验中学2020届高三上学期第一次月考化学试题山东省胶州市胶州一中2020届高三10月月考化学试题重庆市云阳江口中学校2019-2020学年高二上学期第二次月考化学试题2019年秋高三化学复习强化练习—— 与浓度积的相关计算2019年秋高三化学复习强化练习—— 难溶电解质的沉淀溶解平衡(已下线)2020年1月5日《每日一题》人教版(选修4)—— 每周一测2020届高考二轮复习《水溶液中的离子平衡》练习题(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)天津市第二十一中学2021-2022学年高二上学期期中检测化学试题(已下线)第24讲 沉淀溶解平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第八章 水溶液中的离子反应与平衡 第52练 难溶电解质的溶解平衡(已下线)第5讲 难溶电解质的溶解平衡
2011·江苏南通·一模
名校
解题方法
4 . 以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如表。
表1.几种砷酸盐的Ksp
表2.工厂污染物排放浓度及允许排放标准
回答下列问题:
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=________ mol·L-1。
(2)写出难溶物Ca3(AsO4)2的Ksp表达式:
Ksp[Ca3(AsO4)2]=________ ,若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4 mol·L-1,c(AsO43-)最大是______ mol·L-1。
(3)工厂排放出的酸性废水中的三价砷(H3AsO3为弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4为弱酸),写出该反应的离子方程式:_______________________ 。
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为__________ ;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为_______________________ 。
表1.几种砷酸盐的Ksp
| 难溶物 | Ksp | |
| Ca3(AsO4)2 | 6.8×10-19 | |
| AlAsO4 | 1.6×10-16 | |
| FeAsO4 | 5.7×10-21 | |
表2.工厂污染物排放浓度及允许排放标准
| 污染物 | H2SO4 | As |
| 浓度 | 28.42 g·L-1 | 1.6 g·L-1 |
| 排放标准 | pH 6~9 | 0.5 mg·L-1 |
回答下列问题:
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=
(2)写出难溶物Ca3(AsO4)2的Ksp表达式:
Ksp[Ca3(AsO4)2]=
(3)工厂排放出的酸性废水中的三价砷(H3AsO3为弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4为弱酸),写出该反应的离子方程式:
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为
您最近一年使用:0次
2019-12-03更新
|
183次组卷
|
7卷引用:江西赣州市2022~2023学年高二上学期期末考试化学试题
江西赣州市2022~2023学年高二上学期期末考试化学试题河南省中原名校2021-2022学年高二上学期期末联考化学试题(已下线)2011届江苏省南通市高三第一次调研测试化学试卷(已下线)2012届江苏省阜宁、大丰、栟茶高级中学高三第二次调研联考化学试卷(已下线)2013届江苏省泗阳致远中学高三实验班第一次模拟考试化学试卷(已下线)专题8.4 难溶电解质的溶解平衡(练)-《2020年高考一轮复习讲练测》安徽省太和第一中学2020-2021学年高二上学期期中考试化学(普通班)试题
13-14高二·全国·课时练习
名校
5 . 已知25 ℃时一些难溶物质的溶度积常数如下,根据表中数据,判断下列化学方程式不正确的是( )
化学式 | Zn(OH)2 | ZnS | AgCl | Ag2S | MgCO3 | Mg(OH)2 |
溶度积 | 5×10-17 | 2.5×10-22 | 1.8×10-10 | 6.3×10-50 | 6.8×10-6 | 1.8×10-11 |
| A.2AgCl+Na2S===2NaCl+Ag2S |
B.MgCO3+H2O Mg(OH)2+CO2↑ Mg(OH)2+CO2↑ |
| C.ZnS+2H2O===Zn(OH)2↓+H2S↑ |
| D.Mg(HCO3)2+2Ca(OH)2===Mg(OH)2↓+2CaCO3↓+2H2O |
您最近一年使用:0次
2019-12-03更新
|
211次组卷
|
6卷引用:2014-2015江西省德镇市高二上学期期末化学试卷
2014-2015江西省德镇市高二上学期期末化学试卷【全国百强校】吉林省实验中学2018-2019学年高二上学期期末考试化学试题(已下线)【南昌新东方】江西省九江一中2014-2015学年高二上学期期中化学试卷(已下线)2014年高中化学人教版选修四第三章 水溶液中的离子平衡练习卷2016-2017学年山西省大同一中高二12月月考化学试卷(已下线)专题8.4 难溶电解质的溶解平衡(练)-《2020年高考一轮复习讲练测》
名校
6 . 下列解释工业生产或应用的化学用语中,不正确的是( )
| A.FeCl3溶液刻蚀铜电路板:2Fe3+ + Cu==2Fe2++ Cu2+ |
| B.向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O== Al(OH)3↓ + 3NH4 + |
| C.将少量二氧化碳通入次氯酸钠溶液中:CO2+H2O+2ClO-== CO32-+2HClO |
D.Na2CO3溶液处理水垢:CaSO4(s)+CO32−(aq) CaCO3(s)+SO42−(aq) CaCO3(s)+SO42−(aq) |
您最近一年使用:0次
2019-06-12更新
|
415次组卷
|
3卷引用:江西省九江市第一中学2019-2020学年高二下学期期末考试化学试题
7 . 绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
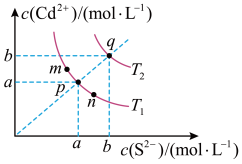

| A.图中a和b分别为T1、T2温度下CdS在水中的溶解度 |
| B.图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q) |
| C.向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动 |
| D.温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动 |
您最近一年使用:0次
2019-06-09更新
|
18592次组卷
|
83卷引用:江西省九江市第一中学2019-2020学年高二下学期期末考试化学试题
江西省九江市第一中学2019-2020学年高二下学期期末考试化学试题江西省新余市2022-2023学年高二上学期期末质量检测化学试题宁夏银川一中2019-2020学年高二上学期期末考试化学试题江西省南昌市新建一中2021届高三上学期第一次月考化学试题黑龙江省哈尔滨市师大附中2020-2021学年高二上学期期末考试化学试题福建省福州第一中学2021-2022学年高二上学期期末考试化学试题新疆喀什市普通高中2021-2022学年高三上学期期末考试化学试题湖北省武汉市青山区2021-2022学年高二上学期期末考试化学试题广东省茂名市电白区2022-2023学年高二上学期期末考试化学(选择性考试)试题宁夏回族自治区银川一中2022-2023学年高二上学期期末考试化学试题福建省福州格致中学2022-2023学年高二上学期期末考试化学试题福建省福清市虞阳中学2022-2023学年高二上学期期末考试化学试题甘肃省兰州第一中学2023-2024学年高二上学期1月期末化学试题陕西省宝鸡市渭滨区2023-2024学年高二上学期期末考试化学试题甘肃省平凉市第二中学2022-2023学年高二上学期期末考试(延考)化学试题2019年全国统一考试化学试题(新课标Ⅱ)(已下线)专题10 水溶液中的离子平衡——2019年高考真题和模拟题化学分项汇编安徽省阜阳市颍上二中等三校2020届高三上学期入学考试化学试题(已下线)专题8.4 难溶电解质的溶解平衡(讲)-《2020年高考一轮复习讲练测》(已下线)专题8.4 难溶电解质的溶解平衡(练)-《2020年高考一轮复习讲练测》贵州省遵义市南白中学2019-2020学年高二上学期第三次月考化学试题(已下线)2019年12月31日《每日一题》 人教版(选修4)——沉淀的生成与溶解(已下线)专题十二 水溶液中的离子平衡(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训西藏自治区林芝市第二高级中学2020届高三上学期第一次月考理科综合化学试题江苏省扬州中学2019-2020学年高二下学期4月月考化学试题四川省南充市白塔中学2019-2020学年高二下学期第二次月考化学试题四川省雅安中学2019-2020学年高二6月月考(期中)理综化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3章 综合检测鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第三章素养检测宁夏石嘴山市第三中学2021届高三上学期第一次月考化学试题人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡(已下线)3.4+难溶电解质的溶解平衡-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)(已下线)第03章 水溶液中的离子反应与平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)(已下线)易错17 难溶电解质的溶解平衡及应用-备战2021年高考化学一轮复习易错题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 过高考 3年真题强化闯关(已下线)第28讲 难溶电解质的溶解平衡 (精讲)——2021年高考化学一轮复习讲练测(已下线)3.4 难溶电解质的溶解平衡(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)江苏省苏州市新草桥中学2019-2020学年高二下学期6月月考化学试题(已下线)小题必刷34 沉淀溶解平衡、溶度积常数及其应用——2021年高考化学一轮复习小题必刷(通用版本)陕西省咸阳市实验中学2020-2021学年高二上学期第四次月考化学试题四川省邻水实验学校2020-2021学年高二上学期第三阶段考试化学试题安徽省池州市第一中学2020-2021学年高二12月月考化学试题湖北省石首一中2020-2021学年高三上学期11月月考化学试题(已下线)专题12 水溶液中离子平衡(攻克各种图像问题)-2021年高考化学必做热点专题(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)专题07 电解质溶液——备战2021年高考化学纠错笔记(已下线)解密10 水溶液中离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)选择性必修1(SJ)专题3专题培优专练广东省惠州市惠城区2021--2022学年高三上学期8月开学摸底化学试题(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)广东省珠海市第二中学2020-2021学年高二上学期10月月考化学试题(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向27 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点微专题湖北省武汉市蔡甸区实验高级中学2020-2021学年高二上学期10月联合考试化学试题(已下线)第5讲 沉淀溶解平衡-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)重庆育才中学2021-2022学年高二上学期第四次定时练习化学试题(已下线)专题27 难溶电解质的溶解平衡(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练(已下线)3.4.2 沉淀溶解平衡的应用(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)四川省泸州市泸县第五中学2021-2022学年高二下学期开学考试化学试题(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题6 Ksp专练(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)第三章 综合拔高练(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题06 水溶液中的离子平衡(练)-2023年高考化学二轮复习讲练测(新高考专用)河南省漯河市高级中学2022-2023学年高二上学期第二次月考化学试题(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第八章 水溶液中的离子反应与平衡 第53讲 沉淀溶解平衡图像的分析(已下线)题型142 有关沉淀溶解平衡图像(已下线)专题16 水溶液中的离子平衡云南省宣威市第三中学2022-2023学年高二下学期第三次月考化学试题(已下线)T12-难溶电解质的沉淀溶解平衡微专题(九)——沉淀溶解平衡曲线(已下线)第32讲难溶电解质的溶解平衡四川省南充市嘉陵第一中学2022-2023学年高二下学期5月期中考试化学试题
名校
8 . 某温度时,CuS、MnS在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是
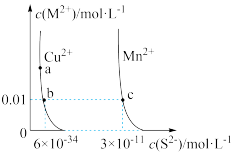
| A.在含有CuS和MnS固体的溶液中c(Cu2+)∶c(Mn2+)=1∶2×10-23 |
| B.向CuSO4溶液中加入MnS发生反应: Cu2+(aq)+MnS(s) |
| C.a点对应的Ksp等于b点对应的Ksp |
| D.该温度下,Ksp(CuS)小于Ksp(MnS) |
您最近一年使用:0次
2019-02-26更新
|
658次组卷
|
3卷引用:【市级联考】江西省鹰潭市2018-2019学年高二上学期期末质量检测化学试题
真题
名校
9 . 往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如右图所示。则原溶液中c(I-)/c(Cl-)的比值为
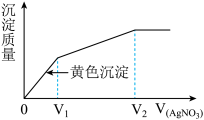

| A.(V2-V1)/V1 | B.V1/V2 |
| C.V1/(V2-V1) | D.V2/V1 |
您最近一年使用:0次
2019-01-30更新
|
1350次组卷
|
24卷引用:2015-2016学年江西省九江一中高一上期末考试化学试卷
2015-2016学年江西省九江一中高一上期末考试化学试卷(已下线)【南昌新东方】江西省九江一中2015-2016学年高一上学期期末化学试题(已下线)2012-2013学年山东省聊城市某重点中学高二第四次模块检测化学试卷(已下线)2012-2013学年山东省聊城市四县六校高二下学期期末联考化学试卷(已下线)2013-2014广东汕头市金山中学第一学期期末高二化学试卷云南省鹤庆三中2018-2019学年高二下学期期末考试化学试题云南省武定民族中学2019-2020学年高二上学期期末考试化学试题2007年普通高等学校招生全国统一考试(上海卷)化学试题(已下线)2012年人教版高中化学选修4 3.4难溶电解质的溶解平衡练习卷(已下线)2014年高考化学鲁科版3.4海水中的元素练习卷(已下线)2013-2014天津市南开中学高三上学期第一次月考化学试卷(已下线)2015届内蒙古北方重工业集团第三中学高三10月考化学试卷(已下线)2015届内蒙古北方重工业三中高三10月月考化学试卷2013—2014福建省闽侯一中高三上学期10月月考化学试卷2016届湖南省衡阳市第八中学高三上学期第二次月考化学试卷2015-2016学年山东省枣庄三中高二上学情调查化学试卷2016届重庆市巴蜀中学高三下3月月考理综化学试卷2015-2016学年湖北省枣阳市高中高二下期中化学试卷2016-2017学年河北省沧州一中高二上开学测化学试卷宁夏石嘴山市第三中学2016-2017学年高二下学期第二次(5月)月考化学试题人教版2017-2018学年高一化学必修1:4.2 富集在海水中的元素-氯 同步测试2【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高二下学期第一次月考(开学)化学试题山东省枣庄市滕州市第一中学2019-2020学年高二下学期学习竞赛化学试题(已下线)练习12 难溶电解质的溶解平衡-2020-2021学年【补习教材·寒假作业】高二化学(人教版)
10 . 已知CuS、PbS、HgS的溶度积分别为l.3xl0﹣36、9.0x10﹣29、6.4x10﹣23.下列推断不正确的是
| A.向含Pb2+、Cu2+、Hg2+的浓度均为0.010 mol•L﹣1的溶液中通入硫化氢气体,产生沉淀的顺序依次为PbS、CuS、HgS |
| B.在硫化铅悬浊液中滴几滴硝酸铜溶液,会生成硫化铜 |
| C.在含Hg2+、Cu2+、Pb2+的溶液中滴加硫化钠溶液,当c(S2﹣)=0.001 mol•L﹣1时三种金属离子都完全沉淀 |
| D.硫化钠是处理废水中含上述金属离子的沉淀剂 |
您最近一年使用:0次
2019-01-19更新
|
112次组卷
|
3卷引用:江西省宜春市丰城中学2023-2024学年高二上学期1月期末考试化学试题

 CuS(s)+Mn2+(aq)
CuS(s)+Mn2+(aq)

