1 . 已知: ,
, 均难溶于水,
均难溶于水, ,离子浓度
,离子浓度 时认为其沉淀完全。
时认为其沉淀完全。 时,
时, ,
, 的沉淀溶解平衡曲线如图所示,其中
的沉淀溶解平衡曲线如图所示,其中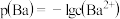 ,
,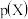
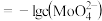 或
或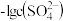 。下列叙述正确的是
。下列叙述正确的是

 ,
, 均难溶于水,
均难溶于水, ,离子浓度
,离子浓度 时认为其沉淀完全。
时认为其沉淀完全。 时,
时, ,
, 的沉淀溶解平衡曲线如图所示,其中
的沉淀溶解平衡曲线如图所示,其中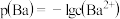 ,
,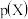
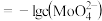 或
或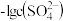 。下列叙述正确的是
。下列叙述正确的是
A. 时, 时,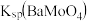 的数量级为 的数量级为 |
B. 时, 时, 点对应为 点对应为 的饱和溶液 的饱和溶液 |
C. 时, 时,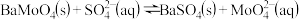 的平衡常数 的平衡常数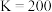 |
D. 时,向浓度均为 时,向浓度均为 的 的 和 和 的混合溶液中加入 的混合溶液中加入 溶液,当 溶液,当 恰好完全沉淀时,溶液中 恰好完全沉淀时,溶液中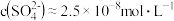 |
您最近一年使用:0次
2021-09-10更新
|
2129次组卷
|
10卷引用:江西省南昌大学附属中学2021-2022学年高二上学期期末考试化学试题
江西省南昌大学附属中学2021-2022学年高二上学期期末考试化学试题山西省运城市2022届高三上学期入学摸底测试化学试题辽宁省沈阳市第二十中学2021-2022学年高二上学期期初考试化学试题(已下线)2021年高考全国甲卷化学试题变式题2022届重庆市缙云教育联盟高三第〇次诊断性检测化学试题(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押江苏卷第13题 水溶液中的离子平衡 -备战2022年高考化学临考题号押题(江苏卷)(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)巩固训练5(已下线)易错点10对沉淀溶解平衡的原理或应用理解不清而出错
名校
2 . 通过表中的相关数据,计算、分析、判断给出结论,题目所给数据和条件均为常温下:
(1)NH4F溶液显_______ 性。
(2)NH4HCO3 溶液与少量NaOH溶液反应时,_______ (填离子符号)先与 NaOH溶液中的OH-反应。
(3)①反应 CuS(s) + H2SO4(aq)⇌H2S(aq) + CuSO4(aq)的 K=_______ ;反应 FeS(s) + H2SO4(aq)⇌H2S(aq)+FeSO4 (aq)的 K= 3.9×103;
②反应 CuS(s)+Fe2+(aq)⇌FeS(s)+Cu2+(aq)的 K=_______ (以上计算结果均保留两位有效数字)。
③由计算结果可以知道实验室制备H2S气体应选用_______ ,检验H2S气体应选用_______ (均用上述反应中的盐类物质作答)
(4)除去废水中的Cu2+使用过量的FeS固体的优点有:
①可以除去废水中的Cu2+,过量的FeS和生成的CuS可以通过过滤一并除去;
②_______ 。
| NH3•H2O | Kb=1.8×10-5 |
| H2CO3 | Ka1=4.4×10-7 Ka2=4.7×10-11 |
| HF | Ka=6.8×10-4 |
| H2S | Ka1=1.3×10-7 Ka2=7.1×10-15 |
| H2O | Kw=10-14 |
| Cu(OH)2 | Ksp=2.2×10-20 |
| Fe(OH)3 | Ksp=4.0×10-38 |
| CuS | Ksp=6.3×10-36 |
| FeS | Ksp=3.6×10-18 |
| 常用对数 | lg2=0.3 lg2.2=0.34 lg3=0.48 |
(1)NH4F溶液显
(2)NH4HCO3 溶液与少量NaOH溶液反应时,
(3)①反应 CuS(s) + H2SO4(aq)⇌H2S(aq) + CuSO4(aq)的 K=
②反应 CuS(s)+Fe2+(aq)⇌FeS(s)+Cu2+(aq)的 K=
③由计算结果可以知道实验室制备H2S气体应选用
(4)除去废水中的Cu2+使用过量的FeS固体的优点有:
①可以除去废水中的Cu2+,过量的FeS和生成的CuS可以通过过滤一并除去;
②
您最近一年使用:0次
名校
3 . 按要求填空。
(1)工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
为除去溶液中的Fe2+,可先加入_______ ,(从下面四个选项选择)将Fe2+氧化为Fe3+,反应的离子方程式为_______ ,然后加入适量的_______ (写化学式)调整溶液的pH使Fe3+转化为Fe(OH)3沉淀。
A.KMnO4 B.Cl2 C.浓硫酸 D.H2O2
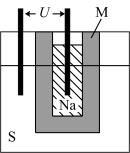
(2)如图为钠硫高能电池的结构示意图,该电池的工作温度为320 ℃左右,电池反应为2Na+xS=Na2Sx,正极的电极反应式为_______ 。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的_______ 倍。
(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,当溶液pH=7时,溶液中各离子浓度由大到小的排列顺序是_______ 。
(1)工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
为除去溶液中的Fe2+,可先加入
A.KMnO4 B.Cl2 C.浓硫酸 D.H2O2
(2)如图为钠硫高能电池的结构示意图,该电池的工作温度为320 ℃左右,电池反应为2Na+xS=Na2Sx,正极的电极反应式为

(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,当溶液pH=7时,溶液中各离子浓度由大到小的排列顺序是
您最近一年使用:0次
名校
解题方法
4 . 已知常温下两种难溶硫化物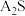 、BS在水中的沉淀溶解平衡曲线如图所示。已知阴、阳离子浓度的单位为
、BS在水中的沉淀溶解平衡曲线如图所示。已知阴、阳离子浓度的单位为 ,下列说法不正确的是
,下列说法不正确的是
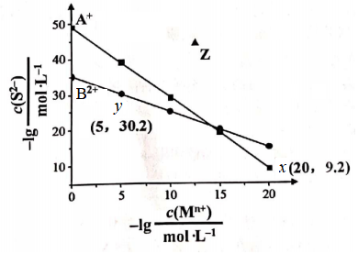
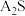 、BS在水中的沉淀溶解平衡曲线如图所示。已知阴、阳离子浓度的单位为
、BS在水中的沉淀溶解平衡曲线如图所示。已知阴、阳离子浓度的单位为 ,下列说法不正确的是
,下列说法不正确的是
A.Z点为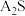 的分散系:v(沉淀)<v(溶解) 的分散系:v(沉淀)<v(溶解) |
B.向含BS沉淀的过饱和溶液中加入一定量的 固体,Ksp(BS)不变 固体,Ksp(BS)不变 |
C.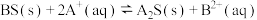 反应趋于完全 反应趋于完全 |
D. |
您最近一年使用:0次
2021-07-12更新
|
220次组卷
|
2卷引用:江西省南昌市外国语学校2021-2022学年高二上学期期末考试 化学(理科)试题
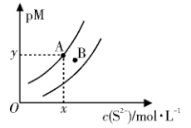
5 . 常温下, 和
和 的沉淀溶解关系如图所示,其中
的沉淀溶解关系如图所示,其中 、
、 ,M为
,M为 或
或 ,
, 表示
表示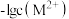 。下列说法正确的是
。下列说法正确的是
 和
和 的沉淀溶解关系如图所示,其中
的沉淀溶解关系如图所示,其中 、
、 ,M为
,M为 或
或 ,
, 表示
表示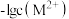 。下列说法正确的是
。下列说法正确的是
A.常温下,B点为 的不饱和溶液 的不饱和溶液 |
B.若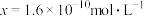 ,则 ,则 |
| C.若对A点浊液加热,A点沿曲线向上移动 |
D.在 和 和 同时沉淀的浊液中, 同时沉淀的浊液中, |
您最近一年使用:0次
2021-07-06更新
|
762次组卷
|
10卷引用:江西省抚州市2021-2022学年高二上学期期末学生学业质量监测化学试题
江西省抚州市2021-2022学年高二上学期期末学生学业质量监测化学试题四川省乐山市2020-2021学年高二下学期期末考试化学试题 江西省南昌市第十中学2023-2024学年高二上学期第二次月考化学试题(已下线)必考点08 沉淀溶解平衡-【对点变式题】2021-2022学年高二化学上学期期中期末必考题精准练(人教版选择性必修1)四川省成都外国语学校2021-2022学年高二下学期入学考试化学试题四川省遂宁中学校2021-2022学年高二下学期期中考试化学试题四川省南充市南部县第二中学2021-2022学年高二下学期5月月考化学试题山东师范大学附属中学2022-2023学年高二上学期期中水平测试化学试题广东省广州市华南师范大学附属中学2022-2023学年高二上学期12月月考化学试题广东省东莞市东莞中学松山湖学校2023-2024学年高二上学期期中考试化学试题
6 . 下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙: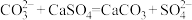 |
B.过量铁粉加入稀硝酸中: |
C.硫酸铝溶液中滴加少量氢氧化钾溶液: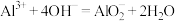 |
D.氯化铜溶液中通入硫化氢: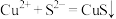 |
您最近一年使用:0次
2021-06-09更新
|
27372次组卷
|
66卷引用:江西省景德镇市乐平中学2021-2022学年高二下学期期末质量检测化学试题
江西省景德镇市乐平中学2021-2022学年高二下学期期末质量检测化学试题河北省石家庄一中2020-2021学年高二下学期期末考试化学试题江西省赣州市第十四中学2022届高三上学期第二次月考化学试题江西省宜春市第九中学2021-2022学年高三上学期10月月考化学试题陕西省咸阳市武功县普集高级中学2021-2022学年高三上学期期末考试化学试题黑龙江省哈尔滨市第一二二中学2021-2022学年高三假期检验性考试化学试题湖南省邵东市第三中学2023-2024学年高二上学期1月期末考试化学试卷 2021年高考全国乙卷化学真题河南省三门峡市实验高中2020-2021学年高二下学期6月月考化学试题(已下线)课时05 电解质与离子方程式-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点04 离子反应-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第4讲 离子反应 (讲)— 2022年高考化学一轮复习讲练测(新教材新高考)宁夏中卫市中宁县第一中学2021-2022学年高三上学期第一次月考化学试题重庆市开州中学高 2021-2022学年高三上学期10月月考化学试题陕西省西安中学2022届高三上学期第一次月考化学试题福建省福清西山学校2021-2022学年高三上学期10月月考化学试题(已下线)考点03 离子反应-备战2022年高考化学学霸纠错(全国通用)(已下线)2021年高考全国乙卷化学试题变式题广东省河源正德中学2021-2022学年高二上学期第一次段考化学试题(已下线)解密04 离子反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题04 离子反应-2022年高考化学二轮复习重点专题常考点突破练(已下线)解密04 离子反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)专题08 化学方程式正误判断—2022年高考化学二轮复习讲练测(全国版)-讲义新疆石河子第一中学2021-2022学年高三上学期8月月考(A卷)化学试题云南省峨山彝族自治县第一中学2021-2022学年高二上学期12月月考化学试题(已下线)卷11 溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)卷03 离子方程式正误判断-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)秘籍03 化学用语-备战2022年高考化学抢分秘籍(全国通用)(已下线)查补易混易错点04 离子反应-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题03离子反应-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题03离子反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)第03练 用分类思想突破离子反应-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)考点04 离子反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第02讲 离子反应(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题06 “四型和四法”破解与量有关离子方程式书写-备战2023年高考化学一轮复习考点微专题(已下线)微专题05 破解“六大陷阱”突破离子方程式书写正误判断-备战2023年高考化学一轮复习考点微专题(已下线)第02练 离子反应-2023年高考化学一轮复习小题多维练(全国通用)陕西省咸阳市武功县普集高级中学2022-2023学年高三上学期第一次月考化学试题 安徽省亳州市第五完全中学2021-2022学年高三上学期期中考试化学试题山东省临沂市兰陵县第四中学2021-2022学年高三12月月考化学试题内蒙古巴彦淖尔市临河区第三中学2021-2022学年高三上学期第二次阶段性测试理综化学试题天津市实验中学滨海学校黄南民族班2021-2022学年高三上学期期中质量监测化学试题(已下线)专题03 离子反应方程式和离子共存 (练)-2023年高考化学二轮复习讲练测(新高考专用)安徽省六安市裕安区新安中学2022-2023学年高三上学期第三次月考化学试题(已下线)专题04 突破离子共存、离子推断、离子方程式正误判断(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)第一部分 二轮专题突破 专题3 离子方程式的书写及正误判断(已下线)第一章 化学物质及其变化 第2练 离子反应 离子方程式(已下线)题型10 离子方程式正误的判断(已下线)专题卷05 离子方程式正误判断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)第2讲 离子反应 离子方程式(已下线)专题04 离子反应(已下线)专题04 离子反应(已下线)微专题 与量有关的离子方程式的书写(已下线)第04练 离子共存 离子方程式的正误判断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点04 离子反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)黑龙江省哈尔滨市第三十二中学校2023-2024学年高三上学期9月月考化学试题四川省江油中学2023-2024学年高三上学期9月月考理科综合化学试题四川省攀枝花市第十五中学校2023-2024学年高三上学期8月考试化学试题安徽省安庆市第一中学龙山校区2021-2022学年高一下学期3月阶段性考试化学试题北京工业大学附属中学2022-2023学年高三上学期开学测试化学试题山东省聊城颐中外国语学校2023-2024学年高三上学期期中考试化学试题甘肃省平凉市泾川县第三中学2023-2024学年高三上学期第3次月考化学试题新疆喀什市第五中学2023-2024学年高三上学期12月大联考化学预测卷(已下线)第02讲 离子反应、离子方程式(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
7 . 向NaHCO3溶液中加入镁条(已去除表面氧化膜)产生大量气泡。为探究其反应原因,设计实验如图:
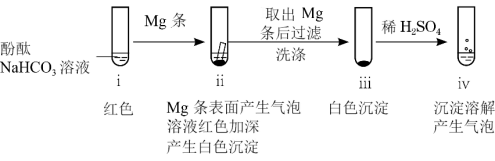
已知:溶度积常数(25℃):MgCO3 Ksp =6.82×10-6 Mg(OH)2 Ksp=5.61×10-12
下列说法不正确的是

已知:溶度积常数(25℃):MgCO3 Ksp =6.82×10-6 Mg(OH)2 Ksp=5.61×10-12
下列说法不正确的是
A.试管i中,HCO 的水解程度大于电离程度 的水解程度大于电离程度 |
| B.试管ii大量气泡中一定含有H2 |
| C.试管iii中白色沉淀一定不含Mg(OH)2 |
| D.Mg与 NaHCO3溶液的反应可表示为:2Mg+2NaHCO3+2H2O=Mg(OH)2 +MgCO3+Na2CO3+2H2↑ |
您最近一年使用:0次
2021-05-10更新
|
400次组卷
|
3卷引用:江西省南昌大学附属中学2021-2022学年高二上学期期末考试化学试题
名校
解题方法
8 . 下列实验方案能实现相应实验目的或得出相应结论的是
| 选项 | 实验方案 | 实验目的或结论 |
| A | 向20%蔗糖溶液中加入少量稀H2SO4,加热;再加入银氨溶液,未出现银镜 | 蔗糖未水解 |
| B | 将NaOH的乙醇溶液加入溴乙烷中加热,将产生的气体直接通入溴水中,褪色 | 证明溴乙烷的消去反应有乙烯生成 |
| C | 用两支试管各取5mL0.1mol·L-1的KMnO4溶液,分别加入2mL0.1mol·L-1和0.2mol·L-1的草酸溶液,记录溶液褪色所需的时间 | 探究浓度对化学反应速率的影响 |
| D | 在相同温度下,向1mL0.2mol·L-1NaOH溶液中滴入2滴0.1mol·L-1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol·L-1FeCl3溶液,又生成红褐色沉淀 | 溶解度:Mg(OH)2>Fe(OH)3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-04-08更新
|
321次组卷
|
2卷引用:江西省宜春市第一中学2022-2023学年高二下学期期末考试化学试题
名校
解题方法
9 . 下列说法正确的是
A.常温下,将 的酸 的酸 溶液与 溶液与 的 的 溶液等体积混合,则混合溶液的 溶液等体积混合,则混合溶液的 一定等于7 一定等于7 |
B.在 的 的 溶液中存在: 溶液中存在: |
C.向 粉末中滴加硼酸溶液,有 粉末中滴加硼酸溶液,有 产生 产生 |
D.当 溶液遇到闪锌矿 溶液遇到闪锌矿 和方铅矿(PbS)时,可转变为铜蓝 和方铅矿(PbS)时,可转变为铜蓝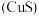 ,说明 ,说明 的溶度积小于 的溶度积小于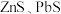 |
您最近一年使用:0次
2021-04-05更新
|
287次组卷
|
4卷引用:江西省南昌市外国语学校2021-2022学年高二上学期期末考试 化学(理科)试题
江西省南昌市外国语学校2021-2022学年高二上学期期末考试 化学(理科)试题陕西省咸阳市2021届高三上学期高考模拟检测(一)化学试题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)(已下线)小题20 弱电解质的电离,水的电离,溶液pH——备战2021年高考化学经典小题考前必刷(全国通用)
10 . 某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断正确的是
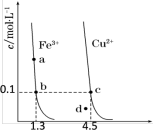

| A.升温可使溶液由a点变到b点 |
B.Ksp[Cu(OH)2]=1.0 10-20 10-20 |
| C.c点变成d点,可以往溶液中加少许Cu(OH)2固体 |
| D.FeCl3溶液中含有少量Cu2+,可以通过调节溶液pH除去 |
您最近一年使用:0次



