名校
1 . 电解质水溶液中存在电离平衡,水解平衡、沉淀溶解平衡。请回答下列问题:
(1)常温下,部分弱酸的电离平衡常数如表:
①等浓度 、
、 、
、 和
和 溶液中,碱性最强的是
溶液中,碱性最强的是___________ (写化学式)。
②等浓度的 与
与 混合溶液中离子浓度由大到小的顺序为
混合溶液中离子浓度由大到小的顺序为___________ 。
(2)室温下,用 盐酸溶液滴定
盐酸溶液滴定 氨水溶液,滴定曲线如图所示。
氨水溶液,滴定曲线如图所示。
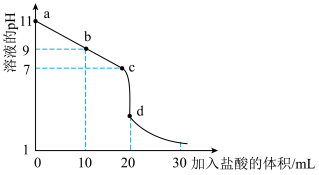
①该中和滴定选用___________ (填“甲基橙”或“酚酞”)作指示剂。
②室温下, 氨水溶液中
氨水溶液中 的电离平衡常数约为
的电离平衡常数约为___________ 
③b点所示的溶液中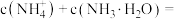
___________ (用溶液的其它离子浓度表示)。
(3)工业上向锅炉里注入所得到的 溶液浸泡,将水垢中的
溶液浸泡,将水垢中的 转化为
转化为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。当把水垢中 完全转化时,混合溶液中的
完全转化时,混合溶液中的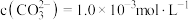 ,则
,则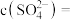
___________  (保留小数点后一位)。
(保留小数点后一位)。
已知: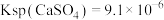 ,
,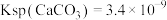
(1)常温下,部分弱酸的电离平衡常数如表:
| 弱酸 |  |  |  |
| 电离平衡常数 | 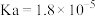 | 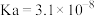 | 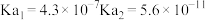 |
 、
、 、
、 和
和 溶液中,碱性最强的是
溶液中,碱性最强的是②等浓度的
 与
与 混合溶液中离子浓度由大到小的顺序为
混合溶液中离子浓度由大到小的顺序为(2)室温下,用
 盐酸溶液滴定
盐酸溶液滴定 氨水溶液,滴定曲线如图所示。
氨水溶液,滴定曲线如图所示。
①该中和滴定选用
②室温下,
 氨水溶液中
氨水溶液中 的电离平衡常数约为
的电离平衡常数约为
③b点所示的溶液中
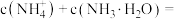
(3)工业上向锅炉里注入所得到的
 溶液浸泡,将水垢中的
溶液浸泡,将水垢中的 转化为
转化为 ,写出该反应的离子方程式:
,写出该反应的离子方程式: 完全转化时,混合溶液中的
完全转化时,混合溶液中的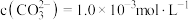 ,则
,则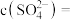
 (保留小数点后一位)。
(保留小数点后一位)。已知:
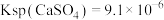 ,
,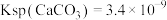
您最近一年使用:0次
名校
2 . 下列实验操作、现象及结论均正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 以 为电极,以酸化的 为电极,以酸化的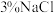 溶液作电解质溶液,连接成原电池装置,过一段时间,从 溶液作电解质溶液,连接成原电池装置,过一段时间,从 电极区域取少量溶液于试管中,再向试管中滴入2滴 电极区域取少量溶液于试管中,再向试管中滴入2滴 溶液,观察现象 溶液,观察现象 | 探究金属的电化学保护法 |
| B | 向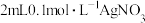 溶液中先滴加4滴 溶液中先滴加4滴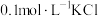 溶液,再滴加4滴 溶液,再滴加4滴 溶液。先产生白色沉淀,再产生黄色沉淀 溶液。先产生白色沉淀,再产生黄色沉淀 |  转化为 转化为 , , 溶解度小于 溶解度小于 溶解度 溶解度 |
| C | 向某溶液中滴加浓盐酸,将产生气体通入石蕊试液,溶液先变红后褪色 | 溶液中含有 或 或 |
| D | 室温下,测定浓度均为 的 的 与 与 溶液的 溶液的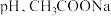 溶液的 溶液的 大 大 | 结合 的能力: 的能力: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-07更新
|
83次组卷
|
2卷引用:江西省宜春市宜丰中学2023-2024学年高二下学期开学考试化学试题(创新部)
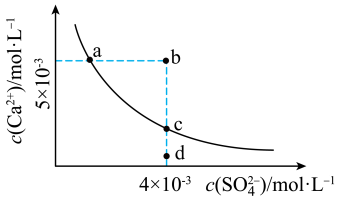
3 . 常温下, 在水中的沉淀溶解平衡曲线如图所示,已知常温下
在水中的沉淀溶解平衡曲线如图所示,已知常温下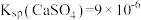 。下列说法正确的是
。下列说法正确的是
 在水中的沉淀溶解平衡曲线如图所示,已知常温下
在水中的沉淀溶解平衡曲线如图所示,已知常温下 。下列说法正确的是
。下列说法正确的是
| A.升高温度曲线会往右上方移动 |
B.d点表示 的过饱和溶液,b点表示 的过饱和溶液,b点表示 的不饱和溶液 的不饱和溶液 |
C.b点加水可以变到如图的曲线上,且此时的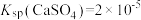 |
D.加入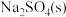 ,可以使溶液由c点变到a点 ,可以使溶液由c点变到a点 |
您最近一年使用:0次
名校
解题方法
4 . 高磷镍铁是生产钙镁磷肥的副产品。以高磷镍铁(主要含金属单质 、
、 、非金属单质P,还含有少量
、非金属单质P,还含有少量 、
、 、
、 的磷化物)为原料生产硫酸镍晶体
的磷化物)为原料生产硫酸镍晶体 的工艺流程如图。
的工艺流程如图。
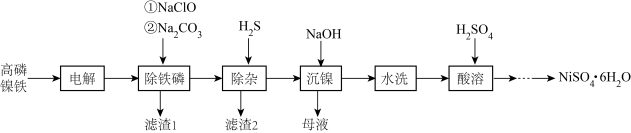
(1)“电解”时,选用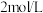 硫酸溶液为电解液。将高磷镍铁制成电极板,则该电极板作
硫酸溶液为电解液。将高磷镍铁制成电极板,则该电极板作___________ (填“阳极”或“阴极”);另一极的主要电极反应为:_____________________ 。此外,溶液中的 有部分在阴极放电。
有部分在阴极放电。
(2)“沉镍”时,离子方程式为___________________________________________ ,为确保镍沉淀完全,理论上应调节溶液
_____________ (已知:在该工业环境下, ;当溶液中离子浓度
;当溶液中离子浓度 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
(3)已知: 时,
时, 、
、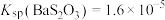 。向上述流程制得的
。向上述流程制得的 溶液中加入
溶液中加入 固体,充分反应后,过滤可得到
固体,充分反应后,过滤可得到 溶液。生成
溶液。生成 的化学方程式为
的化学方程式为________ 。
(4)从 溶液里获取
溶液里获取 的操作主要有:
的操作主要有:___________ 、__________ 、过滤、洗涤、干燥。
 、
、 、非金属单质P,还含有少量
、非金属单质P,还含有少量 、
、 、
、 的磷化物)为原料生产硫酸镍晶体
的磷化物)为原料生产硫酸镍晶体 的工艺流程如图。
的工艺流程如图。
(1)“电解”时,选用
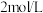 硫酸溶液为电解液。将高磷镍铁制成电极板,则该电极板作
硫酸溶液为电解液。将高磷镍铁制成电极板,则该电极板作 有部分在阴极放电。
有部分在阴极放电。(2)“沉镍”时,离子方程式为

 ;当溶液中离子浓度
;当溶液中离子浓度 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。(3)已知:
 时,
时, 、
、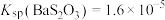 。向上述流程制得的
。向上述流程制得的 溶液中加入
溶液中加入 固体,充分反应后,过滤可得到
固体,充分反应后,过滤可得到 溶液。生成
溶液。生成 的化学方程式为
的化学方程式为(4)从
 溶液里获取
溶液里获取 的操作主要有:
的操作主要有:
您最近一年使用:0次
2024-03-01更新
|
109次组卷
|
2卷引用:江西省新余市第一中学2023-2024学年高二下学期开学考试化学试题
名校
解题方法
5 . 化学与生产、生活息息相关。下列说法正确的是
| A.明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
| B.在铁制品上镀铜时,铁制品所在电极发生氧化反应 |
C.在去除锅炉水垢中的 时,通常先用碳酸钠溶液浸泡,再用酸去除 时,通常先用碳酸钠溶液浸泡,再用酸去除 |
| D.用氯气和氢氧化钠制取消毒液,运用了盐类水解的原理 |
您最近一年使用:0次
2024-01-26更新
|
82次组卷
|
2卷引用:江西省新余市第一中学2023-2024学年高二下学期开学考试化学试题
名校
解题方法
6 . 下列实验操作和实验结论或目的均正确的是
选项 | 实验操作 | 实验结论或目的 |
A | 向含有酚酞的 | 证明 |
B | 等体积 | 证明HX酸性比HY强 |
C | 将氯水滴在湿润的pH试纸上,与标准比色卡对照 | 测定氯水的pH |
D | D.向 | 证明在相同温度下: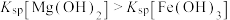 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-24更新
|
65次组卷
|
2卷引用:江西省宜春市丰城中学东校区(九中)2023-2024学年高二下学期开学考试化学试卷
名校
7 . 化学与生产、生活息息相关。下列有关说法错误的是
| A.酒曲酿酒,利用了催化剂使平衡正向移动的原理 |
| B.采用低温冷冻技术保存食物可减慢食物腐烂速率 |
| C.海港码头的钢管桩,可利用“外加电流法”防腐蚀 |
D.盐碱地(含较多 等)可通过施加适量石膏( 等)可通过施加适量石膏( ),降低土壤的碱性 ),降低土壤的碱性 |
您最近一年使用:0次
2024-01-22更新
|
71次组卷
|
3卷引用:江西省宜春市丰城中学东校区(九中)2023-2024学年高二下学期开学考试化学试卷
名校
解题方法
8 . 室温下,下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将1mL0.1mol/L 溶液滴入5mL 0.1mol/L NaOH溶液有沉淀产生,再滴加0.1mol/L 溶液滴入5mL 0.1mol/L NaOH溶液有沉淀产生,再滴加0.1mol/L 溶液 溶液 | 先有白色沉淀生成,后变为浅蓝色沉淀 | 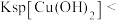 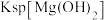 |
| B | 向浓度均为0.1mol/L的 和 和 混合溶液中滴加0.1mol/L 混合溶液中滴加0.1mol/L 溶液 溶液 | 先出现黄色沉淀 |  还原性强于 还原性强于 |
| C | 室温时,在pH试纸上滴2~3滴 溶液 溶液 | 测得, |  溶液中 溶液中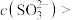  |
| D | 用pH计测量相同浓度NaClO溶液和 溶液的pH值 溶液的pH值 | NaClO溶液的pH值大于 溶液 溶液 |  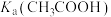 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-29更新
|
416次组卷
|
2卷引用:江西省上饶市第一中学2023-2024学年高二下学期开学考试化学试题
名校
9 . 锂离子电池的应用很广泛,某种锂电池的正极材料为钴酸锂,该材料可以由海水(含较大浓度的LiCI及少量MgCl2、CaCl2、MnCl2等)为原料制备,其工艺流程如图所示:
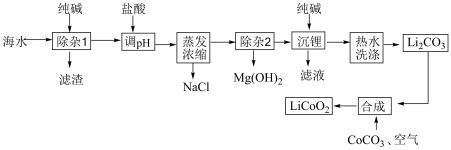
已知:①在常温下几种难溶物质的溶度积常数如表
②Li2CO3微溶于热水,可溶于冷水。回答下列问题:
(1)“除杂1”步骤中除去的杂质离子为Mg2+和_____ 。
(2)“调pH”的目的是_____ 。
(3)金属镁可以通过电解熔融MgC12得到,写出由Mg(OH)2沉淀制MgCl2固体的具体操作_____ 。
(4)20℃时碳酸锂在水中的溶解度为1.295g,饱和溶液密度为1.0148g/cm3,其中Li2CO3的物质的量浓度为_____ 。(结果保留2位有效数字)
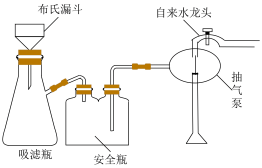
(5)“热水洗涤”的目的是_____ 。在实验室里洗涤Li2CO3时会采用如图所示装置,该装置较于普通过滤装置的优点为_____ 。
(6)“合成”工序需要高温条件,并放出能使澄清石灰水变浑浊的气体,写出该反应的化学方程式_____ 。

已知:①在常温下几种难溶物质的溶度积常数如表
| 物质 | Li2CO3 | MgCO3 | CaCO3 | MnCO3 | Mg(OH)2 |
| K | 2.5×10-2 | 6.8×10-6 | 3.4×10-9 | 2.3×10-11 | 5.6×10-12 |
(1)“除杂1”步骤中除去的杂质离子为Mg2+和
(2)“调pH”的目的是
(3)金属镁可以通过电解熔融MgC12得到,写出由Mg(OH)2沉淀制MgCl2固体的具体操作
(4)20℃时碳酸锂在水中的溶解度为1.295g,饱和溶液密度为1.0148g/cm3,其中Li2CO3的物质的量浓度为
(5)“热水洗涤”的目的是

(6)“合成”工序需要高温条件,并放出能使澄清石灰水变浑浊的气体,写出该反应的化学方程式
您最近一年使用:0次
名校
10 . SrF2是一种难溶于水、但可溶于酸的盐。在常温下,向SrF2浊液中通入氯化氢气体,得到了如下所示的图像,图像表现了该体系中-lgc(X)(X为Sr2+或F-)与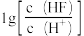 的数量关系。已知100.6=4,下列说法错误的是
的数量关系。已知100.6=4,下列说法错误的是
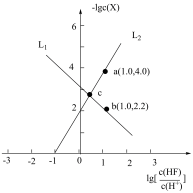
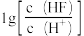 的数量关系。已知100.6=4,下列说法错误的是
的数量关系。已知100.6=4,下列说法错误的是
A.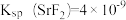 |
| B.a点的溶液中存在c(Cl-)<c(HF) |
C.c点的溶液中存在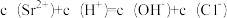 |
| D.由图像可知Ka(HF)的数量级为10-4 |
您最近一年使用:0次

 固体,溶液红色变浅
固体,溶液红色变浅 的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快
的HX和HY两种酸分别与足量的铁反应,排水法收集气体,HX放出的氢气多且反应速率快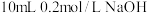 溶液中滴2滴
溶液中滴2滴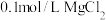 溶液,产生白色沉淀后再滴加2滴
溶液,产生白色沉淀后再滴加2滴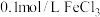 ,又生成红褐色沉淀
,又生成红褐色沉淀

