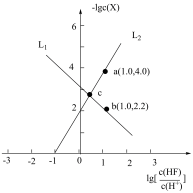
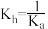SrF2是一种难溶于水、但可溶于酸的盐。在常温下,向SrF2浊液中通入氯化氢气体,得到了如下所示的图像,图像表现了该体系中-lgc(X)(X为Sr2+或F-)与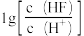 的数量关系。已知100.6=4,下列说法错误的是
的数量关系。已知100.6=4,下列说法错误的是
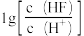 的数量关系。已知100.6=4,下列说法错误的是
的数量关系。已知100.6=4,下列说法错误的是
A.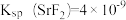 |
| B.a点的溶液中存在c(Cl-)<c(HF) |
C.c点的溶液中存在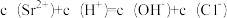 |
| D.由图像可知Ka(HF)的数量级为10-4 |
更新时间:2023-08-29 08:41:08
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知:pKa=- lgKa, 25°C时,弱酸H2A的pKa1=1.85,pKa2=7.19。常温下,用0.1 mo/L NaOH溶液滴定20 mL 0.1 mol/L H2A溶液的曲线如下图所示。

下列说法不正确的是

下列说法不正确的是
| A.d点所得溶液中溶质的水解平衡常数Kh1=10-7.19 |
| B.c点所得溶液中:c(Na+)+c(H+)= 2c(A2-)+ c(HA-)+ c(OH-) |
| C.b点所得溶液中: c(A2-)>c(H2A) |
| D.a点所得溶液中:溶质是NaHA和H2A |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法不正确 的是( )
| A.室温下浓度均为0.1 mol/L的盐酸和氨水混合呈中性时,消耗盐酸的体积大于氨水 |
| B.室温下向0.1 mol/L氨水中加入等浓度等体积的盐酸,溶液导电能力增强 |
| C.室温下pH相等的CH3COOH溶液和盐酸中,c(OH-)相等 |
| D.室温下pH=1的CH3COOH溶液和pH=13的NaOH溶液中,c(CH3COO-)=c(Na+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,一些金属离子(用Mn+表示)形成M(OH)n沉淀与溶液pH平衡关系曲线如图。已知:c(Mn+)≤1×10-5 mol·L-1时可认为金属离子沉淀完全;pM=-lgc(Mn+),pKsp=-lg Ksp。下列叙述正确的是
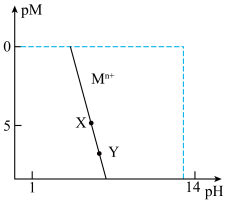

| A.Mn+开始沉淀的pH与起始浓度c(Mn+)无关 |
| B.不同的金属沉淀完全时的pH相同 |
| C.图中Y点与X点pKsp不相同 |
| D.Y点:pM=pKsp+npH-14n |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,下列有关电解质溶液的说法正确的是
| A.相同浓度的HCOONa和NaF溶液,前者的pH较大,则Ka(HCOOH)>Ka(HF) |
B.已知FeS溶于稀硫酸,而CuS不溶于稀硫酸,则 |
| C.相同浓度的CH3COOH和CH3COONa溶液等体积混合后pH约为4.7,则溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.在1mol/LNa2S溶液中,c(S2-)+c(HS-)+c(H2S)=2c(Na+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,用NaOH溶液分别滴定HX、CuSO4、FeSO4三种溶液,pM[p表示负对数,M表示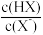 、c(Cu2+)、c(Fe2+)等]随pH变化关系如图所示,已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列说法错误的是
、c(Cu2+)、c(Fe2+)等]随pH变化关系如图所示,已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列说法错误的是
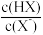 、c(Cu2+)、c(Fe2+)等]随pH变化关系如图所示,已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列说法错误的是
、c(Cu2+)、c(Fe2+)等]随pH变化关系如图所示,已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列说法错误的是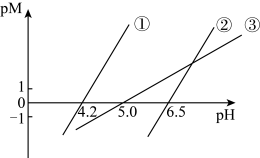
| A.①代表滴定CuSO4溶液的变化关系 |
| B.Cu(OH)2难溶于HX溶液中 |
| C.调整溶液pH=9,无法除去工业废水中的Fe2+ |
| D.HX的电离平衡常数Ka=10-5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,以Na2S为沉淀剂除去废水中的重金属离子A2+ (M2+、N2+、Q2+、R2+),沉淀与离子关系[pA2+=−lg c(A2+),pS2−=−lg c(S2−)]图象如图所示。下列说法正确的是
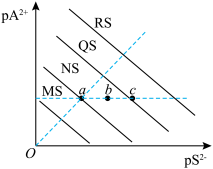

| A.Ksp(MS)<Ksp(NS)<Ksp(QS)<Ksp(RS) |
| B.a、c点的pN2+=pQ2+,向含N2+、Q2+且pN2+=pQ2+的混合液中滴加Na2S溶液,先生成QS沉淀 |
| C.若a点时pS2−=14,pN2+=14,则Ksp(NS)=1028 |
| D.b点对应溶液中不能形成QS沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,分别向MnCl2、ZnCl2、CH3COOH溶液中滴加NaOH溶液,溶液pX[pX=-lgc(X),X代表Mn2+、Zn2+、OH-, ]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是
]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是
 ]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是
]与pH关系如图所示。已知:Ksp[Mn(OH)2]>Ksp[Zn(OH)2]。下列叙述正确的是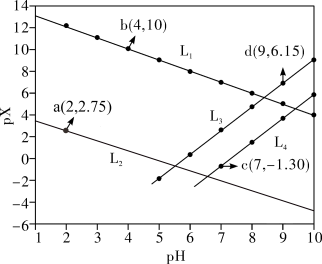
A.图中L2代表 ,L3代表Mn2+ ,L3代表Mn2+ |
| B.室温下,Ksp[Zn(OH)2]的数量级为10-13 |
C.同时产生两种沉淀时,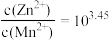 |
D.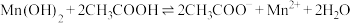 的平衡常数K=105.8 的平衡常数K=105.8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某化学小组利用DIS技术对0.1006mol·L-1醋酸溶液在不同温度下进行电导率测定,得到了如图所示的曲线。下列说法正确的是
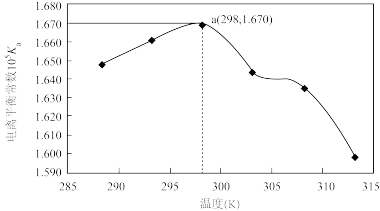
| A.配制0.1006mol·L-1醋酸溶液用到部分仪器是量筒、烧杯、胶头滴管、容量瓶 |
| B.298K时,醋酸的电离平衡常数为1.670 |
| C.温度高于298K,电离平衡常数降低的原因是醋酸电离过程的焓变∆H<0 |
| D.该小组的结论:随着温度升高,弱电解质的电离平衡常数都是先增大,后减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】按一定的速率用0.10
 溶液滴定10.0
溶液滴定10.0 0.10
0.10
 溶液,溶液
溶液,溶液 和温度随
和温度随 的变化曲线如图所示。下列说法正确的是
的变化曲线如图所示。下列说法正确的是


 溶液滴定10.0
溶液滴定10.0 0.10
0.10
 溶液,溶液
溶液,溶液 和温度随
和温度随 的变化曲线如图所示。下列说法正确的是
的变化曲线如图所示。下列说法正确的是
| A.滴定分析时,X点可用甲基橙、Z点可用酚酞作指示剂指示滴定终点 |
B.当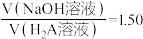 时溶液的 时溶液的 ,且溶液中 ,且溶液中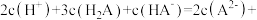 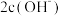 |
C.25℃时, 的电离常数 的电离常数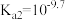 |
D.从W至Z点,Z点水的电离程度和 都最大 都最大 |
您最近一年使用:0次

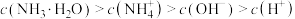
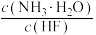 的值减小
的值减小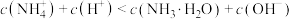



 胶体中的NaCl
胶体中的NaCl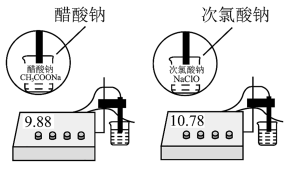

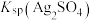 大于
大于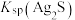
 溶液中主要成分的分布分数[如
溶液中主要成分的分布分数[如 的分布分数表示为
的分布分数表示为 ]随
]随 )。下列说法错误的是
)。下列说法错误的是
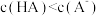
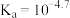
 时,则溶液中
时,则溶液中 约为4
约为4 的水解常数
的水解常数