名校
解题方法
1 . 下列“实验现象”和“结论”的因果关系有错误的是。
| 选项 | 操作 | 现象 | 结论 |
| A | 相同温度下,测定等浓度的 和 和 溶液的pH 溶液的pH | 前者pH比后者大 | 非金属性:S>C |
| B | 火柴梗上滴少量的浓硫酸 | 火柴梗变黑 | 浓硫酸具有强氧化性 |
| C | 将20℃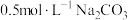 溶液加热到60℃,用pH传感器测定pH 溶液加热到60℃,用pH传感器测定pH | 溶液的pH逐渐减小 |  改变与水解平衡移动共同作用的结果 改变与水解平衡移动共同作用的结果 |
| D | 取一支试管装入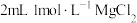 溶液,先滴加 溶液,先滴加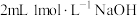 溶液,再滴加几滴 溶液,再滴加几滴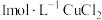 溶液 溶液 | 先生成白色沉淀,后沉淀变为蓝色 | 溶度积: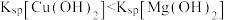 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-09更新
|
106次组卷
|
2卷引用:江西省赣州市全南中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
2 . 下列实验操作和实验现象所对应的实验结论均正确的是
选项 | 实验操作 | 实验现象 | 实验结论 |
A | 把分别盛有NaCl溶液和 胶体的两烧杯置于暗处,均用红色激光笔照射烧杯中的液体 胶体的两烧杯置于暗处,均用红色激光笔照射烧杯中的液体 | 观察到 胶体中有一条光亮的通路,NaCl溶液无明显现象 胶体中有一条光亮的通路,NaCl溶液无明显现象 | 丁达尔效应是胶体和溶液的本质区别 |
B | 向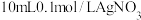 溶液中先滴入5滴0.1mol/LNaCl溶液,再滴入5滴0.1mol/L的KI溶液 溶液中先滴入5滴0.1mol/LNaCl溶液,再滴入5滴0.1mol/L的KI溶液 | 先产生白色沉淀,后产生黄色沉淀 | 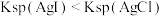 |
C | 向2支试管各加入 的草酸溶液,分别滴加 的草酸溶液,分别滴加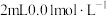 、 、 高锰酸钾溶液 高锰酸钾溶液 | 高锰酸钾溶液褪色并观察褪色时间 | 其他条件不变时,反应物浓度越大,反应速率越快 |
D | 取淀粉溶液于试管中,加入适量稀 后水浴加热5min,冷却后先加足量NaOH溶液,再加入适量新制 后水浴加热5min,冷却后先加足量NaOH溶液,再加入适量新制 悬浊液并加热煮沸 悬浊液并加热煮沸 | 生成砖红色沉淀 | 淀粉已水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-08更新
|
135次组卷
|
2卷引用:江西省乐安县第二中学2023-2024学年高三上学期开学考试化学试题
解题方法
3 . 化学与社会、生活密切相关,下列说法不正确 的是
A.锅炉水垢中含有的 ,可先用 ,可先用 溶液处理,后用酸除去 溶液处理,后用酸除去 |
| B.食品中添加适量的二氧化硫,可以起到漂白、防腐和抗氧化等作用 |
| C.神舟十四号飞船返回舱外面的材料是耐高温的陶瓷,属于新型无机非金属材料 |
| D.明矾净水与自来水的杀菌消毒原理相同 |
您最近一年使用:0次
名校
4 . 化学与生产、生活息息相关。下列说法错误的是
| A.热的纯碱溶液可用于清洗厨房油污 |
| B.霓红灯的发光机制与氢原子光谱形成的机制基本相同 |
C.误服 或 或 后可用 后可用 溶液解毒 溶液解毒 |
D. 可以用于天然水的消毒、净化 可以用于天然水的消毒、净化 |
您最近一年使用:0次
名校
5 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向3mL KI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色 | Br2的氧化性比I2的强 |
B | 向浓度均为0.05mol·L−1的NaI、NaCl混合溶液中滴加少量AgNO3溶液,有黄色沉淀生成 | Ksp(AgI)> Ksp(AgCl) |
C | 某溶液中滴加K3[Fe(CN)6]溶液,产生蓝色沉淀 | 原溶液中有Fe2+,无Fe3+ |
D | 用pH试纸测得:CH3COONa溶液的pH约为9,NaNO2溶液的pH约为8 | HNO2电离出H+的能力比CH3COOH的强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列表中实验操作、现象与结论对应关系正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体 固体 | 有白色沉淀生成,溶液红色变浅 | 纯碱溶液呈碱性是由 水解引起 水解引起 |
| B | 向盛有2mL NaOH溶液的试管中滴加4~5滴 NaOH溶液的试管中滴加4~5滴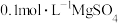 溶液,再向其中滴加 溶液,再向其中滴加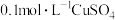 溶液 溶液 | 先生成白色沉淀,后生成蓝色沉淀 | 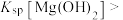  |
| C | 常温下,用玻璃棒蘸取某浓度NaOH溶液滴在湿润的pH试纸中央,与标准比色卡对比 | pH为13 | 该NaOH溶液的浓度为 |
| D | 分别取两支洁净的试管,甲试管中加入10mL 溶液,乙试管中加入5mL 溶液,乙试管中加入5mL 溶液和5mL蒸馏水,然后同时向两支试管中加入10mL 溶液和5mL蒸馏水,然后同时向两支试管中加入10mL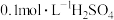 溶液 溶液 | 甲试管出现浑浊的时间更短 | 增大 浓度,可以加快反应速率 浓度,可以加快反应速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-08更新
|
88次组卷
|
2卷引用:江西省丰城中学2022-2023学年高二下学期入学考试化学试题
7 . 常温下,难溶物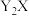 与ZX在水中的沉淀溶解平衡曲线如图所示,若定义其坐标图示,
与ZX在水中的沉淀溶解平衡曲线如图所示,若定义其坐标图示,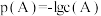 ,
, 表示
表示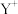 或
或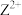 。下列说法错误的是
。下列说法错误的是
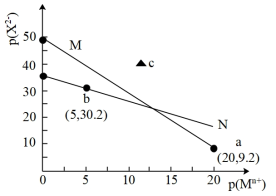
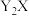 与ZX在水中的沉淀溶解平衡曲线如图所示,若定义其坐标图示,
与ZX在水中的沉淀溶解平衡曲线如图所示,若定义其坐标图示,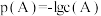 ,
, 表示
表示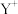 或
或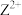 。下列说法错误的是
。下列说法错误的是
A.N表示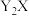 的溶解平衡曲线 的溶解平衡曲线 |
B.常温下,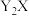 的分散系在c点时为悬浊液 的分散系在c点时为悬浊液 |
C.向b点溶液中加入 饱和溶液,析出ZX固体 饱和溶液,析出ZX固体 |
D.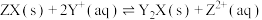 的平衡常数 的平衡常数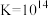 |
您最近一年使用:0次
2022-12-06更新
|
127次组卷
|
2卷引用:江西省丰城中学2022-2023学年高二下学期开学考试化学试题
8 . 工业生产中利用方铅矿(主要成分为PbS,含有FeS2等杂质)制备PbSO4晶体的工艺流程如图:

已知:PbCl2难溶于冷水,易溶于热水;PbCl2(s)+2Cl-(aq) PbCl
PbCl (aq) △H>0;Ksp(PbSO4)=1×10-8,Ksp(PbCl2)=1.6×10-5。下列说法错误的是
(aq) △H>0;Ksp(PbSO4)=1×10-8,Ksp(PbCl2)=1.6×10-5。下列说法错误的是

已知:PbCl2难溶于冷水,易溶于热水;PbCl2(s)+2Cl-(aq)
 PbCl
PbCl (aq) △H>0;Ksp(PbSO4)=1×10-8,Ksp(PbCl2)=1.6×10-5。下列说法错误的是
(aq) △H>0;Ksp(PbSO4)=1×10-8,Ksp(PbCl2)=1.6×10-5。下列说法错误的是| A.“浸取”时的主要离子反应为MnO2+PbS+4H++2Cl-=PbCl2 +S+Mn2++2H2O |
| B.“滤渣2”的主要成分是Fe(OH)3 |
C.“沉降”时加入冰水,PbCl2(s)+2Cl-(aq) PbCl PbCl (aq)平衡左移,有利于PbCl2沉淀更完全 (aq)平衡左移,有利于PbCl2沉淀更完全 |
D.“沉淀转化”过程达平衡时,溶液中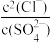 =1.6×103 =1.6×103 |
您最近一年使用:0次
2022-07-19更新
|
729次组卷
|
4卷引用:江西省九校2022-2023学年高二下学期开学联考化学试题
江西省九校2022-2023学年高二下学期开学联考化学试题湖南省长沙麓山国际实验学校2023-2024学年高二下学期第一次学情检测化学试卷 河北省石家庄市第二中学教育集团2021-2022学年高二下学期期末考试化学试题(已下线)3.4.2 沉淀溶解平衡的应用-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)
名校
解题方法
9 . 以印刷线路板酸性蚀刻废液(含有CuCl2、FeCl2、FeCl3)为原料制备纳米CuO的流程如图:
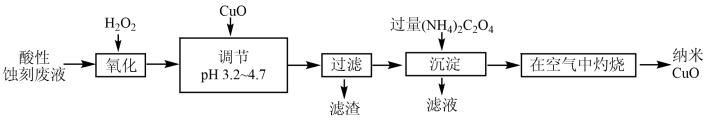
下列说法错误的是

下列说法错误的是
| A.“沉淀”产生的CuC2O4,不洗涤直接灼烧不影响产品质量 |
| B.“在空气中灼烧”时发生了非氧化还原反应 |
| C.调节pH为3.2~4.7的目的是使Fe3+完全沉淀,Cu2+不沉淀 |
| D.“沉淀”过程中用Na2C2O4代替(NH4)2C2O4,得到的CuC2O4中可能混有Cu(OH)2 |
您最近一年使用:0次
2022-06-01更新
|
725次组卷
|
6卷引用:江西省新余市第一中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
10 . 氧化钴(Co2O3)在工业、电子、电讯等领域都有着广阔的应用前景。以铜钴矿石[主要成分为CoO(OH),CoCO3、Cu2(OH)2CO3和 SiO2,还有少量Fe、Mg、Ca的氧化物]为原料制备氧化钴(Co2O3)的工艺流程如图所示:

已知:常温下:Ksp(FeS)=6.3×10-18 Ksp(CuS)=6.3×10-36 Ksp(CaF2)=4.0×10-11 Ksp(MgF2)=9.0×10-11。
回答下列问题:
(1)写出“浸泡”过程中CoO(OH)与Na2SO3反应的离子方程式_______ 。
(2)“除铜”过程中,加入FeS固体得到更难溶的CuS,写出“除铜”过程的离子方程式_______ 。
(3)检验过程Ⅰ所得滤液中铁元素的离子已被完全沉淀的实验操作及现象:取少量待测液于试管中,_______ 。
(4)常温下,在过程Ⅱ中加入足量的NaF溶液可除去Ca2+、Mg2+,当两者沉淀完全时F-的浓度至少为_______ mol·L-1(溶液中离子浓度小于1×10-5 mol·L-1视为该离子沉淀完全)。
(5)过程Ⅲ中加入Na2CO3得到滤渣后又加入盐酸溶解,其目的是_______ 。

已知:常温下:Ksp(FeS)=6.3×10-18 Ksp(CuS)=6.3×10-36 Ksp(CaF2)=4.0×10-11 Ksp(MgF2)=9.0×10-11。
回答下列问题:
(1)写出“浸泡”过程中CoO(OH)与Na2SO3反应的离子方程式
(2)“除铜”过程中,加入FeS固体得到更难溶的CuS,写出“除铜”过程的离子方程式
(3)检验过程Ⅰ所得滤液中铁元素的离子已被完全沉淀的实验操作及现象:取少量待测液于试管中,
(4)常温下,在过程Ⅱ中加入足量的NaF溶液可除去Ca2+、Mg2+,当两者沉淀完全时F-的浓度至少为
(5)过程Ⅲ中加入Na2CO3得到滤渣后又加入盐酸溶解,其目的是
您最近一年使用:0次



