解题方法
1 . 下表中实验操作、现象与结论对应关系正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 以酚酞为指示剂,用盐酸标准液滴定氢氧化钠溶液 | 溶液由红色变为浅红色便立刻读数 | 测得c(NaOH)偏大 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 有白色沉淀生成,溶液红色变浅 | 纯碱溶液呈碱性是由 水解引起 水解引起 |
| C | 测定等浓度的NaClO溶液、CH3COONa溶液的pH | 前者大 | 酸性:HClO>CH3COOH |
| D | 除去锅炉中沉积的CaSO4用饱和Na2CO3溶液浸泡,再用稀盐酸溶解除去 | 白色沉淀溶解 | CaSO4比CaCO3的 小 小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 下列实验操作、现象和结论均正确且具有对应关系的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向FeBr2溶液中通入Cl2 | 溶液变黄 | 氧化性:Cl2>Br2 |
| B | 将石蜡油在碎瓷片上强热,产生的气体通入酸性KMnO4溶液中 | 溶液紫色褪色 | 石蜡油分解产物为乙烯 |
| C | 向CaCl2溶液中通入CO2 | 溶液变浑浊 | 生成了CaCO3 |
| D | 在试管装入2mL1mol·L-1MgCl2溶液,先滴加1mL1mol·L-1NaOH溶液,再滴加几滴1mol·L-1CuCl2溶液 | 先生成白色沉淀,后变为蓝色 | Ksp: Cu(OH)2<Mg(OH)2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 表中实验操作、现象与结论对应关系均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 等体积pH=2的两种酸HX和HY分别与足量的锌反应 | HX溶液中放出的H2多 | HX的酸性比HY强 |
| B | 用广泛pH试纸测定1mol/LNaHSO3溶液的酸碱性 | 测得pH=3.2 | NaHSO3溶液呈酸性,证明HSO 在水中的电离程度小于水解程度 在水中的电离程度小于水解程度 |
| C | 在KSCN与FeCl3的混合液中再加入KCl固体 | 溶液颜色变浅 | 增大生成物浓度,平衡逆向移动 |
| D | 向浓度均为0.1mol/L的NaCl和NaI的混合溶液中滴加少量0.1mol/L的AgNO3溶液 | 产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-16更新
|
680次组卷
|
8卷引用:辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校五校协作体2020-2021学年高二上学期期末化学试题
辽宁省实验中学、大连八中、大连二十四中、鞍山一中、东北育才学校五校协作体2020-2021学年高二上学期期末化学试题黑龙江省哈尔滨市第六中学2021-2022学年高二上学期期末考试化学试题湖南省永州市宁远县第一中学2022-2023学年高二上学期期中考试化学试题广东省江门市培英高级中学2022-2023学年高二上学期期中考试化学试题江西省临川第二中学2022-2023学年高二上学期第三次月考化学试题湖南省衡阳县2022-2023学年高二上学期期末考试化学试题广东省梅州市兴宁市沐彬中学2021-2022学年高二下学期期中考试化学试题江西省宜春市宜丰中学2023-2024学年高二上学期10月月考化学试题
4 . 下列实验“操作和现象”与“结论”对应关系均正确的
| 操作和现象 | 结论 | |
| A | 处理锅炉水垢中的CaSO4时,依次加入饱和Na2CO3溶液和盐酸,水垢溶解 | Ksp:CaCO3>CaSO4 |
| B | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色 | 溶液中一定含有Fe2+ |
| C | 向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色 | 还原性Br->Cl- |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有Ag+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-02-17更新
|
311次组卷
|
2卷引用:2016-2017学年贵州省凯里一中高二上期末化学卷
5 . 下列实验操作、现象与结论对应关系正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向盛有Fe(NO3)2溶液的试管中加入0.1 mol/L H2SO4溶液 | 试管口出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
| B | 向SO2水溶液中滴入几滴BaCl 2溶液,振荡 | 滴加BaCl2后出现白色沉淀 | 此沉淀一定是BaSO3 |
| C | 等体积PH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | HB酸性比HA强 |
| D | 先向2mL 0.1mol/L Na2S溶液中滴入几滴0.1mol/LZnSO4溶液,再加入几滴0.1mol/L CuSO4溶液 | 开始有白色沉淀生成;后又有黑色沉淀生成 | 溶度积(Ksp):ZnS>CuS |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
12-13高二下·安徽安庆·期末
6 . 下列实验“操作和现象”与“结论”对应关系均正确的是( )
| 操作和现象 | 结论 | |
| A | 处理锅炉水垢中的CaSO4时,依次加入饱和Na2CO3溶液和盐酸,水垢溶解 | Ksp:CaCO3<CaSO4 |
| B | 用石墨作电极电解MgSO4溶液,某电极附近有白色沉淀生成 | 该电极为阳极 |
| C | 向FeCl3和CuCl2混合溶液中加入少量铁粉,有红色固体析出 | 氧化性:Cu2+<Fe3+ |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有Ag+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2013-08-07更新
|
283次组卷
|
4卷引用:2012-2013学年安徽省桐城市天城中学高二下学期期末考试化学试卷
(已下线)2012-2013学年安徽省桐城市天城中学高二下学期期末考试化学试卷2015届山西大学附中高三12月月考化学试卷2015-2016学年河南省许昌市四校高二上学期第三次联考化学试卷2015-2016学年湖北省汉川市高二上学期期末考试化学试卷
7 . 下列有关物质的性质和用途具有因果关系的是
| 选项 | 性质 | 用途 |
| A | 小苏打溶液呈碱性 | 小苏打常用作食品膨松剂 |
| B | Zn的金属性比Fe强 | 在轮船船体镶嵌锌块,防止轮船腐蚀 |
| C | FeS不溶于水 | 用FeS除去废水中的Hg2+ |
| D | 重金属盐可以使蛋白质变性 | 在煮沸的豆浆中加入石膏粉制豆腐 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-18更新
|
95次组卷
|
3卷引用:河北省石家庄市辛集中学、衡水中学2023-2024高三上学期期末联考化学试题
名校
解题方法
8 . 铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅等的氧化物,从铬钒渣中分离提取铬和钒的一种流程如图所示。下列说法正确的是
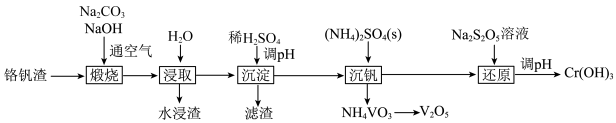
已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
② 。
。

已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
②
 。
。A.“煅烧”后的含铬化合物是 |
B.“滤渣”中只含有 |
C.“沉钒”时 固体可增大 固体可增大 的浓度,有利于沉淀的生成 的浓度,有利于沉淀的生成 |
D.“还原”工序中氧化剂和还原剂的物质的量之比为 |
您最近一年使用:0次
2023-12-03更新
|
373次组卷
|
2卷引用:山东省菏泽市2023-2024学年高三上学期期中化学试题
名校
9 . 下列物质的用途或事实与盐类的水解无关的是
A.用 溶液处理锅炉水垢中的 溶液处理锅炉水垢中的 |
B.明矾[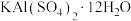 ]用于净水 ]用于净水 |
C.用热饱和 溶液清洗试管壁上附着的植物油 溶液清洗试管壁上附着的植物油 |
D.由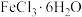 制取无水 制取无水 固体时,需在HCl气流中蒸发 固体时,需在HCl气流中蒸发 |
您最近一年使用:0次
2023-11-29更新
|
312次组卷
|
3卷引用:北京师范大学附属实验中学2023-2024学年高二上学期期中考试化学试题
名校
10 . 四氯化钛(TiCl4)是工业生产重要中间产品的原料,并有着广泛的用途。它为无色或淡黄色液体,熔点为—30℃,沸点为136.4℃,极易水解。在实验室用钛铁矿(FeTiO3)为原料制备TiCl4实验装置如图所示:
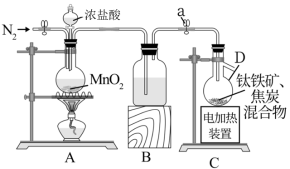
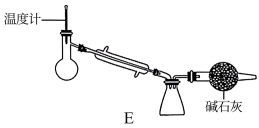
已知:(1)FeCl3熔点为306℃,沸点为316℃,极易水解;
(2)①Ag++SCN—=AgSCN↓;②Ksp(AgCl)>Ksp(AgSCN)。
请回答下列问题:
(1)装置A加热前先通一段时间N2,其目的是___ 。
(2)仪器D的名称是___ ;装置B中盛放的试剂名称是___ 。
(3)装置A中发生反应的离子方程式为___ 。
(4)装置C中发生反应的化学方程式为___ 。
(5)该制备装置不足之处:
①无尾气处理装置,CO与剩余Cl2会污染环境;
②___ 。
(6)停止滴加浓盐酸并关闭止水夹a,将装置c中所得物质转移到装置E中进行相关操作。装置E的作用是___ 。
(7)测定TiCl4产品的纯度。实验步骤如下:
①E装置相关操作结束后,待锥形瓶中的液体冷却至室温,准确称取14.0gTiCl4产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,过滤后将水解液配成100.00mL溶液。
②取10.00mL溶液于锥形瓶中,加入10.00mL2.900mol•L-1AgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X溶液为指示剂,用0.1000mol•L-1KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00mLKSCN溶液。
根据以上步骤计算产品中TiCl4的质量分数为___ (已知产品中杂质不参与反应);若省去步骤③,所测定TiCl4产品的质量分数将会___ (选填“偏大”“偏小”或“不变”)。


已知:(1)FeCl3熔点为306℃,沸点为316℃,极易水解;
(2)①Ag++SCN—=AgSCN↓;②Ksp(AgCl)>Ksp(AgSCN)。
请回答下列问题:
(1)装置A加热前先通一段时间N2,其目的是
(2)仪器D的名称是
(3)装置A中发生反应的离子方程式为
(4)装置C中发生反应的化学方程式为
(5)该制备装置不足之处:
①无尾气处理装置,CO与剩余Cl2会污染环境;
②
(6)停止滴加浓盐酸并关闭止水夹a,将装置c中所得物质转移到装置E中进行相关操作。装置E的作用是
(7)测定TiCl4产品的纯度。实验步骤如下:
①E装置相关操作结束后,待锥形瓶中的液体冷却至室温,准确称取14.0gTiCl4产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,过滤后将水解液配成100.00mL溶液。
②取10.00mL溶液于锥形瓶中,加入10.00mL2.900mol•L-1AgNO3标准溶液。
③加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖。
④以X溶液为指示剂,用0.1000mol•L-1KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00mLKSCN溶液。
根据以上步骤计算产品中TiCl4的质量分数为
您最近一年使用:0次



