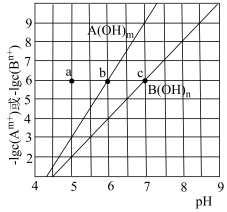
| A.m:n=3:2 |
| B.Ksp[A(OH)m]<Ksp[B(OH)n] |
| C.饱和A(OH)m溶液和饱和B(OH)n溶液中:c(Bn+)<c(Am+) |
| D.若溶液中c(Am+)的浓度如a点所示,则加入NaOH可使溶液沿水平线向右移动至b点 |
 溶液与过量
溶液与过量 固体混合,溶液
固体混合,溶液 随时间变化如图所示。
随时间变化如图所示。
已知:
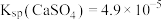
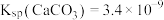
下列说法
A.两者混合发生反应: |
B.随着反应的进行, 逆向移动,溶液 逆向移动,溶液 下降 下降 |
C.充分反应后上层清液中 约为 约为 |
D. 内上层清液中存在: 内上层清液中存在: |
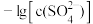 、
、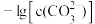 与
与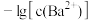 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是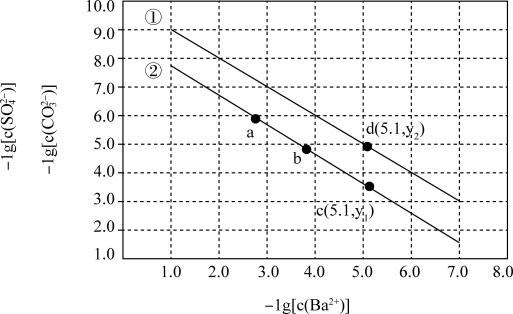
| A.曲线②代表BaCO3的沉淀溶解曲线 |
| B.加适量BaCl2固体可使溶液由a点变到b点 |
C.该温度下BaSO4的Ksp(BaSO4)为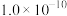 |
D.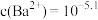 时,两溶液中 时,两溶液中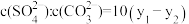 |
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向NaHCO3溶液中滴入酚酞,溶液变成红色 | HCO 的水解程度大于其电离程度 的水解程度大于其电离程度 |
| B | 向NaOH固体中加入少量稀盐酸,测得温度高于室温 | 盐酸与NaOH的反应为放热反应 |
| C | 室温下,测得相同浓度的NaX和NaY溶液的pH分别为8和9 | 酸性:HX<HY |
| D | 向等浓度的NaCl、KI的混合溶液中滴加少量AgNO3溶液,得到黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| A.A | B.B | C.C | D.D |
| 选项 | 实验 | 现象 | 结论 |
| A | 相同条件下,用0.1mol·L−1的CH3COOH和0.1mol·L−1的HCl分别做导电性实验 | CH3COOH溶液对应的灯泡较暗 | CH3COOH是弱电解质 |
| B | 向某溶液中加铜和浓H2SO4 | 试管口有红棕色气体产生 | 原溶液可能含有NO |
| C | 向某钠盐中滴加浓盐酸,将产生的气体通入品红溶液 | 品红溶液褪色 | 该钠盐为Na2SO3或NaHSO3 |
| D | 向浓度均为0.1mol·L−1的MgCl2、CuCl2混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | 溶解度:Cu(OH)2<Mg(OH)2 |
| A.A | B.B | C.C | D.D |
(2)常温下,将pH=3的盐酸aL分别与下列三种溶液混合,所得溶液均呈中性。
①浓度为1.0×10-3mol·L-1的氨水bL;②c(OH-)=1×10-3mol·L-1的氨水cL;③c(OH-)=1×10-3mol·L-1的氢氧化钡溶液dL,则a、b、c、d之间的大小关系是
(3)某温度时,测得0.01mol·L-1NaOH溶液的pH=10。在此温度下,将pH=2的H2SO4溶液VaL与pH=12的NaOH溶液VbL混合,若所得混合液pH=11,则Va:Vb=
(4)已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+⇌Fe3++3H2O的平衡常数K=
7 . 根据题目提供的溶度积数据进行计算并回答下列问题:
(1)已知25℃时,Ksp[Mg(OH)2]=5.6×10﹣12;酸碱指示剂百里酚蓝变色的pH范围如下:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25℃时,在Mg(OH)2饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为
(2)向50mL0.018mol•L﹣1的AgNO3溶液中加入50mL0.020mol•L﹣1的盐酸,生成沉淀。已知该温度下AgCl的Ksp=1.0×10﹣10,忽略溶液的体积变化,请计算:
①完全沉淀后,溶液中c(Ag+)=
②完全沉淀后,溶液的pH=
③如果向完全沉淀后的溶液中继续加入50mL0.001mol•L﹣1的盐酸,是否有白色沉淀生成?
(3)在某温度下,Ksp(FeS)=6.25×10﹣18,FeS饱和溶液中c(H+)与c(S2﹣)之间存在关系:c2(H+)•c(S2﹣)=1.0×10﹣22,为了使溶液里c(Fe2+)达到1mol•L﹣1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)约为
| 物质 | AgCl | AgBr | AgI | Ag2S |
| 颜色 | 白 | 淡黄 | 黄 | 黑 |
| Ksp | 1.8×10-10 | 7.7×10-13 | 1.5×10-16 | 1.8×10-50 |
| A.向AgCl的白色悬浊液中加入0.1 mol/L KI溶液,有黄色沉淀产生 |
| B.25 ℃时,利用表中的溶度积(Ksp),可以计算AgCl、AgBr、AgI、Ag2S饱和水溶液中Ag+的浓度 |
| C.25 ℃,AgCl固体分别在等物质的量浓度NaCl、CaCl2溶液中溶解达到平衡,两溶液中,c(Ag+)和溶度积均相同 |
| D.在5 mL 1.8×10-6 mol/L NaCl溶液中,加入1滴(20滴约为1 mL)1×10-3 mol/L AgNO3溶液,不能产生白色沉淀 |
| A.AgCl、AgBr、AgI | B.AgI、AgBr、AgCl |
| C.AgBr、AgCl、AgI | D.三种沉淀同时析出 |



