名校
解题方法
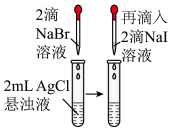
1 . 下列操作或装置能达到实验目的的是
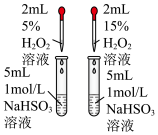
| A.证明Ksp(AgBr)>Ksp(AgI) | B.探究浓度对反应速率的影响 |
|
|
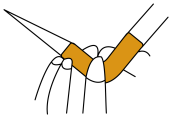
| C.碱式滴定管排气泡 | D.制备FeSO4固体 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 已知Ksp(AgCl)=1.56×10-10、Ksp(AgBr)=7.7×10-13、Ksp(Ag2CrO4)=9×10-11,某溶液中含有Cl-、Br-和CrO ,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
 ,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为A. Cl-、Br-、CrO | B.Br-、Cl-、CrO | C.CrO42-、Br-、Cl- | D.Br-、CrO 、Cl- 、Cl- |
您最近一年使用:0次
3 . 硫化汞(HgS)是一种难溶于水的红褐色颜料,其在水中的沉淀溶解平衡曲线如图所示(已知T1<T2),下列说法错误的是


| A.图中a点对应的是T2温度下HgS的不饱和溶液 |
| B.图中各点对应的Ksp的关系为:p<q |
| C.向p点的溶液中加入少量Hg(NO3)2固体,p点向a点转化 |
| D.升高温度,可实现p点向q点的转化 |
您最近一年使用:0次
4 . 秦俑彩绘中含有难溶的铅白(PbCO3)和黄色的PbI2。常温下,PbCO3和PbI2在水溶液中各自分别达到沉淀溶解平衡时pM与pR的关系如图所示,其中pM为阳离子浓度的负对数,pR为阴离子浓度的负对数。下列说法正确的是


| A.PbCO3转化为PbI2的反应趋势很大 |
| B.z点溶液对于PbCO3来说尚未饱和 |
| C.Ksp(PbI2)的数量级为10-14 |
D.完全沉淀废液中的Pb2+,I-的效果不如CO |
您最近一年使用:0次
名校
解题方法
5 . 下列说法中正确的是
A. 的溶液中: 的溶液中: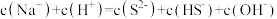 |
B.浓度均为 的① 的① ② ② ③ ③ ④ ④ , , 由小到大的顺序:④<③<①<② 由小到大的顺序:④<③<①<② |
C.向 、 、 的混合饱和溶液中加入少量 的混合饱和溶液中加入少量 ,溶液中 ,溶液中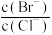 减小 减小 |
D. 溶液中离子浓度大小顺序为 溶液中离子浓度大小顺序为 |
您最近一年使用:0次
2024-01-15更新
|
264次组卷
|
2卷引用:广东省深圳市罗湖高级中学2023-2024学年高二上学期12月阶段性考试化学试题
解题方法
6 . 稀土抛光粉 有优良抛光性能。某抛光后产生的抛光渣(含
有优良抛光性能。某抛光后产生的抛光渣(含 、
、 、
、 、
、 、
、 、
、 等的化合物)进行提纯的工艺如下:
等的化合物)进行提纯的工艺如下:
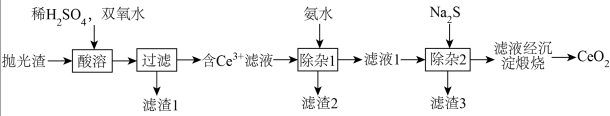
已知:25℃时, ,
,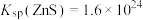 ,
, 。一定条件下,一些金属氢氧化物沉淀时的
。一定条件下,一些金属氢氧化物沉淀时的 如下表:
如下表:
(1)“酸溶”时,需控制80℃水浴加热,若温度过高浸出率降低的原因是_____ 。 发生反应的离子方程式为
发生反应的离子方程式为_____ 。
(2)“滤渣1”的主要成分为_____ 。
(3)“除杂1”中,加入氨水控制 范围为
范围为_____ ,溶液中
_____  (填“>”“=”或“<”)。“除杂2”中,主要除去的金属元素为
(填“>”“=”或“<”)。“除杂2”中,主要除去的金属元素为_____ 。
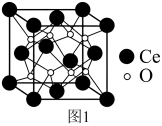
(4) 的晶胞结构如图1所示,晶胞参数为
的晶胞结构如图1所示,晶胞参数为 ,
, 原子处于
原子处于 形成的四面体间隙中。则
形成的四面体间隙中。则 原子的配位数为
原子的配位数为_____ ,晶胞密度为_____  。(列出计算式,
。(列出计算式, 的式量为
的式量为 ,阿伏加德罗常数为
,阿伏加德罗常数为 )
)
(5)纳米 分散液用于光学玻璃抛光时,
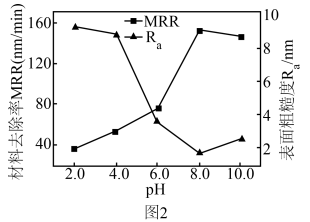
分散液用于光学玻璃抛光时, 值对抛光效果(材料抛光去除速率及抛光后表面粗糙度)的影响如图所示,已知抛光液中,
值对抛光效果(材料抛光去除速率及抛光后表面粗糙度)的影响如图所示,已知抛光液中, 纳米颗粒表面吸附了负电荷相互排斥而稳定。从图2中可看出,最佳
纳米颗粒表面吸附了负电荷相互排斥而稳定。从图2中可看出,最佳 值为
值为_____ ,在较低 值,抛光效果不理想的原因为
值,抛光效果不理想的原因为_____ 。
 有优良抛光性能。某抛光后产生的抛光渣(含
有优良抛光性能。某抛光后产生的抛光渣(含 、
、 、
、 、
、 、
、 、
、 等的化合物)进行提纯的工艺如下:
等的化合物)进行提纯的工艺如下:
已知:25℃时,
 ,
,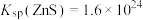 ,
, 。一定条件下,一些金属氢氧化物沉淀时的
。一定条件下,一些金属氢氧化物沉淀时的 如下表:
如下表:| 金属氢氧化物 |  |  |  | 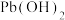 |  |
开始沉淀的 | 2.3 | 3.5 | 6.4 | 7.2 | 6.2 |
完全沉淀的 | 3.2 | 4.6 | 9.0 | 9.1 | 8.2 |
 发生反应的离子方程式为
发生反应的离子方程式为(2)“滤渣1”的主要成分为
(3)“除杂1”中,加入氨水控制
 范围为
范围为
 (填“>”“=”或“<”)。“除杂2”中,主要除去的金属元素为
(填“>”“=”或“<”)。“除杂2”中,主要除去的金属元素为(4)
 的晶胞结构如图1所示,晶胞参数为
的晶胞结构如图1所示,晶胞参数为 ,
, 原子处于
原子处于 形成的四面体间隙中。则
形成的四面体间隙中。则 原子的配位数为
原子的配位数为 。(列出计算式,
。(列出计算式, 的式量为
的式量为 ,阿伏加德罗常数为
,阿伏加德罗常数为 )
) 
(5)纳米
 分散液用于光学玻璃抛光时,
分散液用于光学玻璃抛光时, 值对抛光效果(材料抛光去除速率及抛光后表面粗糙度)的影响如图所示,已知抛光液中,
值对抛光效果(材料抛光去除速率及抛光后表面粗糙度)的影响如图所示,已知抛光液中, 纳米颗粒表面吸附了负电荷相互排斥而稳定。从图2中可看出,最佳
纳米颗粒表面吸附了负电荷相互排斥而稳定。从图2中可看出,最佳 值为
值为 值,抛光效果不理想的原因为
值,抛光效果不理想的原因为
您最近一年使用:0次
名校
解题方法
7 . 按要求回答下列问题:
(1)配制FeCl3溶液时,需将固体溶于较浓的盐酸后按需要进行稀释,用离子方程式解释其原因_______ 。
(2)常温下,浓度均为0.1mol/L的下列五种溶液的pH值如下表所示:
①根据表中数据,将pH=2的下列四种酸的溶液分别稀释100倍,pH变化最小的是_______ 。
A. HCN B. HClO C. H2CO3 D. CH3COOH
②根据以上数据,判断下列反应可以成立的是_______ 。(填字母)
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.NaHCO3+HCN=NaCN+H2O+CO2
(3)已知在Cu2+、Mg2+、Fe2+浓度相同的溶液中,其开始沉淀时的pH如下:
①若向该溶液中滴加NaOH溶液,则离子沉淀先后顺序是_______ (填离子符号)。
②已知Ksp[Cu(OH)2]=2.5×10-20,若向该溶液中加入生石灰调节其pH,当pH=_______ 时,溶液中Cu2+沉淀完全。[已知1g2=0.3]
③下列说法不正确的是_______ (填字母)。
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl少
B.一般地,物质的溶解度随温度的升高而增加,故物质的溶解大多是吸热的
C.除去溶液中的Mg2+,用OH-沉淀比用CO 好,说明Mg(OH)2的溶解度比MgCO3的大
好,说明Mg(OH)2的溶解度比MgCO3的大
D.沉淀反应中常加过量的沉淀剂,其目的是使沉淀更完全
(1)配制FeCl3溶液时,需将固体溶于较浓的盐酸后按需要进行稀释,用离子方程式解释其原因
(2)常温下,浓度均为0.1mol/L的下列五种溶液的pH值如下表所示:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
A. HCN B. HClO C. H2CO3 D. CH3COOH
②根据以上数据,判断下列反应可以成立的是
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.NaHCO3+HCN=NaCN+H2O+CO2
(3)已知在Cu2+、Mg2+、Fe2+浓度相同的溶液中,其开始沉淀时的pH如下:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
②已知Ksp[Cu(OH)2]=2.5×10-20,若向该溶液中加入生石灰调节其pH,当pH=
③下列说法不正确的是
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl少
B.一般地,物质的溶解度随温度的升高而增加,故物质的溶解大多是吸热的
C.除去溶液中的Mg2+,用OH-沉淀比用CO
 好,说明Mg(OH)2的溶解度比MgCO3的大
好,说明Mg(OH)2的溶解度比MgCO3的大D.沉淀反应中常加过量的沉淀剂,其目的是使沉淀更完全
您最近一年使用:0次
2023-06-07更新
|
57次组卷
|
2卷引用:广东省梅州市大埔县虎山中学2022-2023学年高二上学期12月月考化学试题
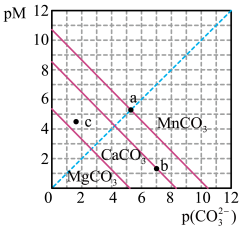
8 . 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如下图所示。已知:pM=-lgc(M),pc(CO )=-lgc(CO
)=-lgc(CO )。下列说法正确的是
)。下列说法正确的是
 )=-lgc(CO
)=-lgc(CO )。下列说法正确的是
)。下列说法正确的是
| A.MgCO3、CaCO3、MnCO3的Ksp依次增大 |
B.a点可表示MnCO3的饱和溶液,且c(Mn2+)=c(CO ) ) |
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO ) ) |
D.c点可表示MgCO3的过饱和溶液,且c(Mg2+)>c(CO ) ) |
您最近一年使用:0次
名校
9 . 根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 室温下,0.1 mol∙L−1CH3COONa溶液的pH大于7 | 乙酸是弱酸 |
| B | 室温下,向浓度均为0.1 mol∙L−1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀 | Ksp(BaSO4)<Ksp(CaSO4) |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的还原性比I2的强 |
| D | 室温下,用pH试纸测得:0.1 mol∙L−1Na2SO3溶液的pH约为10;0.1 mol∙L−1NaHSO3溶液的pH约为5 | HSO 结合H+的能力比SO 结合H+的能力比SO 的强 的强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 下列类比或推理合理的是
| 已知 | 方法 | 结论 | |
| A | 沸点: | 类比 | 沸点:Li<Na<K |
| B | 酸性:三氟乙酸>三氯乙酸 | 类比 | 酸性:氢氟酸>氢氯酸 |
| C | 金属性:Na>Mg>Al | 推理 | 碱性: |
| D |  : :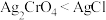   | 推理 | 溶解度: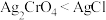 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-18更新
|
384次组卷
|
3卷引用:广东省部分学校2023届高三5月联合考试化学试题