解题方法
1 . 广安代市镇火力发电厂需要燃烧大量的煤,产生大量CO2和SO2等,并留下大量煤渣,对环境有较大影响。其中一种不能继续燃烧的煤渣成分俗名叫“铁甲石”,主要成分为:Al2O3(15%~24%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)、FeO(0.9%~2.0%)、CuO(8.5%~11.0%)以及其他不溶性杂质,铁甲石中的氧化铝难溶于酸,可以通过煅烧改变铁甲石结构,使其溶于酸。铁甲石经过下列化工工艺,可以制取无水CuCl2。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
(1)第一次过滤的滤渣为___________ 。
(2)加H2O2后发生反应的离子方程式为___________ 。
(3)调节溶液pH需要控制的范围是___________ ,“调节溶液pH”的过程中除添加试剂,还需借助于___________ 测定溶液pH值。
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
(5)从滤液2中得到无水CuCl2的操作为___________ 。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| 开始沉淀pH | 5.8 | 5.8 | 2.0 | 4.0 |
| 沉淀完成pH | 7.5 | 8.3 | 3.1 | 5.4 |
(1)第一次过滤的滤渣为
(2)加H2O2后发生反应的离子方程式为
(3)调节溶液pH需要控制的范围是
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
| A.氢氧化钠 | B.氨水 | C.CuO | D.AlCl3 |
(5)从滤液2中得到无水CuCl2的操作为
您最近一年使用:0次
2019高二上·全国·专题练习
名校
解题方法
2 . 下列有关AgCl的沉淀溶解平衡的说法中,正确的是
| A.AgCl的生成和溶解不断进行,但速率相等 |
B.AgCl难溶于水,溶液中没有 和 和 |
| C.升高温度,AgCl的溶解度不变 |
| D.向AgCl的沉淀溶解平衡体系中加入NaCl固体,AgCl溶解的量不变 |
您最近一年使用:0次
2024-02-08更新
|
90次组卷
|
14卷引用:四川省宜宾市叙州区第一中学校2023-2024学年高二上学期1月期末化学试题
四川省宜宾市叙州区第一中学校2023-2024学年高二上学期1月期末化学试题(已下线)2019年11月11日《每日一题》人教版(选修4)—— 沉淀溶解平衡的理解福建省莆田第十五中学2018-2019学年高二下学期期中测试化学试题(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)第四节 沉淀溶解平衡 第1课时 难溶电解质的沉淀溶解平衡天津市河北区2022-2023学年高二上学期期末考试化学试题黑龙江省哈尔滨市德强学校2022-2023学年高二上学期期末考试化学试题内蒙古呼伦贝尔市满洲里市第一中学2022-2023学年高二下学期第一次月考化学试题(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)3.4.1沉淀溶解平衡原理 课前(已下线)专题07 沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(天津专用)安徽省阜阳市临泉第一中学(高铁分校)2023-2024学年高二上学期期末考试化学试题黑龙江省海林市朝鲜族中学2023-2024学年高二上学期第二次月考化学试题天津北京师范大学静海附属学校2023-2024学年高二上学期第三次月考化学试题
名校
解题方法
3 . ZnO有优异的常温发光性能,在半导体领域的液晶显示器、薄膜晶体管、发光二极管等产品中均有应用。工业上利用锌焙砂(主要成分为ZnO、ZnFe2O4,还含有Fe3O4、Al2O3、SiO2等)制取氧化锌的工艺流程如图所示:
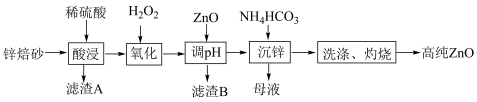
已知:相关金属离子c(Mn+)=0.1mol·L-1生成氢氧化物沉淀的pH如下表所示:
回答下列问题:
(1)“酸浸”时为了提高浸取速率,可以采取的措施是________ (任写一种)。
(2)“氧化”步骤中发生的离子方程式为________ ,H2O2的实际用量比理论用量要大,原因是___________ 。
(3)滤渣B的主要成分为________ ;加ZnO时,为了不生成Zn(OH)2,该步骤需要控制溶液pH的范围是_______ 。
(4)“沉锌”反应中,往滤液加入NH4HCO3溶液,生成ZnCO3·Zn(OH)2及CO2,写出相应的离子方程式_______ 。“沉锌”后的母液可进一步处理,获得一种化工原料,写出该原料在生产中的一种用途________ 。

已知:相关金属离子c(Mn+)=0.1mol·L-1生成氢氧化物沉淀的pH如下表所示:
| Fe2+ | Fe3+ | Al3+ | Zn2+ | |
| 开始沉淀 | 6.5 | 2.7 | 3.4 | 6.5 |
| 沉淀完全 | 9.7 | 3.7 | 4.7 | 8.5 |
(1)“酸浸”时为了提高浸取速率,可以采取的措施是
(2)“氧化”步骤中发生的离子方程式为
(3)滤渣B的主要成分为
(4)“沉锌”反应中,往滤液加入NH4HCO3溶液,生成ZnCO3·Zn(OH)2及CO2,写出相应的离子方程式
您最近一年使用:0次
4 . 工业领域常利用生成沉淀来分离或除去某些离子。可除去工业废水中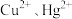 的沉淀剂是
的沉淀剂是
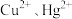 的沉淀剂是
的沉淀剂是A. | B. | C. | D. |
您最近一年使用:0次
名校
5 . 化学中常用图象直观地描述化学反应的进程或结果。下列图像描述正确的是


A.根据图①可判断可逆反应A2(g)+3B2(g) 2AB3(g)的 2AB3(g)的 >0 >0 |
B.图②表示压强对2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
| C.图③表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D.根据图④,相同温度下Ksp[Fe(OH)3]一定小于Ksp[Cu(OH)2] |
您最近一年使用:0次
名校
6 . 已知K、Ka、Kb、Kw、Kh、Ksp分别表示化学平衡常数、弱酸的电离平衡常数、弱碱的电离平衡常数、水的离子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。下列说法正确的是
| A.化学平衡常数K的大小与温度、浓度、压强有关,与催化剂无关 |
| B.K、Ka、Kb、Kw、Kh、Ksp都与温度有关,温度越高,常数值越大 |
| C.相同温度下,在等体积、等物质的量浓度的NaCl溶液和BaCl2溶液中,AgCl的溶度积Ksp相同 |
D. 的电离常数和水解常数关系: 的电离常数和水解常数关系: |
您最近一年使用:0次
7 . 如图所示进行实验,下列分析错误的是


| A.②中黄色沉淀变成黑色沉淀 |
| B.该实验可以说明溶度积Ksp(AgI)>Ksp(Ag2S) |
| C.反应后的溶液中c(Ag+):①<② |
| D.②中反应为:2AgI(s)+S2−(aq)⇌Ag2S(s)+2I−(aq) |
您最近一年使用:0次
名校
8 . 某温度下,向10mL0.1mol·L−1Pb(NO3)2溶液中滴加0.1mol·L−1Na2S溶液,溶液中-lgc(Pb2+)与滴加的Na2S溶液体积V的关系如图所示(忽略体积变化)。已知:Ksp(PbS)<Ksp(FeS)。下列判断正确的是


| A.a、b、c三点中Ksp(PbS)从大到小的顺序为:a>b>c |
| B.b点:c(Pb2+)<c(S2−) |
| C.c点:2c(Pb2+)+c(H+)=c(NO3−)+c(OH−) |
| D.其他条件相同时,若将Pb(NO3)2溶液换成同浓度、同体积的Fe(NO3)2溶液,图中-lgc(Pb2+)换成-lgc(Fe2+),则b点会沿虚线向下移动 |
您最近一年使用:0次
2024-01-18更新
|
266次组卷
|
3卷引用:四川省成都市蓉城名校2023-2024学年高二上学期期末联考化学试题
四川省成都市蓉城名校2023-2024学年高二上学期期末联考化学试题江西省宜春市宜丰中学2023-2024学年高三上学期1月月考化学试题(已下线)专题07 水溶液中的离子反应与平衡-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
9 . 常温下,向 和
和 的混合液中滴加
的混合液中滴加 溶液,
溶液, 与
与 的关系如图所示。知:
的关系如图所示。知: 代表
代表 或
或 ;
; ;当被沉淀的离子的物质的量浓度小于
;当被沉淀的离子的物质的量浓度小于 时,认为该离子已沉淀完全。下列叙述错误的是
时,认为该离子已沉淀完全。下列叙述错误的是
 和
和 的混合液中滴加
的混合液中滴加 溶液,
溶液, 与
与 的关系如图所示。知:
的关系如图所示。知: 代表
代表 或
或 ;
; ;当被沉淀的离子的物质的量浓度小于
;当被沉淀的离子的物质的量浓度小于 时,认为该离子已沉淀完全。下列叙述错误的是
时,认为该离子已沉淀完全。下列叙述错误的是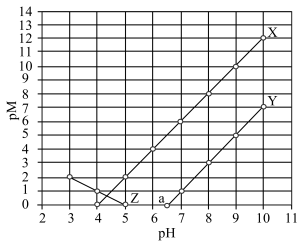
A.X、Z分别代表 与 与 的关系 的关系 |
B.常温下,弱酸 的电离常数 的电离常数 |
C.图中 点对应溶液的 点对应溶液的 为6.5,此时溶液中 为6.5,此时溶液中 |
D.向浓度均为 的 的 和 和 的混合溶液中逐滴加入 的混合溶液中逐滴加入 溶液,能通过沉淀的方式将两种离子分离 溶液,能通过沉淀的方式将两种离子分离 |
您最近一年使用:0次
名校
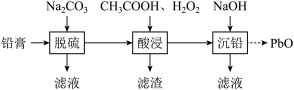
10 . 废旧铅蓄电池的铅膏中主要含有 、
、 。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法
。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法不正确 的是(已知常温下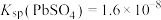 ,
,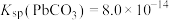 )
)
 、
、 。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法
。为了保护环境、充分利用铅资源,通过如图流程实现铅的回收。下列说法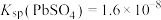 ,
,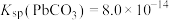 )
)
A.“铅膏”中 主要来源于该电池的正极材料 主要来源于该电池的正极材料 |
B.“脱硫”利用了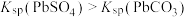 |
C.“酸浸”后溶液中的主要阳离子为 和 和 |
D.“沉铅”后的滤液中存在: |
您最近一年使用:0次
2023-12-13更新
|
177次组卷
|
2卷引用:四川省成都市第七中学2023-2024学年高一上学期12月月考化学试题



