1 . 为研究用 溶液将混合溶液中的
溶液将混合溶液中的 和
和 沉淀分离,绘制了25℃时AgCl和
沉淀分离,绘制了25℃时AgCl和 两种难溶化合物的溶解平衡曲线。其中,
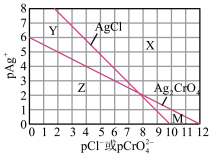
两种难溶化合物的溶解平衡曲线。其中, ,其余离子类推。两条相交的溶解平衡曲线把图像分成了X、Y、Z、M四个区域。下列说法中不正确的是
,其余离子类推。两条相交的溶解平衡曲线把图像分成了X、Y、Z、M四个区域。下列说法中不正确的是
 溶液将混合溶液中的
溶液将混合溶液中的 和
和 沉淀分离,绘制了25℃时AgCl和
沉淀分离,绘制了25℃时AgCl和 两种难溶化合物的溶解平衡曲线。其中,
两种难溶化合物的溶解平衡曲线。其中, ,其余离子类推。两条相交的溶解平衡曲线把图像分成了X、Y、Z、M四个区域。下列说法中不正确的是
,其余离子类推。两条相交的溶解平衡曲线把图像分成了X、Y、Z、M四个区域。下列说法中不正确的是
A.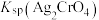 约为 约为 , ,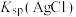 的数量级为 的数量级为 |
B.M区域内可析出 沉淀,而不析出AgCl沉淀 沉淀,而不析出AgCl沉淀 |
C.向 、 、 均为0.1mol/L的混合溶液中逐滴加入稀硝酸银溶液,先析出AgCl沉淀 均为0.1mol/L的混合溶液中逐滴加入稀硝酸银溶液,先析出AgCl沉淀 |
D.向 、AgCl混合固体和水的溶解平衡体系中加少量水, 、AgCl混合固体和水的溶解平衡体系中加少量水, 增大 增大 |
您最近一年使用:0次
2023-01-13更新
|
499次组卷
|
11卷引用:山西省临汾市2020届高考考前适应性训练考试(一)理综化学试题
山西省临汾市2020届高考考前适应性训练考试(一)理综化学试题云南省昆明市第一中学2019-2020高三第三次双基检测化学试题2020届高三《新题速递·化学》12月第02期(考点07-11)2020届高三化学化学二轮复习——常考题型:沉淀溶解平衡的曲线分析【精编25题】广东省韶关市2020届高三下学期线上教学摸底自测化学试题黑龙江省大庆铁人、鸡西一中、鹤岗一中三校2021届高三上学期联考化学试题(已下线)第26讲 难溶电解质的溶解平衡(精练)-2022年高考化学一轮复习讲练测广东省深圳市福田区福田中学2022-2023学年高三上学期第三次考试化学试题(已下线)第6讲 沉淀溶解平衡图像分析黑龙江省大庆市大庆中学2022-2023学年高三第二次模拟考试化学试题浙江省余姚中学2022-2023学年高二下学期期中考试 化学试题
2 . 25℃时,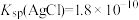 ,
,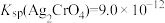 ,下列说法正确的是
,下列说法正确的是
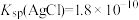 ,
,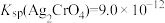 ,下列说法正确的是
,下列说法正确的是A.AgCl和 共存的悬浊液中, 共存的悬浊液中,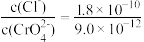 |
B.向 悬浊液中加入NaCl浓溶液, 悬浊液中加入NaCl浓溶液, 不可能转化为AgCl 不可能转化为AgCl |
C.向AgCl饱和溶液中加入NaCl固体,有AgCl析出且溶液中 |
D.向浓度均为0.1mol/L的 和NaCl混合溶液中滴加 和NaCl混合溶液中滴加 溶液,AgCl先析出 溶液,AgCl先析出 |
您最近一年使用:0次
2021-08-07更新
|
504次组卷
|
11卷引用:山西省太原市2018届高三上学期期末考试化学试题
山西省太原市2018届高三上学期期末考试化学试题福建省莆田第六中学2020届高三上学期期中考试化学试题福建省三明第一中学2020届高三上学期第二次月考化学试题2020届高三化学一轮复习 溶度积常数及溶解平衡常数的分析河北省石家庄市辛集市第一中学2019-2020学年高二第二次考试(二)化学试题课选择性必修1 专题3 第四单元 课时2 Ksp相关计算及其图像分析(已下线)第三章第四节 难溶电解的溶解平衡(备作业)-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)(已下线)第3章 水溶液中的离子反应与平衡(章末检测)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)湖南省株洲市攸县第二中学2022-2023学年高二上学期期中考试化学试题湖南省隆回县第二中学2022-2023学年高二上学期线上课程摸底(期中)考试化学试题3.4.2沉淀溶解平衡原理的应用 课后
3 . 某温度时硫酸盐MSO4(M:Pb2+、Ba2+、Sr2+)的沉淀溶解平衡曲线如图所示。已知p(M)=-lgc(M),p(SO42-)=-lgc(SO42-)。下列说法正确的是


| A.向BaSO4悬浊液中加入浓度较大的Pb(NO3)2溶液可能转化成PbSO4 |
| B.X、Y两点对应的SrSO4均是饱和溶液,不能继续溶解SrSO4 |
| C.蒸发Z点的BaSO4溶液可得到C点状态的BaSO4溶液 |
| D.溶度积:Ksp(SrSO4)<Ksp(PbSO4)<Ksp(BaSO4) |
您最近一年使用:0次
2020-07-09更新
|
569次组卷
|
5卷引用:山东省邹城市第一中学2020届高三下学期第5次模拟考试化学试题
山东省邹城市第一中学2020届高三下学期第5次模拟考试化学试题山西省太原市希望双语学校2021届高三5月押题预测卷化学试题山东省青岛第二中学2020-2021学年高三上学期期中考试化学试题(已下线)第26讲 难溶电解质的溶解平衡(精练)-2022年高考化学一轮复习讲练测(已下线)考向27 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点微专题
名校
解题方法
4 . 已知25° C时,二元酸H2X的电离平衡常数K1=5.0×10-2,K2=5.4×10-5。此温度下用AgNO3溶液分别滴定浓度均为0.01mol·L-1的KY和K2X溶液,所得的沉淀(AgY和Ag2X)溶解平衡图像如图所示。下列叙述正确的是


| A.25°C时,KHX的溶液pH>7 |
| B.反应Ag2X+2Y- ⇌2AgY+ X2-的平衡常数为103.29 |
| C.a点既可以表示AgY的不饱和溶液也可以表示Ag2X的过饱和溶液 |
| D.向c(Y-)=c(X2-)=0.01 mol·L-1的混合液中滴入AgNO3溶液时,先生成AgY沉淀 |
您最近一年使用:0次
2020-05-31更新
|
357次组卷
|
2卷引用:山西省2020届高考考前适应性测试(二)A卷理综化学试题
解题方法
5 . 某研究性学习小组为研究水垢的生成,查得CaCO3和Mg(OH)2溶解度曲线如图所示。已知:40°C时,Ksp(MgCO3)=7×10-6,下列有关分析错误的是( )
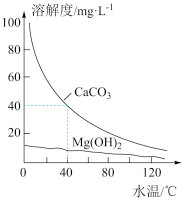

| A.CaCO3、Mg(OH)2溶解均放热 |
| B.MgCl2溶液中加入少量CaCO3粉末加热搅拌,有Mg(OH)2生成 |
| C.含有Ca(HCO3)2和Mg(HCO3)2的自来水长时间加热,水垢的主要成分为CaCO3和MgCO3 |
| D.40℃时,Ksp(CaCO3)=1.6×10-7 |
您最近一年使用:0次
名校
6 . 在25℃和100℃两种温度下,碳酸钙(CaCO3)在水中的溶解平衡曲线如图所示:下列有关说法正确的是( )
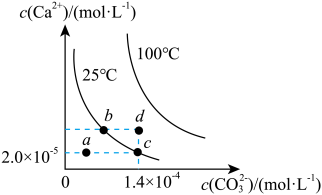

A.CaCO3(s) Ca2+(aq)+CO32-(aq) ΔH<0 Ca2+(aq)+CO32-(aq) ΔH<0 |
| B.a、b、c、d四点对应的溶度积Ksp相等 |
| C.25℃时,水分挥发,可使溶液由a点移动到c点 |
| D.25℃,Ksp(CaCO3)=2.8×10-9 |
您最近一年使用:0次
2019-12-04更新
|
300次组卷
|
3卷引用:山西省晋中市平遥县和诚中学2020届高三上学期12月月考化学试题
山西省晋中市平遥县和诚中学2020届高三上学期12月月考化学试题吉林省长春市第六中学2019-2020学年高二上学期第二段考化学试题(已下线)3.4.1 沉淀溶解平衡原理(重点练)-2020-2021学年高二化学十分钟同步课堂专练(苏教版选修4)
7 . 某温度下, (s)分别在溶液中达到沉淀溶解平衡后,改变溶液
(s)分别在溶液中达到沉淀溶解平衡后,改变溶液 ,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
 (s)分别在溶液中达到沉淀溶解平衡后,改变溶液
(s)分别在溶液中达到沉淀溶解平衡后,改变溶液 ,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是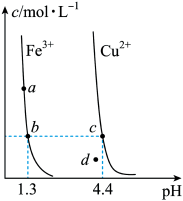
A.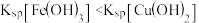 |
B.加适量 固体可使溶液由 固体可使溶液由 点变到 点变到 点 点 |
C. 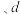 两点代表的溶液中 两点代表的溶液中 与 与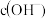 乘积相等 乘积相等 |
D. 、 、 分别在 分别在 、 、 两点代表的溶液中达到饱和 两点代表的溶液中达到饱和 |
您最近一年使用:0次
2019-01-30更新
|
1529次组卷
|
53卷引用:2010年普通高等学校招生全国统一考试理综化学部分(山东卷)
2010年普通高等学校招生全国统一考试理综化学部分(山东卷)(已下线)2011届广东省高三全真高考模拟试卷(一)(理综)化学部分2015-2016学年山西重点中学协作体高二下学期期末化学试卷2018版化学(苏教版)高考总复习专题八对接高考精练--难溶电解质的沉淀溶解平衡河北省故城县高级中学2018届高三12月月考化学试题云南省保山市2018届高三毕业复习统一检测(一) 高三理综化学部分贵州省铜仁第一中学2020届高三上学期第二次月考化学试题山西省朔州市怀仁一中2018-2019学年高二上学期第五次月考化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——溶度积常数及相关计算(强化练习)山西省大同市2022届高三上学期学情调研测试化学试题2010年高考化学试题分项专题十 电解质溶液(已下线)2010年湖北省孝感高中高二上学期期中考试化学试卷(已下线)2010-2011年福建省福州八中高二下学期期末考试化学试卷(已下线)2011-2012学年河北省元氏一中高二上学期期中考试化学试卷(已下线)2012-2013学年陕西省西安市第一中学高二上学期期末考试理科化学卷2015-2016学年广东深圳高级中学高二上期中考试化学试卷2015-2016学年黑龙江省双鸭山一中高二上期末化学试卷2015-2016学年甘肃省兰州一中高二上学期期末化学试卷2015-2016学年山东省淄博六中高二上学期期末化学试卷2015-2016学年内蒙古鄂尔多斯一中高一下期末化学试卷2016-2017学年广西柳州铁路一中高二上段考理化学卷宁夏育才中学勤行校区2017-2018学年高二12月月考化学试题河南省林州市第一中学2017-2018学年高二(火箭班)上学期期末考试化学试题江西省南昌市第二中学2017-2018学年高二上学期期末考试化学试题湖北省公安县车胤中学2017-2018学年高二3月月考化学试题2018-2019学年鲁科版高中化学选修四:模块综合检测题(二)高二人教版选修4 第三章 章末知识测评(三)辽宁省普兰店市第一中学2018-2019学年高二(理)上学期期中考试化学试题甘肃省兰州市第五十八中学2018-2019学年高二(理科)第一学期期末考试化学试题【校级联考】安徽省宿州市十三所重点中学2018-2019学年高二(理科)第一学期期末质量检测化学试题【全国百强校】安徽省黄山市屯溪第一中学2018-2019学年高二下学期入学摸底考试化学试题湖北省荆门龙泉中学2018-2019学年高二下学期期中考试化学试题贵州省龙里中学2019-2020学年高二上学期期末考试化学试题鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡江西省吉安市省重点中学2020-2021学年高二上学期期中联合考试化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 易错疑难集训(二)人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期第三次月考化学试题陕西省富平县蓝光中学2021-2022学年高三上学期期末教学检测化学试题选择性必修1 专题3 第四单元综合训练江西省吉安市2020-2021学年高二上学期期中统考化学试题广东省梅州市三校(蕉岭中学、虎山中学、平远中学)2021-2022学年高二上学期(11月)联考化学试题(已下线)3.4.1 难溶电解质的沉淀溶解平衡(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)第三章水溶液中的离子反应与平衡吉林省乾安县第七中学2021-2022学年高二上学期第三次质量检测化学试题天津市第四十二中学2022-2023学年高二上学期末考试化学试题陕西省西安市第八十九中学2022-2023学年高二上学期期末测试化学试题四川省宜宾市叙州区第一中学校2022-2023学年高二下学期开学考试化学试题新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二上学期第三次月考化学试卷四川省广安市华蓥中学2023-2024学年高二上学期12月月考化学试题重庆市巫溪县中学校2023-2024学年高二上学期第三次月考化学试题海南省琼海市嘉积中学2023-2024学年高二上学期末考试化学试题B卷内蒙古呼伦贝尔市满洲里远方中学2023-2024学年高二上学期期末考试化学试题
14-15高三上·河南郑州·阶段练习
名校
8 . ①已知t ℃时AgCl的Ksp=2.0×10-10;②在t ℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
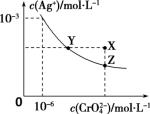

| A.在t ℃时,Ag2CrO4的Ksp为1.0×10-12 |
| B.在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点 |
| C.在t ℃时,以0.01 mol·L-1AgNO3溶液滴定20.00 mL 0.01 mol·L-1KCl和0.01 mol·L-1K2CrO4的混合溶液,CrO42-后沉淀 |
D.在t ℃时,反应Ag2CrO4(s)+2Cl-(aq) 2AgCl(s)+CrO 2AgCl(s)+CrO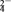 (aq)的平衡常数K=2.5×107 (aq)的平衡常数K=2.5×107 |
您最近一年使用:0次
2019-01-20更新
|
470次组卷
|
5卷引用:【全国百强校】山西省太原市第五中学2019届高三上学期12月阶段检测理科综合化学试题
9 . 硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如下图),下列说法错误的是


| A.碱式硫酸铁水解能产生Fe(OH)3胶体,可用做净水剂 |
| B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行,该反应的离子方程式为:Fe2++2HCO3-= FeCO3+ CO2↑+H2O |
| C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化 |
| D.该温度下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大 |
您最近一年使用:0次
2018-12-29更新
|
406次组卷
|
2卷引用:山西省大同市第一中学2020届高三3月月考理综化学试题
名校
10 . 下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | 酸的强弱:HX<HY |
| B | 向2 mL 0.1 mol/L Na2S溶液中滴2滴0.1 mol/L ZnSO4溶液;再滴2滴0.1 mol/L CuSO4 | 先生成白色沉淀,后生成黑色沉淀 | 溶度积(Ksp):ZnS>CuS |
| C | 向FeCl3和KSCN混合溶液中,加入少量KCl的固体 | 溶液颜色变浅 | FeCl3+3KSCN Fe(SCN)3 +3KCl平衡向逆反应方向移动 Fe(SCN)3 +3KCl平衡向逆反应方向移动 |
| D | 常温下,用pH计分别测定饱和NaA溶液和饱和NaB溶液的pH | pH:NaA>NaB | 常温下酸性:HA﹤HB |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-08-30更新
|
1267次组卷
|
11卷引用:山西省实验中学2019届高三上学期第五次月考化学试题
山西省实验中学2019届高三上学期第五次月考化学试题四川省成都市第七中学(高新校区)2018届高三理科综合化学试题(八)四川省宜宾县第一中学2019届高三上学期第一次月考理综化学试题河北省实验中学2021届高三上学期第一次月考化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二(理)上学期期中考试化学试题【全国百强校】湖南省衡阳市第八中学2018-2019学年高二上学期六科联赛试题(12月)化学试题新疆维吾尔自治区第二师华山中学2018-2019学年高二上学期期中考试化学试题【全国百强校】四川省成都市石室中学2018-2019学年高二上学期期中考试化学试题湖北省随州一中2019-2020学年高二上学期期中考试化学试题浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(实验班)化学试题浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(平行班)化学试题



