名校
解题方法
1 . 下列有关实验操作、实验现象和所得结论均正确的是
| 实验操作 | 实验现象 | 结论 | |
| A | 向某溶液中加入硝酸酸化的硝酸钡溶液 | 产生白色沉淀 | 原溶液一定含 |
| B | 向某溶液中滴加几滴新制氯水,再滴加硫氰化钾溶液 | 试管中溶液变红 | 原溶液中一定含有Fe2+ |
| C | 室温下用pH计分别测定 、NaHSO3溶液的pH 、NaHSO3溶液的pH | Na2SO3的pH大于NaHSO3溶液的pH |  结合H+的能力比 结合H+的能力比 的强 的强 |
| D | 向相同物质的量浓度的MgSO4、CuSO4混合溶液中滴入少量NaOH稀溶液 | 有蓝色沉淀产生 | 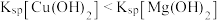 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 下列有关实验操作和现象及所得出的结论均正确的是
实验操作 | 现象 | 结论 | |
A | 向某有机物中先滴加NaOH水溶液,加热,再加入AgNO3溶液 | 有白色沉淀生成 | 一定含有氯原子 |
B | 向4mL0.01mol/酸性KMnO4溶液中加入2mL0.1mol/LH2C2O4溶液 | 产生气泡的速率先增大后减小 | 该反应一定为放热反应 |
C | 向发黄的浓硝酸中通入O2 | 黄色褪去 | 浓硝酸中混有Fe3+ |
D | 向均为0.1mol·L-1的MgCl2、CuCl2混合溶液中逐滴加入少量氨水 | 先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 下列装置或操作能达到相应实验目的的是
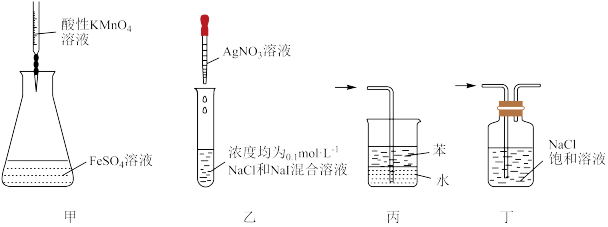

| A.装置甲可用酸性KMnO4溶液滴定FeSO4溶液 |
| B.装置乙进行实验时若逐滴滴加AgNO3溶液,先出现黄色沉淀,可说明Ksp(AgCl)>Ksp(AgI),且AgCl可转化成AgI |
| C.装置丙可用于吸收氨气,且能防止倒吸 |
| D.装置丁可除去氯气中的HCl |
您最近一年使用:0次
名校
4 . 下列实验中,根据实验操作和现象得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向 与稀硫酸反应的溶液中滴加少量 与稀硫酸反应的溶液中滴加少量 溶液 溶液 | 气泡产生速率加快 |  有催化作用 有催化作用 |
| B | 将湿润的淀粉KI试纸放入含有红棕色气体的集气瓶中 | 试纸变蓝 | 该气体为 ,具有氧化性 ,具有氧化性 |
| C |  白色悬浊液中滴入几滴 白色悬浊液中滴入几滴 稀溶液 稀溶液 | 出现黑色沉淀 | 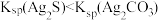 |
| D | 将稀硫酸酸化后的 溶液滴入 溶液滴入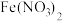 溶液中 溶液中 | 溶液由浅绿色变为黄色 | 氧化性: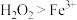 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-04-09更新
|
748次组卷
|
3卷引用:辽宁省锦州市2021届高考第一次模拟(普通高中高三质量检测)化学试题
5 . 铅及其化合物用途广泛,请回答下列相关问题:
(1)铅元素(82Pb)位于周期表中第_______ 周期,基态价电子排布式为_______ 。相同温度下,同浓度的Na2PbO3溶液碱性比Na2CO3溶液碱性_______ (填“强”或“弱”)。
(2)工业上利用铅浮渣(主要成分是PbO2、Pb,含有少量Ag、CaO和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示:
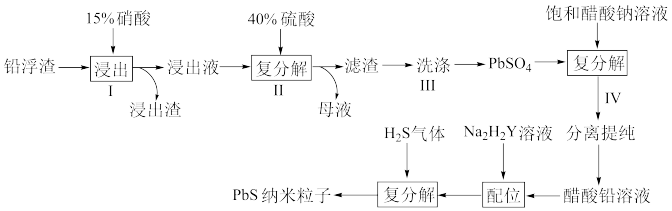
已知:25℃时,Ksp(CaSO4)=4.9×10−5,Ksp(PbSO4)=1.6×10−8,Ksp(PbS)=1.0×10−28。
①已知步骤Ⅰ有NO产生,Pb被稀硝酸氧化成Pb2+。写出Pb参加反应的离子方程式:_______ 。
②步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有_______ 。
③步骤Ⅲ需用Pb(NO3)2溶液多次洗涤硫酸铅的原因是_______ 。
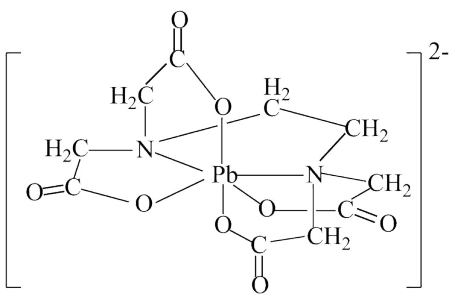
④EDTA二钠简写成Na2H2Y,可以与Pb2+形成稳定的配离子,其结构如图,此配离子内所含作用力除σ键外,还有_______ 。
⑤PbS晶胞与NaCl晶胞相同,则S2−的配位数是_______ 。
(1)铅元素(82Pb)位于周期表中第
(2)工业上利用铅浮渣(主要成分是PbO2、Pb,含有少量Ag、CaO和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示:

已知:25℃时,Ksp(CaSO4)=4.9×10−5,Ksp(PbSO4)=1.6×10−8,Ksp(PbS)=1.0×10−28。
①已知步骤Ⅰ有NO产生,Pb被稀硝酸氧化成Pb2+。写出Pb参加反应的离子方程式:
②步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,浸出渣的成分除了不溶于硝酸的杂质和铅外,还主要有
③步骤Ⅲ需用Pb(NO3)2溶液多次洗涤硫酸铅的原因是
④EDTA二钠简写成Na2H2Y,可以与Pb2+形成稳定的配离子,其结构如图,此配离子内所含作用力除σ键外,还有

⑤PbS晶胞与NaCl晶胞相同,则S2−的配位数是
您最近一年使用:0次
解题方法
6 . 从下列事实所得出的相应结论正确的是
| 实验事实 | 结论 | |
| A | 在相同温度下,向1 mL0.2 mol/LNaOH溶液中滴入2滴0.1 mol/LMgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol/LFeCl3溶液,又生成红褐色沉淀 | 溶解度:Mg(OH)2>Fe(OH)3 |
| B | 某气体能使湿润的蓝色石蕊试纸变红 | 该气体水溶液一定显碱性 |
| C | 同温同压下,等体积pH=3的HA和HB两种酸分别于足量的锌反应,排水法收集气体,HA放出的氢气多且反应速率快 | HB的酸性比HA强 |
| D | SiO2既能与氢氟酸反应又能与碱反应 | SiO2是两性氧化物 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-03-30更新
|
455次组卷
|
2卷引用:辽宁省丹东市2020年高三线上教学质量监测(全国II卷)理综化学试题
7 . 根据下列实验操作所得结论正确的是( )
| 选项 | 实验操作 | 实验结论 |
| A | 向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL5%H2O2溶液 | 浓度越大,反应速率越快 |
| B | 向40mL的沸水中滴入5~6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。当光束通过液体时,可观察到丁达尔效应 | 得到Fe(OH)3胶体 |
| C | 向NaCl、NaI的混合稀溶液中滴入浓AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl)>Ksp(AgI) |
| D | 同温下用pH试纸分别测定浓度为0.1mol/L NaClO溶液、0.1mol/LCH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-02-25更新
|
320次组卷
|
3卷引用:辽宁省大连市2020届高三双基测试化学试题
名校
8 . 关于下列各图的叙述,正确的是
A. 向 向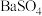 饱和溶液中加入硫酸钠固体 饱和溶液中加入硫酸钠固体 |
B.  与 与 发生反应过程中的能量变化,则 发生反应过程中的能量变化,则 的燃烧热为483.6kJ·mol 的燃烧热为483.6kJ·mol |
C. 25℃时,用0.1 25℃时,用0.1 盐酸滴定20mL0.1 盐酸滴定20mL0.1 氨水,溶液的pH随加入盐酸体积的变化 氨水,溶液的pH随加入盐酸体积的变化 |
D. 表示一定条件下进行的反应 表示一定条件下进行的反应  各成分的物质的量变化, 各成分的物质的量变化,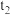 时刻改变的条件可能是降低温度有时间 时刻改变的条件可能是降低温度有时间 |
您最近一年使用:0次
9 . 下列实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 分离Fe2O3、Al2O3 | 将混合物投入足量NaOH溶液中然后依次进行过滤、洗涤、蒸发、灼烧四项操作 |
| B | 验证淀粉溶液水解生成葡萄糖 | 向淀粉溶液中加入稀硫酸共热,冷却后再加入新制Cu(OH)2悬浊液,加热 |
| C | 证明:Ksp(Ag2CrO4)<Ksp(AgCl) | 向浓度均为0.1mol/L的KC1和K2CrO4的混合溶液中逐滴加入AgNO3溶液 |
| D | 检验FeCl2晶体是否完全变质 | 取少量久置的FeCl2晶体于试管中,逐滴加入酸性高锰酸钾溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 下列实验操作、现象和结论均正确的是
| 实验操作 | 现象 | 结论 | |
| A | 将少量的饱和硼酸溶液滴加到碳酸钠溶液中 | 无气泡 | Ka2H2CO3>H3BO3 |
| B | 向蔗糖溶液中加入稀硫酸并水浴加热,一段时间后再向混合液中加入新制备的Cu(OH)2悬浊液并加热 | 无红色沉淀 | 蔗糖未水解 |
| C | 将浸透了石蜡油的石棉放置在硬质试管底部,加入少量碎瓷片,并加强热,将生成的气体通入酸性高锰酸钾溶液 | 溶液褪色 | 石蜡油分解产物中含有不饱和烃 |
| D | 向1mL2mol/L的NaOH溶液中,滴加1-2滴1mol/ L MgCl2溶液,再滴加2滴1mol/ L FeCl3溶液 | 先有白色沉淀,后有红褐色沉淀 | Ksp:Mg(OH)2>Fe(OH)3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



