1 . 市售一次性保暖贴的主要成分为:铁粉、水、食盐、活性炭、蛭石、吸水性树脂。下列叙述错误的是
| A.保暖贴使用前要密封保存,使之与空气隔绝 |
| B.使用时以电池反应的形式加快了铁与氧气的放热反应 |
| C.活性炭为正极材料,食盐溶于水成为离子导体 |
D.使用后袋内深褐色物质的主要成分是 |
您最近一年使用:0次
2 . 某课外活动小组用如图装置进行实验,试回答下列问题:
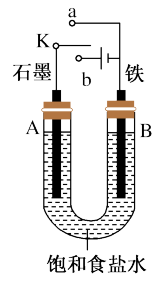
(1)若开始时开关K与a连接,B极的Fe发生_______ 腐蚀(填“析氢”或“吸氧”)。
(2)若开始时开关K与b连接,下列说法正确的是_______ (填序号)。
① 溶液中Na+向A极移动
② 从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③ 反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④ 若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

① 该电解槽的阳极反应式为_______ ,此时通过阴离子交换膜的离子数_______ (填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
② 制得的氢氧化钾溶液从出口_______ (填“A”“B”“C”或“D”)导出。
(4)用惰性电极电解体积为1L的CuSO4溶液,当阴阳极都产生3.36L(标况)气体时,请问硫酸铜的浓度为_______ ,若要此溶液恢复到原状态需要加入_______ (填选项)。
ACuSO4 BCuO CCu(OH)2 DCu2(OH)2CO3

(1)若开始时开关K与a连接,B极的Fe发生
(2)若开始时开关K与b连接,下列说法正确的是
① 溶液中Na+向A极移动
② 从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③ 反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④ 若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

① 该电解槽的阳极反应式为
② 制得的氢氧化钾溶液从出口
(4)用惰性电极电解体积为1L的CuSO4溶液,当阴阳极都产生3.36L(标况)气体时,请问硫酸铜的浓度为
ACuSO4 BCuO CCu(OH)2 DCu2(OH)2CO3
您最近一年使用:0次
名校
解题方法
3 . 下列生活中的现象,与盐的水解无关的是
| A.古代用草木灰的水溶液来洗涤衣物 |
| B.明矾净水 |
| C.铁在潮湿环境中生锈 |
| D.氯化铵溶液可做金属焊接中的除锈剂 |
您最近一年使用:0次
2023-01-10更新
|
145次组卷
|
3卷引用:福建省泉州市永春第一中学2022-2023学年高二上学期期末考试化学试题
福建省泉州市永春第一中学2022-2023学年高二上学期期末考试化学试题四川省内江市第六中学2023-2024学年高二上学期第二次月考化学试卷(已下线)黑龙江省牡丹江市第一高级中学2022-2023学年高三上学期期末考试变式汇编(1-10)
名校
解题方法
4 . 对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)镀铜可防止铁制品腐蚀,电镀时用铜作阳极,阳极电极方程式是:_______ 。在此过程中,两个电极上质量的变化值:阴极_______ 阳极(填“>”“<”或“=”)。
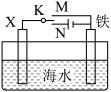
(2)利用如图所示的装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于_______ (填“M”或“N”)处。若X为锌,开关K置于M处,该电化学防护法称为_______ 。
(1)镀铜可防止铁制品腐蚀,电镀时用铜作阳极,阳极电极方程式是:
(2)利用如图所示的装置,可以模拟铁的电化学防护。若X为碳棒,为减缓铁的腐蚀,开关K应置于

您最近一年使用:0次
名校
解题方法
5 . 电化学原理在能量转换、物质合成、防止金属腐蚀等方面应用广泛。
(1)下图是常见电化学装置图
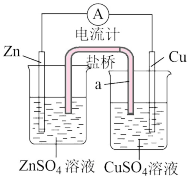
①Zn棒发生的电极反应是___________ 。
②若用一根铜丝代替盐桥插入两烧杯中,电流计指针也发生偏转,推测:其中一个为原电池,一个为电解池,写出a端发生的电极反应___________ 。
(2)下图为探究金属Fe是否腐蚀的示意图
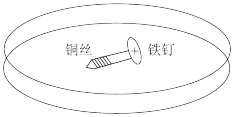
在培养皿中加入一定量的琼脂和饱和 溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为
溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为___________ 端(填“铜丝附近”或“铁丝附近”),请结合文字和方程式解释变红的原因___________ 。
(3)一种利用原电池原理治污的装置如下图,其反应原理是 。
。
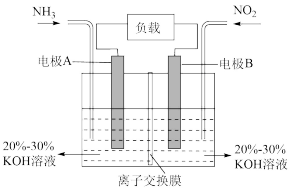
①A电极的电极反应式为___________ 。
②下列关于该电池说法正确的是___________ (填序号)。
A.电子从右侧电极经过负载后流向左侧电极
B.当有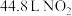 被处理时,转移电子的物质的量为
被处理时,转移电子的物质的量为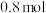
C.电池工作一段时间,溶液的pH不变
D.为使电池持续放电,离子交换膜需选用阴离子交换膜
(1)下图是常见电化学装置图

①Zn棒发生的电极反应是
②若用一根铜丝代替盐桥插入两烧杯中,电流计指针也发生偏转,推测:其中一个为原电池,一个为电解池,写出a端发生的电极反应
(2)下图为探究金属Fe是否腐蚀的示意图

在培养皿中加入一定量的琼脂和饱和
 溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为
溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为(3)一种利用原电池原理治污的装置如下图,其反应原理是
 。
。
①A电极的电极反应式为
②下列关于该电池说法正确的是
A.电子从右侧电极经过负载后流向左侧电极
B.当有
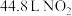 被处理时,转移电子的物质的量为
被处理时,转移电子的物质的量为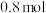
C.电池工作一段时间,溶液的pH不变
D.为使电池持续放电,离子交换膜需选用阴离子交换膜
您最近一年使用:0次
2022-12-25更新
|
349次组卷
|
2卷引用:福建省福州市福建师范大学附属中学2022-2023学年高二上学期期末考试化学试题
6 . 下列对于电化学说法正确的是
| A.为保护浸入海水中的钢闸门,可在闸门表面镶上铜锭 |
| B.电解精炼铜时,阳极泥中常含有金属金、银、锌等 |
| C.可充电电池放电时,化学能转变为电能 |
| D.镀锌铁皮的镀层损坏后,铁更容易腐蚀 |
您最近一年使用:0次
7 . 对下列图示实验的描述正确的是
| 选项 | 实验装置图 | 相关描述 |
| A | 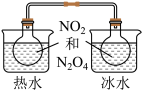 | 根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)判断 正反应是吸热反应 正反应是吸热反应 |
| B | 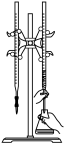 | 用已知浓度的NaOH溶液滴定锥形瓶中未知浓度的盐酸 |
| C | 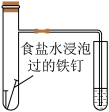 | 根据小试管中液面的变化判断铁钉发生吸氧腐蚀 |
| D | 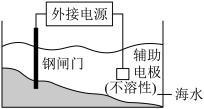 | 该保护金属的方法为牺牲阳极法 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-11更新
|
350次组卷
|
2卷引用:福建省福州第一中学2022-2023学年高二上学期期末考试化学试题
8 . 将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,液滴外沿为棕色铁锈环(b),如图所示,下列说法不正确 的是
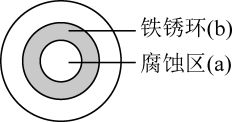

A.铁片腐蚀过程发生的总化学方程式为: 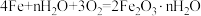 |
B.液滴之下氧气含量少,铁片作负极,发生的还原反应为: |
C.液滴边缘是正极区,发生的电极反应为: |
| D.铁片腐蚀最严重区域不是生锈最多的区域 |
您最近一年使用:0次
2022-12-11更新
|
251次组卷
|
2卷引用:福建省泉州第五中学2022-2023学年高二上学期期中考化学试题
解题方法
9 . 填空。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知①2CH4(g)+ 3O2(g) = 2 CO(g)+ 4 H2O(l) △H1 = -1214.6 kJ/mol
②2 CO(g)+ O2(g) =2 CO2(g) ΔH2 = -566 kJ/mol
则反应CH4(g)+2O2(g) = CO2(g)+2H2O(l) 的△H=_______ 。
(2)如图,水槽中试管内有一枚铁钉,放置数天观察:
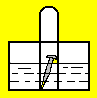
若液面上升,发生_______ 腐蚀(填“析氢”或“吸氧”),负极电极反应式:_______ ,正极电极反应式:_______
(3)将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。通入CH4的一极,其电极反应式是_______ 。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知①2CH4(g)+ 3O2(g) = 2 CO(g)+ 4 H2O(l) △H1 = -1214.6 kJ/mol
②2 CO(g)+ O2(g) =2 CO2(g) ΔH2 = -566 kJ/mol
则反应CH4(g)+2O2(g) = CO2(g)+2H2O(l) 的△H=
(2)如图,水槽中试管内有一枚铁钉,放置数天观察:

若液面上升,发生
(3)将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。通入CH4的一极,其电极反应式是
您最近一年使用:0次
解题方法
10 . 下图容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是


| A.① > ② > ③ > ⑤ > ④ | B.⑤ > ① > ③ > ② > ④ |
| C.⑤ > ① > ② > ③ > ④ | D.① > ⑤ > ③ > ④ > ② |
您最近一年使用:0次



