1 . 电化学在科技、生产、社会和生活的各个发面都发挥着重要的作用。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择_______ (填字母)。这种防止金属材料腐蚀的方法叫做_______ 。

a.金块 b .锌板 c.铜板 d.钠块
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图。(电极均为石墨电极)

①写出A装置中发生反应的离子反应方程式:_______ 。
②写出燃料电池B中的负极的电极反应:_______ ;分析比较图示中a%与b%的大小:a% _______ b%(填“>”“<”或“=”);燃料电池B中的离子交换膜为_______ 离子交换膜。
(3)通过NO传感器可监测汽车尾气中NO的含量,工作原理如图所示:
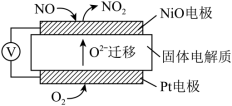
NiO电极上的电极反应式为_______ 。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择

a.金块 b .锌板 c.铜板 d.钠块
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图。(电极均为石墨电极)

①写出A装置中发生反应的离子反应方程式:
②写出燃料电池B中的负极的电极反应:
(3)通过NO传感器可监测汽车尾气中NO的含量,工作原理如图所示:

NiO电极上的电极反应式为
您最近一年使用:0次
2 . 下列关于电化学的说法不正确的是
| A.铝制品可利用阳极氧化法处理表面,使之形成致密的氧化膜而起到防护作用 |
| B.水库的钢闸门接直流电源的正极,可以减缓闸门的腐蚀 |
| C.轮船在船壳水线以下常装有一些锌块,这是利用了牺牲阳极的阴极保护法 |
| D.氯碱工业选用阳离子交换膜隔离两个电极区 |
您最近一年使用:0次
2022-11-06更新
|
417次组卷
|
4卷引用:浙江省温州十校联合体2022-2023学年高二上学期期中联考化学试题
浙江省温州十校联合体2022-2023学年高二上学期期中联考化学试题湖南省雅礼中学2022-2023学年高二上学期第三次月考化学试题(已下线)【2022】【高二上】【期中考】【温州十校】【高中化学】【李鼎收集】浙江省温州市2022-2023学年高二上学期11月期中考试化学试题
名校
解题方法
3 . 下列有关化学反应原理的说法中,不正确的说法组合是
①有效碰撞一定能导致化学反应的发生
②难溶物的溶解度和 Ksp 的大小都仅仅只受温度的影响
③某反应正方向能自发进行,则逆方向一定难以自发进行
④某溶液的 pH 不受温度的影响,那么该溶液一定显强酸性
⑤用盐酸滴定氨水,若选择酚酞做指示剂,则测定的结果会偏小
⑥中和热的测定实验,若量取 NaOH 溶液的量筒仰视读数,则所测的△H 偏大
⑦金属的吸氧腐蚀比析氢腐蚀更普遍,但吸氧腐蚀的速率不如金属的析氢腐蚀
①有效碰撞一定能导致化学反应的发生
②难溶物的溶解度和 Ksp 的大小都仅仅只受温度的影响
③某反应正方向能自发进行,则逆方向一定难以自发进行
④某溶液的 pH 不受温度的影响,那么该溶液一定显强酸性
⑤用盐酸滴定氨水,若选择酚酞做指示剂,则测定的结果会偏小
⑥中和热的测定实验,若量取 NaOH 溶液的量筒仰视读数,则所测的△H 偏大
⑦金属的吸氧腐蚀比析氢腐蚀更普遍,但吸氧腐蚀的速率不如金属的析氢腐蚀
| A.②③ | B.①③⑥ | C.①③④ | D.②③⑥ |
您最近一年使用:0次
名校
解题方法
4 . 电化学反应原理的实验装置如图所示。下列叙述错误的是
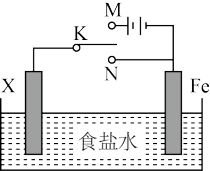

| A.若X为碳棒,开关K置于M处可减缓铁的腐蚀 |
| B.若X为锌棒,开关K置于M或N处都可减缓铁的腐蚀 |
| C.若X为锌棒,开关K置于N处时,为牺牲阳极的阴极保护法 |
| D.若X为碳棒,开关K置于N处时,X电极上发生的反应为2H+ +2e-=H2↑ |
您最近一年使用:0次
2022-09-06更新
|
918次组卷
|
16卷引用:云南省玉溪第三中学2021-2022学年高二下学期3月入学考试化学试题
云南省玉溪第三中学2021-2022学年高二下学期3月入学考试化学试题河南省濮阳市2021-2022学年高二上学期期末学业质量监测化学试题第三节 金属的腐蚀与防护云南省曲靖市马龙区第一中学2021-2022学年高二下学期3月考试化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高二上学期期末考试化学试题新疆柯坪县柯坪湖州国庆中学2021-2022学年高二3月月考化学试题(已下线)4.3 金属的腐蚀与防护-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)山东省章丘市第一中学2020-2021学年高二上学期9月月考化学试题内蒙古通辽市开鲁县第一中学2020-2021学年高二上学期期中考试化学试题河北省迁安市第一中学2020-2021学年高二上学期期中考试化学试题(已下线)4.3.2 金属(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)的防护安徽省六安市城南中学2021届高三上学期第三次月考化学试题山东省济南德润高级中学2021-2022学年高二上学期10月月考化学试题河北省保定市博野中学2021-2022学年高二上学期12月月考化学试题浙江省宁波市余姚中学2020-2021学年高二上学期期中考试化学试题河北省唐山市第二中学2022-2023学年高二上学期期末考试化学试题
5 . 用下列仪器或装置(夹持装置略)进行相应实验,能达到实验目的的是
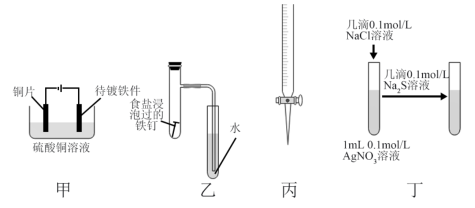

| A.甲装置:完成铁件上镀铜 |
| B.乙装置:验证铁的吸氧腐蚀 |
| C.丙装置:量取20.00mL NaOH溶液 |
D.丁装置:比较AgCl和 溶解度大小 溶解度大小 |
您最近一年使用:0次
6 . 下列实验装置或操作正确,且能达到相应实验目的的是
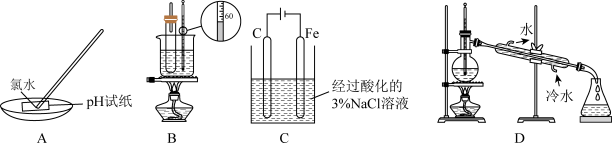

| A.图A是测定氯水的pH | B.图B是实验室制备硝基苯 |
| C.图C是用铁氰化钾溶液验证牺牲阳极法保护铁 | D.图D是分离苯和溴苯 |
您最近一年使用:0次
7 . 铁及其化合物在生活、生产中有着重要作用。请按要求回答下列问题。
(1)基态Fe原子的简化电子排布式为____ 。
(2)因生产金属铁的工艺和温度等因素不同,产生的铁单质的晶体结构、密度和性质均不同。
①用____ 实验测定铁晶体,测得A、B两种晶胞,其晶胞结构如图:
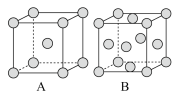
②A、B两种晶胞中含有的铁原子个数比为____ 。
③在A晶胞中,每个铁原子周围与它最近且相等距离的铁原子有____ 个。
(3)常温下,铁不易和水反应,而当撕开暖贴(内有透气的无纺布袋,袋内装有铁粉、活性炭、无机盐、水、吸水性树脂等)的密封外包装时,即可快速均匀发热。利用所学知识解释暖贴发热的原因:___ 。
(4)工业盐酸因含有[FeCl4]—而呈亮黄色,在高浓度Cl—的条件下[FeCl4]—才是稳定存在的。
①[FeCl4]—的中心离子是____ ,配体是____ ;其中的化学键称为____ 。
②取4mL工业盐酸于试管中,逐滴滴加AgNO3饱和溶液,至过量,预计观察到的现象有____ ,由此可知在高浓度Cl—的条件下[FeCl4]—才是稳定存在的。
(1)基态Fe原子的简化电子排布式为
(2)因生产金属铁的工艺和温度等因素不同,产生的铁单质的晶体结构、密度和性质均不同。
①用

②A、B两种晶胞中含有的铁原子个数比为
③在A晶胞中,每个铁原子周围与它最近且相等距离的铁原子有
(3)常温下,铁不易和水反应,而当撕开暖贴(内有透气的无纺布袋,袋内装有铁粉、活性炭、无机盐、水、吸水性树脂等)的密封外包装时,即可快速均匀发热。利用所学知识解释暖贴发热的原因:
(4)工业盐酸因含有[FeCl4]—而呈亮黄色,在高浓度Cl—的条件下[FeCl4]—才是稳定存在的。
①[FeCl4]—的中心离子是
②取4mL工业盐酸于试管中,逐滴滴加AgNO3饱和溶液,至过量,预计观察到的现象有
您最近一年使用:0次
2022-06-01更新
|
751次组卷
|
3卷引用:天津市河西区2022届高考三模化学试题
8 . 羰基硫是一种粮食熏蒸剂,能防治某些害虫和真菌的危害,利用CO等制备羰基硫原理:CO+H2S⇌COS+H2。
(1)用FeOOH作催化剂,CO(g)+H2S(g)⇌COS(g)+H2(g)的反应分两步进行,其反应过程能量变化如图1所示。
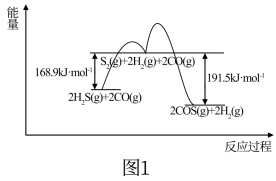
①CO(g)+H2S(g)⇌COS(g)+H2(g) △H=___________ 。
②决定COS生成速率的主要步骤是___________ (填“第1步”或“第2步”)。
(2)在2L的密闭容器中,保持温度不变,开始投入9molH2S和amolCO,经10min达到平衡,Kp=0.2(Kp为以分压表示的平衡常数),n(H2S)=5mol,则CO的平衡转化率α=___________ 。
(3)在2L的密闭容器中,开始时投入amolCO和1molH2S,图2中曲线I和II表示某温度下,CO和H2S投料比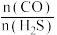 不同时,CO转化率随时间变化关系,则曲线I和II中a值的大小关系为:I
不同时,CO转化率随时间变化关系,则曲线I和II中a值的大小关系为:I___________ II(填“>”“<”或“=”),理由是___________ 。
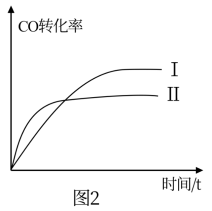
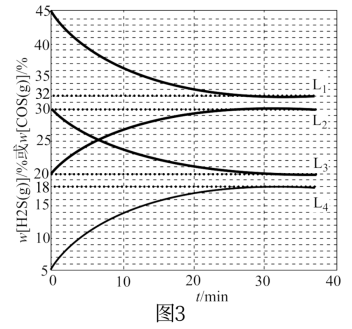
(4)已知起始密闭容器中ω[H2S(g)]和ω[CO(g)]、ω[COS(g)]和ω[H2(g)]分别相等,在240℃时该反应平衡常数K=1,在300℃、340℃时反应中H2S(g)和COS(g)的体积分数(ω)随时间(t)的变化关系如图3所示。则300℃时,ω[COS(g)]随时间变化的曲线为___________ ,340℃时,ω[H2S(g)]随时间变化的曲线为___________ 。
(5)羰基硫在水存在时会缓慢水解生成H2S,会使钢铁设备发生析氢腐蚀,则其正极的电极反应式为___________ ,负极的反应产物为___________ (填化学式)。
(1)用FeOOH作催化剂,CO(g)+H2S(g)⇌COS(g)+H2(g)的反应分两步进行,其反应过程能量变化如图1所示。

①CO(g)+H2S(g)⇌COS(g)+H2(g) △H=
②决定COS生成速率的主要步骤是
(2)在2L的密闭容器中,保持温度不变,开始投入9molH2S和amolCO,经10min达到平衡,Kp=0.2(Kp为以分压表示的平衡常数),n(H2S)=5mol,则CO的平衡转化率α=
(3)在2L的密闭容器中,开始时投入amolCO和1molH2S,图2中曲线I和II表示某温度下,CO和H2S投料比
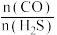 不同时,CO转化率随时间变化关系,则曲线I和II中a值的大小关系为:I
不同时,CO转化率随时间变化关系,则曲线I和II中a值的大小关系为:I
(4)已知起始密闭容器中ω[H2S(g)]和ω[CO(g)]、ω[COS(g)]和ω[H2(g)]分别相等,在240℃时该反应平衡常数K=1,在300℃、340℃时反应中H2S(g)和COS(g)的体积分数(ω)随时间(t)的变化关系如图3所示。则300℃时,ω[COS(g)]随时间变化的曲线为

(5)羰基硫在水存在时会缓慢水解生成H2S,会使钢铁设备发生析氢腐蚀,则其正极的电极反应式为
您最近一年使用:0次
名校
解题方法
9 . 某同学做如下实验,下列说法正确的是
| 装置 | 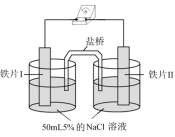 | 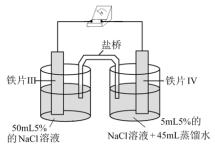 |
| 现象 | 电流计指针未发生偏转 | 电流计指针发生偏转 |
| A.“电流计指针未发生偏转”,说明铁片I、铁片II均未被腐蚀 |
| B.铁片IV的电极反应式为Fe-3e-=Fe3+ |
| C.铁片I、III所处的电解质溶液浓度相同,二者的腐蚀速率相等 |
| D.用K3[Fe(CN)6]溶液检验铁片III、IV附近溶液,可判断电池的正、负极 |
您最近一年使用:0次
2021-02-05更新
|
438次组卷
|
3卷引用:江西省师范大学附属中学2021-2022学年高二上学期期末化学试题
10 . 食品包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧过程与电化学知识相关。下列分析正确的是
| A.脱氧过程是吸热反应,可降低温度,延长食品保质期 |
| B.脱氧过程中炭作原电池正极,电极反应为:4H++O2+4e-=2H2O |
| C.含有0.56 g铁粉的脱氧剂,理论上最多能吸收氧气168 mL(标准状况) |
| D.该过程实现了电能到化学能的转化 |
您最近一年使用:0次
2020-11-18更新
|
731次组卷
|
6卷引用:江苏省丹阳高级中学2021-2022学年高二下学期期初考试化学试题
江苏省丹阳高级中学2021-2022学年高二下学期期初考试化学试题河北省张家口市第一中学2021届高三上学期期中考试(衔接班)化学试题(已下线)练习10 金属的腐蚀与防护-2020-2021学年【补习教材·寒假作业】高二化学(人教版2019)广东省广州市第六中学2022届高三第二次月考化学试题江苏省苏州市相城区陆慕高级中学2021-2022学年高二上学期第一次月考化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题1-5)



