名校
1 . 下列电极反应式与出现的环境相匹配的是
| 电极反应式 | 出现的环境 | |
| A | C2H5OH-12e-+3H2O=CO2↑+12H+ | 碱性环境下乙醇燃料电池的负极反应 |
| B | O2+2H2O-4e-=4OH- | 钢铁吸氧腐蚀的正极反应 |
| C | CO-2e-+CO =2CO2 =2CO2 | 熔融碳酸盐环境下的CO燃料电池负极 |
| D | 2H++2e-=H2↑ | 用惰性电极电解H2SO4溶液的阳极反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 电化学反应原理的实验装置如图所示。下列叙述错误的是
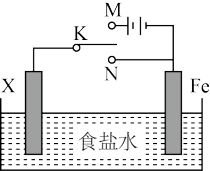

| A.若X为碳棒,开关K置于M处可减缓铁的腐蚀 |
| B.若X为锌棒,开关K置于M或N处都可减缓铁的腐蚀 |
| C.若X为锌棒,开关K置于N处时,为牺牲阳极的阴极保护法 |
| D.若X为碳棒,开关K置于N处时,X电极上发生的反应为2H+ +2e-=H2↑ |
您最近一年使用:0次
2022-09-06更新
|
918次组卷
|
16卷引用:云南省玉溪第三中学2021-2022学年高二下学期3月入学考试化学试题
云南省玉溪第三中学2021-2022学年高二下学期3月入学考试化学试题河南省濮阳市2021-2022学年高二上学期期末学业质量监测化学试题第三节 金属的腐蚀与防护云南省曲靖市马龙区第一中学2021-2022学年高二下学期3月考试化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高二上学期期末考试化学试题新疆柯坪县柯坪湖州国庆中学2021-2022学年高二3月月考化学试题(已下线)4.3 金属的腐蚀与防护-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)山东省章丘市第一中学2020-2021学年高二上学期9月月考化学试题内蒙古通辽市开鲁县第一中学2020-2021学年高二上学期期中考试化学试题河北省迁安市第一中学2020-2021学年高二上学期期中考试化学试题(已下线)4.3.2 金属(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)的防护安徽省六安市城南中学2021届高三上学期第三次月考化学试题山东省济南德润高级中学2021-2022学年高二上学期10月月考化学试题河北省保定市博野中学2021-2022学年高二上学期12月月考化学试题浙江省宁波市余姚中学2020-2021学年高二上学期期中考试化学试题河北省唐山市第二中学2022-2023学年高二上学期期末考试化学试题
3 . 实验小组研究金属电化学腐蚀,实验如下:
实验Ⅰ

5min时的现象:铁钉表面及周边未见明显变化。
25min时的现象:铁钉周边零星、随机出现极少量红色和蓝色区域,有少量红棕色铁锈生成。
实验Ⅱ
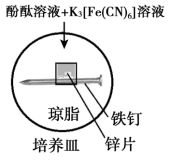
5min时的现象:铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化。
25min时的现象:铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化。
下列说法不正确的是
实验Ⅰ

5min时的现象:铁钉表面及周边未见明显变化。
25min时的现象:铁钉周边零星、随机出现极少量红色和蓝色区域,有少量红棕色铁锈生成。
实验Ⅱ

5min时的现象:铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化。
25min时的现象:铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化。
下列说法不正确的是
| A.实验Ⅱ中Zn保护了Fe,使铁的腐蚀速率比实验Ⅰ慢 |
B.实验Ⅱ中正极的电极反应式: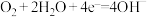 |
C.实验Ⅰ的现象说明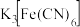 溶液与Fe反应生成了 溶液与Fe反应生成了 |
| D.若将Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色 |
您最近一年使用:0次
2022-09-04更新
|
1372次组卷
|
13卷引用:北京市第十二中学2021-2022学年高一下学期6月月考化学试题
北京市第十二中学2021-2022学年高一下学期6月月考化学试题北京十二中2021-2022学年高一下学期六月月考(等级考)化学试题(已下线)【教材实验热点】17 金属的腐蚀与防护第四章 综合拔高练北京市海淀实验中学2022-2023学年高三上学期10月学科展示化学试题北京市北京师范大学燕化附中2022-2023学年高二上学期10月月考化学试题福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(2卷)试题山东省枣庄市第一中学2022-2023学年高二上学期期末达标化学试题北京市朝阳区2021届高三上学期期末考试化学试题(已下线)2021年高考化学押题预测卷(辽宁卷)(03)(已下线)北京市第四中学2021-2022学年高二上学期期中考试化学试题福建省龙岩市连城县第一中学2023-2024学年高二上学期8月月考化学试题山东省滨州市2023-2024学年高三上学期11月期中考试化学试题
4 . 用下列仪器或装置(夹持装置略)进行相应实验,能达到实验目的的是
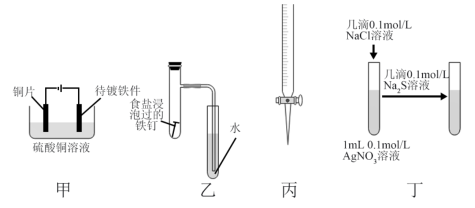

| A.甲装置:完成铁件上镀铜 |
| B.乙装置:验证铁的吸氧腐蚀 |
| C.丙装置:量取20.00mL NaOH溶液 |
D.丁装置:比较AgCl和 溶解度大小 溶解度大小 |
您最近一年使用:0次
5 . 下列实验装置或操作正确,且能达到相应实验目的的是
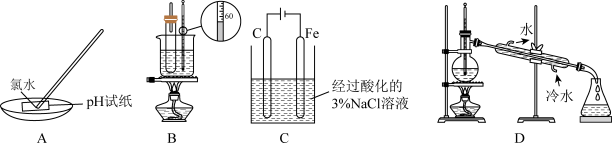

| A.图A是测定氯水的pH | B.图B是实验室制备硝基苯 |
| C.图C是用铁氰化钾溶液验证牺牲阳极法保护铁 | D.图D是分离苯和溴苯 |
您最近一年使用:0次
名校
解题方法
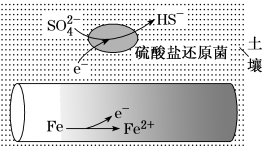
6 . 潮湿土壤中的铁管道在硫酸盐还原菌(最佳生存环境 为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
 为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
为7~8)作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图所示。下列说法错误的是
| A.铁作负极发生氧化反应 |
B.正极反应为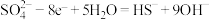 |
| C.将管道连接废锌块可防止腐蚀 |
| D.酸性环境下铁管道不易被硫酸根腐蚀 |
您最近一年使用:0次
2022-07-07更新
|
800次组卷
|
5卷引用:山东省潍坊2021-2022学年高一下学期期末测试化学试题
解题方法
7 . 工业废水中的六价铬[Cr(VI)]常采用还原沉淀法、离子交换法和微生物法等方法进行处理。
(1)室温下,含Cr(VI)的微粒在水溶液中存在如下平衡:
H2CrO4⇌H++HCrO ΔH1
ΔH1
HCrO ⇌H++CrO
⇌H++CrO ΔH2
ΔH2
2HCrO ⇌
⇌ +H2O ΔH3
+H2O ΔH3
室温下,反应2CrO +2H+⇌
+2H+⇌ +H2O的ΔH=
+H2O的ΔH=_______ (用含ΔH1、ΔH2或ΔH3的代数式表示)。
(2)还原沉淀法:使用Na2SO3将Cr(VI)还原为Cr3+,再将Cr3+转化为沉淀除去。
①酸性条件下Cr(VI)具有很强的氧化能力, 将
将 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为_______ 。
②其他条件相同,用Na2SO3处理不同初始pH的含Cr(VI)废水相同时间,当pH<2时,Cr(VI)的去除率随pH降低而降低的原因是_______ 。
(3)微生物法:
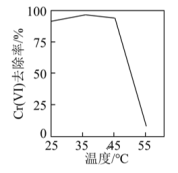
①用硫酸盐还原菌(SRB)处理含Cr(VI)废水时,Cr(VI)去除率随温度的变化如图所示。55℃时,Cr(VI)的去除率很低的原因是_______ 。
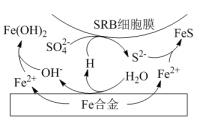
②水体中,Fe合金在SRB存在条件下腐蚀的机理如图所示。Fe腐蚀后生成FeS的过程可描述为:Fe失去电子转化为Fe2+,_______ 。
(4)离子交换法:用强碱性离子交换树脂(ROH)与 和HCrO
和HCrO 等发生离子交换,交换过程中发生如下反应:
等发生离子交换,交换过程中发生如下反应:
ROH(s)+HCrO (aq)⇌ RHCrO4(s)+OH-(aq)
(aq)⇌ RHCrO4(s)+OH-(aq)
2ROH(s)+ (aq)⇌ R2CrO4(s)+2OH-(aq)
(aq)⇌ R2CrO4(s)+2OH-(aq)
其他条件相同,当pH>4时,Cr(VI)去除率随pH升高而下降的原因是_______ 。
(1)室温下,含Cr(VI)的微粒在水溶液中存在如下平衡:
H2CrO4⇌H++HCrO
 ΔH1
ΔH1HCrO
 ⇌H++CrO
⇌H++CrO ΔH2
ΔH22HCrO
 ⇌
⇌ +H2O ΔH3
+H2O ΔH3室温下,反应2CrO
 +2H+⇌
+2H+⇌ +H2O的ΔH=
+H2O的ΔH=(2)还原沉淀法:使用Na2SO3将Cr(VI)还原为Cr3+,再将Cr3+转化为沉淀除去。
①酸性条件下Cr(VI)具有很强的氧化能力,
 将
将 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为②其他条件相同,用Na2SO3处理不同初始pH的含Cr(VI)废水相同时间,当pH<2时,Cr(VI)的去除率随pH降低而降低的原因是
(3)微生物法:
①用硫酸盐还原菌(SRB)处理含Cr(VI)废水时,Cr(VI)去除率随温度的变化如图所示。55℃时,Cr(VI)的去除率很低的原因是

②水体中,Fe合金在SRB存在条件下腐蚀的机理如图所示。Fe腐蚀后生成FeS的过程可描述为:Fe失去电子转化为Fe2+,

(4)离子交换法:用强碱性离子交换树脂(ROH)与
 和HCrO
和HCrO 等发生离子交换,交换过程中发生如下反应:
等发生离子交换,交换过程中发生如下反应:ROH(s)+HCrO
 (aq)⇌ RHCrO4(s)+OH-(aq)
(aq)⇌ RHCrO4(s)+OH-(aq)2ROH(s)+
 (aq)⇌ R2CrO4(s)+2OH-(aq)
(aq)⇌ R2CrO4(s)+2OH-(aq)其他条件相同,当pH>4时,Cr(VI)去除率随pH升高而下降的原因是
您最近一年使用:0次
8 . 含可钝化金属的工业管道或反应器,由于会被内部溶液腐蚀,通过外接电源而钝化,称之为阳极保护法。下图是某金属外接电势与电流密度的变化关系,有关说法正确的是
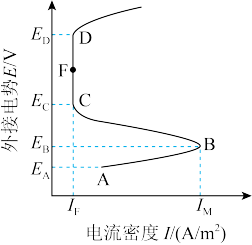

| A.阳极保护法中受保护的金属外接电源的负极 |
| B.电流密度越大,金属受保护程度越好 |
| C.CFD区,金属受到保护 |
| D.外接电势越高,对金属保护性越有效 |
您最近一年使用:0次
2022-06-14更新
|
907次组卷
|
4卷引用:江西省抚州市2022届高三下学期4月教学质量监测理综化学试题
江西省抚州市2022届高三下学期4月教学质量监测理综化学试题(已下线)专题11 金属的腐蚀与防护-备战2023年高考化学母题题源解密(广东卷)(已下线)第19讲 电解池 金属的电化学腐蚀与防护(练)-2023年高考化学一轮复习讲练测(全国通用)黑龙江省大庆实验中学实验三部2023-2024学年高三上学期阶段考试(二)化学试题
9 . 铁的腐蚀与防护与生产生活密切相关。
Ⅰ.研究铁的腐蚀
实验步骤如下:
步骤1:将铁粉放置于0.002
 溶液中浸泡,过滤后用水洗涤。
溶液中浸泡,过滤后用水洗涤。
步骤2:向15.00 mL 1 NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。
NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。
步骤3:采集溶液pH随时间变化的数据。
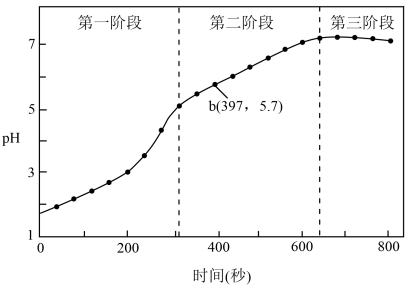
(1)第一阶段,主要发生析氢腐蚀,Cu上发生的电极反应为___________ 。
(2)第二、三阶段主要发生吸氧腐蚀。
①选取b点进行分析,经检验溶液中含有 ,写出Fe被腐蚀的总反应
,写出Fe被腐蚀的总反应___________ 。
②取b点溶液向其中滴加KSCN无明显现象,加入稀盐酸后立即变红。写出b点 被氧化的离子方程式
被氧化的离子方程式___________ 。
③依据b点发生的反应,分析第二阶段pH上升的原因是___________ 。
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知: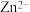 放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。
放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。
①镀件Fe应与电源的___________ 相连。
②向 电解液中加入NaCN溶液,将
电解液中加入NaCN溶液,将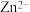 转化为
转化为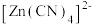 ,电解得到的镀层更加致密、细腻,原因是
,电解得到的镀层更加致密、细腻,原因是___________ 。
(4)电镀后的废水中含有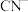 ,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c
,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c 
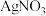 溶液滴定,消耗
溶液滴定,消耗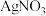 溶液V mL。已知:
溶液V mL。已知: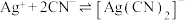 (无色)
(无色) 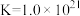 ,
,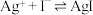
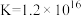 。
。
①滴定终点的现象是___________ 。
②废水中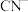 的含量是
的含量是___________  (填计算式)。
(填计算式)。
Ⅰ.研究铁的腐蚀
实验步骤如下:
步骤1:将铁粉放置于0.002

 溶液中浸泡,过滤后用水洗涤。
溶液中浸泡,过滤后用水洗涤。步骤2:向15.00 mL 1
 NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。
NaCl溶液(用盐酸调pH=1.78)中加入浸泡过的Fe粉。步骤3:采集溶液pH随时间变化的数据。

(1)第一阶段,主要发生析氢腐蚀,Cu上发生的电极反应为
(2)第二、三阶段主要发生吸氧腐蚀。
①选取b点进行分析,经检验溶液中含有
 ,写出Fe被腐蚀的总反应
,写出Fe被腐蚀的总反应②取b点溶液向其中滴加KSCN无明显现象,加入稀盐酸后立即变红。写出b点
 被氧化的离子方程式
被氧化的离子方程式③依据b点发生的反应,分析第二阶段pH上升的原因是
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知:
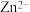 放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。
放电的速率缓慢且平稳,有利于得到致密、细腻的镀层。①镀件Fe应与电源的
②向
 电解液中加入NaCN溶液,将
电解液中加入NaCN溶液,将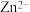 转化为
转化为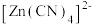 ,电解得到的镀层更加致密、细腻,原因是
,电解得到的镀层更加致密、细腻,原因是(4)电镀后的废水中含有
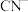 ,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c
,一种测定其含量的方法是:取废水50 mL,再加KI溶液1 mL,用c 
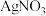 溶液滴定,消耗
溶液滴定,消耗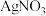 溶液V mL。已知:
溶液V mL。已知: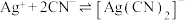 (无色)
(无色) 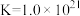 ,
,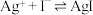
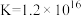 。
。①滴定终点的现象是
②废水中
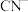 的含量是
的含量是 (填计算式)。
(填计算式)。
您最近一年使用:0次
2022-03-25更新
|
719次组卷
|
5卷引用:北京市丰台区2022届高三一模化学试题
名校
10 . 用如图所示装置及试剂进行铁的电化学腐蚀实验探究,测定具支锥形瓶中压强随时间变化关系以及溶解氧随时间变化关系的曲线如下。下列说法不正确的是
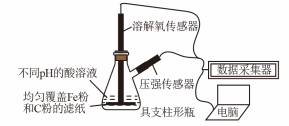
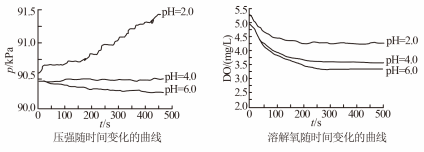


| A.压强增大主要是因为产生了H2 |
| B.整个过程中,负极电极反应式均为:Fe–2e- = Fe2+ |
| C.pH= 4.0时,体系为弱酸性,同时发生析氢腐蚀和吸氧腐蚀 |
| D.pH= 2.0时,体系为强酸性,正极只发生析氢腐蚀,电极方程式为:2H+ + 2e- = H2↑ |
您最近一年使用:0次
2021-11-26更新
|
1446次组卷
|
6卷引用:重庆南开中学2021-2022学年高一下学期4月第一次月考化学试题
重庆南开中学2021-2022学年高一下学期4月第一次月考化学试题湖北省武汉市华中师范大学第一附属中学2021-2022学年高一下学期期中考试化学试题福建省厦门市厦门双十中学2021-2022学年上学期期中考试化学试题(已下线)4.3 金属的腐蚀和防护-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)周末培优4 新型电池的电化学原理问题-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第四单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)



