解题方法
1 . 锌—空气电池可用作电动车的动力电源。该电池的电解质溶液为KOH溶液,总反应为: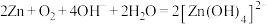 。下列说法错误的是
。下列说法错误的是
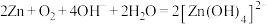 。下列说法错误的是
。下列说法错误的是A.Zn做负极, 在正极发生还原反应 在正极发生还原反应 |
| B.当电路中通过2mol电子时,消耗氧气22.4L(标准状况) |
C.电解质溶液中 向正极移动 向正极移动 |
D.负极反应式为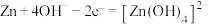 |
您最近一年使用:0次
2 . 液体锌电池具有成本低、安全性强等特点,其工作原理如图所示(KOH凝胶中允许离子存在、生成或迁移)。
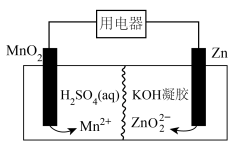
下列说法正确的是

下列说法正确的是
A.电流由 极经用电器流向Zn极 极经用电器流向Zn极 |
B.负极反应式为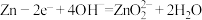 |
| C.工作一段时间后,锌极区pH升高 |
| D.13.0gZn参与反应,理论上电路中转移0.2mol电子 |
您最近一年使用:0次
3 . 科学家开发出一种新系统,用于捕捉 生成氢气并产生电能,其工作原理如图所示,下列说法正确的是
生成氢气并产生电能,其工作原理如图所示,下列说法正确的是
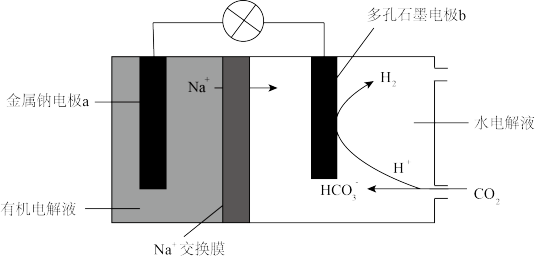
 生成氢气并产生电能,其工作原理如图所示,下列说法正确的是
生成氢气并产生电能,其工作原理如图所示,下列说法正确的是
A.电极 发生还原反应 发生还原反应 |
| B.可以用乙酸作有机电解液 |
C.电池总反应为 |
D.当电路中转移 电子时, 电子时, 极产生 极产生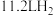 |
您最近一年使用:0次
2023-06-28更新
|
60次组卷
|
2卷引用:陕西省安康市2022-2023学年高二下学期6月期末考试化学试题
4 . 电化学在物质制备、新材料和环境保护等方面具有独到的应用优势。
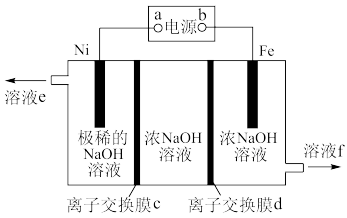
(1)高铁酸钠(Na2FeO4)是一种新型水处理剂,强碱性条件下稳定存在。电解法制备Na2FeO4的工作原理如图所示,a是电源的______ 极(填“正”或“负”)。阳极电极的电极反应式为_____ ,其中离子交换膜c是______ (阳离子交换膜或阴离子交换膜)。
(2)燃煤烟气中的SO2可用如图装置进行处理。
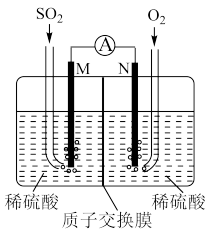
M极发生的电极反应式为_____ ,当外电路通过0.2mol电子时,质子交换膜左侧溶液质量的变化______ g。
(1)高铁酸钠(Na2FeO4)是一种新型水处理剂,强碱性条件下稳定存在。电解法制备Na2FeO4的工作原理如图所示,a是电源的

(2)燃煤烟气中的SO2可用如图装置进行处理。

M极发生的电极反应式为
您最近一年使用:0次
解题方法
5 . 如图所示,若电解5min时铜电极质量增加2.16g,回答:
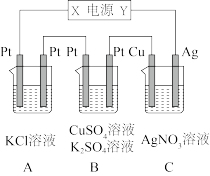
(1)电源电极X名称为___________ 。
(2)pH变化:A池___________ ,B池___________ ,C池___________ 。
(3)若A中KCl溶液的体积是200mL,电解后溶液的pH=___________ 。

(1)电源电极X名称为
(2)pH变化:A池
(3)若A中KCl溶液的体积是200mL,电解后溶液的pH=
您最近一年使用:0次
6 . Ⅰ.我国是世界氯碱工业大国,氯碱工业即采用电解饱和食盐水的方法来制备工业原料 、
、 、NaOH,它广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。其电解装置原理图如图1。
、NaOH,它广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。其电解装置原理图如图1。
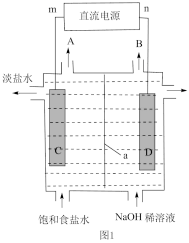
(1)n为直流电源的___________ (填“正”或“负”)极,电极D附近的pH___________ (填“增大”、“减小”或“不变”);离子交换膜a为___________ (填“阴”或“阳”)离子交换膜。
(2)写出该电解装置的总反应方程式:___________ 。
Ⅱ.一次化学实验课上,某兴趣小组组装了电化学装置(如图2),其中A、B、C、D、E、F均为石墨电极,U形管中为滴有几滴酚酞的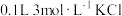 溶液,甲、乙烧杯中溶质电离出的离子均是
溶液,甲、乙烧杯中溶质电离出的离子均是 、
、 、
、 、
、 中的某两种,通电后甲、乙两烧杯中溶液pH随时间变化的曲线如图3所示,已知通电一段时间后,F极产生的气体体积比A极产生的少1.12L(标准状况下)。
中的某两种,通电后甲、乙两烧杯中溶液pH随时间变化的曲线如图3所示,已知通电一段时间后,F极产生的气体体积比A极产生的少1.12L(标准状况下)。
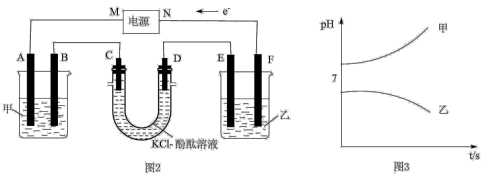
(3)甲、乙两烧杯中溶液的溶质分别为___________ 、___________ 。(填化学式)
(4)F极上的电极反应式为___________ 。
(5)①U形管中溶液先变红的一极为___________ (填“C”或“D”)极。
②若要将U形管中的溶液恢复到电解前的状态,应加入___________ mol的___________ (填物质名称)。
 、
、 、NaOH,它广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。其电解装置原理图如图1。
、NaOH,它广泛应用于轻工业、纺织工业、冶金工业、石油化学工业以及公用事业。其电解装置原理图如图1。
(1)n为直流电源的
(2)写出该电解装置的总反应方程式:
Ⅱ.一次化学实验课上,某兴趣小组组装了电化学装置(如图2),其中A、B、C、D、E、F均为石墨电极,U形管中为滴有几滴酚酞的
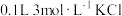 溶液,甲、乙烧杯中溶质电离出的离子均是
溶液,甲、乙烧杯中溶质电离出的离子均是 、
、 、
、 、
、 中的某两种,通电后甲、乙两烧杯中溶液pH随时间变化的曲线如图3所示,已知通电一段时间后,F极产生的气体体积比A极产生的少1.12L(标准状况下)。
中的某两种,通电后甲、乙两烧杯中溶液pH随时间变化的曲线如图3所示,已知通电一段时间后,F极产生的气体体积比A极产生的少1.12L(标准状况下)。
(3)甲、乙两烧杯中溶液的溶质分别为
(4)F极上的电极反应式为
(5)①U形管中溶液先变红的一极为
②若要将U形管中的溶液恢复到电解前的状态,应加入
您最近一年使用:0次
2022-01-08更新
|
179次组卷
|
4卷引用:陕西省安康市2021-2022学年高二上学期期末考试化学试题
名校
解题方法
7 . 利用电解法将CO2转化为CH4的原理如图所示(两电极均为惰性电极且完全相同),下列说法正确的是
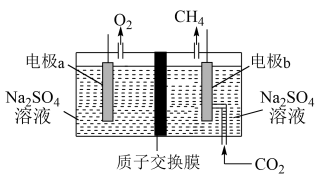

A.电极a上的反应为 |
| B.电池工作一段时间后,左侧Na2SO4溶液浓度降低 |
| C.电解过程中化学能转化为电能 |
| D.每转移1 mol电子,此时生成的O2和CH4的质量比为4:1 |
您最近一年使用:0次
2021-12-20更新
|
939次组卷
|
14卷引用:陕西省安康市2021-2022学年高二上学期期末考试化学试题
陕西省安康市2021-2022学年高二上学期期末考试化学试题湖北省部分名校2021-2022学年高二上学期12月联考化学试题云南省名校联盟2021-2022学年高二上学期期末考试化学试题辽宁省县级重点高中协作体2021-2022学年高二上学期期末考试化学试题湖南省岳阳市岳阳县第一中学2021-2022学年高二下学期期中考试化学试题江西省丰城市第九中学2021-2022学年高二上学期期末考试化学试题陕西省黄陵中学2021-2022学年高二上学期期末考试化学试题江苏省江阴市四校2022-2023学年高二上学期期中联考化学试题湖北省潜江市华师潜江附属中学2021-2022学年高二上学期期末考试化学试题天津市第一中学2022-2023学年高二上学期期中考试化学试题新疆哈密第十五中学2021-2022学年高二上学期期末考试化学试题吉林省吉林松花江中学2022-2023学年高二上学期1月期末考试化学试题贵州省龙里中学2022-2023学年高二上学期11月期中考试化学试题福建省福州屏东中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
8 . 已知部分弱酸的电离平衡常数如下表,根据表中数据回答下列问题。
(1)已知某浓度的NaCN水溶液pH=8,原因是___________ (用离子方程式表示),pH=8的NaCN溶液中,由水电离出的OH-浓度为___________ 。
(2)同浓度HCOONa、NaCN、NaHCO3、Na2CO3这4种溶液中碱性由强到弱的顺序是___________ ;NaHCO3溶液中各离子浓度由大到小的顺序是___________ 。
(3)体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)___________ 。
(4)其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:
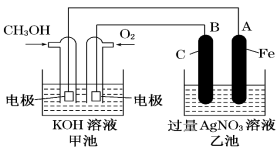
①甲池中,通入甲醇电极反应式为___________ 。
②乙池中,总反应离子方程式为___________ 。
③在此过程中若完全反应,乙池中A极的质量增加648g,则甲池中理论上消耗O2_____ L(标准状况下)。
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常(25℃) | Ka=1.77104 | Ka=5.01010 | Ka1=4.3107 Ka2=5.61011 |
(2)同浓度HCOONa、NaCN、NaHCO3、Na2CO3这4种溶液中碱性由强到弱的顺序是
(3)体积相同、c(H+)相同的三种酸溶液a.HCOOH;b.HCN;c.HCl分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)
(4)其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:

①甲池中,通入甲醇电极反应式为
②乙池中,总反应离子方程式为
③在此过程中若完全反应,乙池中A极的质量增加648g,则甲池中理论上消耗O2
您最近一年使用:0次
2021-12-06更新
|
498次组卷
|
3卷引用:陕西省安康市白河高中2021-2022学年高二上学期期末考试(实验班)化学试题



