名校
1 . 用铜片、银片设计成如图所示的原电池。以下有关该原电池的叙述正确的是
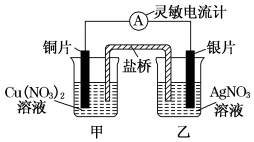

| A.电流从铜电极通过灵敏电流计流向银电极 |
| B.盐桥中的阴离子向AgNO3溶液中迁移 |
| C.银片上发生的电极反应是:Ag-e-=Ag+ |
| D.铜片插入硝酸银溶液中发生的化学反应与该原电池总反应相同 |
您最近一年使用:0次
名校
解题方法
2 . 高能LiFePO4电池,多应用于公共交通。电池中间是聚合物的隔膜,主要作用是在反应过程中只让Li+通过。结构如图所示:
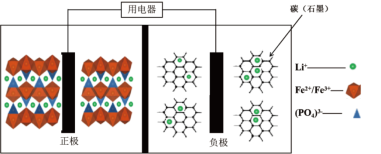
原理为:(1− x)LiFePO4+xFePO4+LixCn LiFePO4+nC。下列说法
LiFePO4+nC。下列说法不正确 的是

原理为:(1− x)LiFePO4+xFePO4+LixCn
 LiFePO4+nC。下列说法
LiFePO4+nC。下列说法A.放电时,导线中每流过 ,理论上就有2 mol Li+从正极区经聚合物隔膜向负极区移动并嵌入石墨中 ,理论上就有2 mol Li+从正极区经聚合物隔膜向负极区移动并嵌入石墨中 |
| B.正极和负极的质量变化相等 |
| C.拆解废电池前先进行充电处理既可以保证安全又有利于回收锂 |
| D.放电时,正极电极反应式:xFePO4+xLi++xe− =xLiFePO4 |
您最近一年使用:0次
名校
解题方法
3 . 由锌片、铜片和200mL稀H2SO4组成的原电池如下图所示:
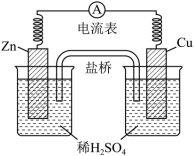
(1)原电池的负极反应式为___________ ,正极反应式为___________ ,盐桥中的K+向___________ (填“铜”或“锌”)电极移动。
(2)一段时间后,当在铜片上放出5.6L(标准状况)气体时,H2SO4恰好消耗一半,则产生这些气体的同时,共消耗___________ g锌,有___________ mol电子通过了导线,原硫酸的物质的量浓度是___________ 。
(3)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为___________ 。

(1)原电池的负极反应式为
(2)一段时间后,当在铜片上放出5.6L(标准状况)气体时,H2SO4恰好消耗一半,则产生这些气体的同时,共消耗
(3)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为
您最近一年使用:0次
4 . 下列有关原电池的说法正确的是
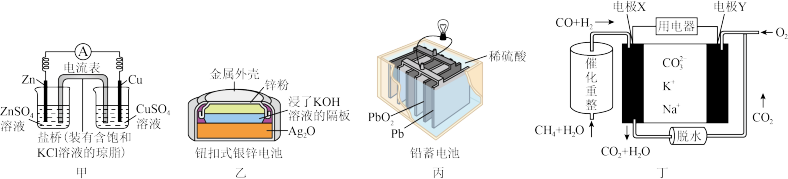

A.图甲所示装置工作时,盐桥中的 会向右池移动 会向右池移动 |
B.图乙所示装置工作时,正极的电极反应式为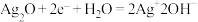 |
C.图丙所示装置工作时,电子从Pb电极流出,经电解质溶液回到 电极 电极 |
D.图丁所示装置工作时,正极的电池反应式为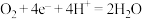 |
您最近一年使用:0次
名校
5 . 某化学兴趣小组,使用相同的铜片和锌片为电极,探究水果电池水果的种类和电极间距离对电流的影响,实验装置图和所得实验所得数据如下:
电池工作时,下列说法不正确 的是
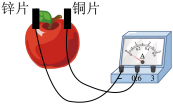
实验编号 | 水果种类 | 电极间距离/cm | 电流/ |
Ⅰ | 番茄 | 1 | 98.7 |
Ⅱ | 番茄 | 2 | 72.5 |
Ⅲ | 苹果 | 2 | 27.2 |
A.负极的电极反应为 |
| B.电子从锌片经水果流向铜片 |
| C.水果种类和电极间距离对电流数值的大小均有影响 |
| D.若用石墨电极代替铜片进行实验,电流数值会发生变化 |
您最近一年使用:0次
2024-01-20更新
|
185次组卷
|
3卷引用:北京市顺义区2023-2024学年高二上学期期末质量监测化学试题
名校
6 . 电化学的应用领域非常广泛。下列说法不正确的是
| A.铜板上铁铆钉在中性水膜中被腐蚀时,正极发生的电极反应为:O2+2H2O+4e-=4OH- |
| B.电解CuCl2溶液时,与直流电源负极相连的石墨棒上逐渐覆盖红色的铜 |
| C.电解饱和食盐水的过程中,阴极区碱性不断增强 |
| D.铅蓄电池放电时,电子由PbO2通过导线流向Pb |
您最近一年使用:0次
名校
解题方法
7 . 为了实现碳中和, 的处理成为各国科学家的研究重点。
的处理成为各国科学家的研究重点。
Ⅰ.将二氧化碳转化为绿色液体燃料甲醇,制备原理为 。已知某些化学键的键能数据如表所示。
。已知某些化学键的键能数据如表所示。
(1)当反应 生成
生成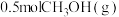 时,
时,_____ (填“放出”或“吸收”)_____  能量。
能量。
(2)在体积为 的恒温、恒容密闭容器中,充入
的恒温、恒容密闭容器中,充入 和
和 进行反应
进行反应 (不考虑其他副反应)。
(不考虑其他副反应)。 时,测得
时,测得 和
和 的体积分数之比为
的体积分数之比为 且比值不再随时间变化。回答下列问题:
且比值不再随时间变化。回答下列问题:
①反应开始到平衡时,以 的浓度变化表示反应的平均速率v(H2)=
的浓度变化表示反应的平均速率v(H2)=_____  。
。
② 时,正、逆反应速率的大小关系为
时,正、逆反应速率的大小关系为
_____  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③该条件下反应达到平衡的标志有_____ (填字母)。
A. 和
和 的浓度之比为
的浓度之比为
B.断裂 键的同时生成
键的同时生成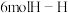 键
键
C.容器内混合气体的密度保持不变
D.容器内混合气体的平均摩尔质量保持不变
Ⅱ.用二氧化碳作原料设计 辅助
辅助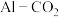 电池,电池反应产物为
电池,电池反应产物为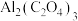 ,电池工作原理如图所示。正极的电极反应式为
,电池工作原理如图所示。正极的电极反应式为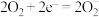 、
、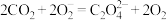 。
。_____ (填“ ”或“多孔碳”)电极流出,电池的负极反应式为
”或“多孔碳”)电极流出,电池的负极反应式为_____ 。
 的处理成为各国科学家的研究重点。
的处理成为各国科学家的研究重点。Ⅰ.将二氧化碳转化为绿色液体燃料甲醇,制备原理为
 。已知某些化学键的键能数据如表所示。
。已知某些化学键的键能数据如表所示。| 化学键 |  |  |  |  |  |
键能/( ) ) | 413.6 | 436.0 | 351.0 | 745.0 | 462.8 |
(1)当反应
 生成
生成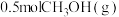 时,
时, 能量。
能量。(2)在体积为
 的恒温、恒容密闭容器中,充入
的恒温、恒容密闭容器中,充入 和
和 进行反应
进行反应 (不考虑其他副反应)。
(不考虑其他副反应)。 时,测得
时,测得 和
和 的体积分数之比为
的体积分数之比为 且比值不再随时间变化。回答下列问题:
且比值不再随时间变化。回答下列问题:①反应开始到平衡时,以
 的浓度变化表示反应的平均速率v(H2)=
的浓度变化表示反应的平均速率v(H2)= 。
。②
 时,正、逆反应速率的大小关系为
时,正、逆反应速率的大小关系为
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③该条件下反应达到平衡的标志有
A.
 和
和 的浓度之比为
的浓度之比为
B.断裂
 键的同时生成
键的同时生成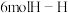 键
键C.容器内混合气体的密度保持不变
D.容器内混合气体的平均摩尔质量保持不变
Ⅱ.用二氧化碳作原料设计
 辅助
辅助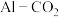 电池,电池反应产物为
电池,电池反应产物为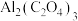 ,电池工作原理如图所示。正极的电极反应式为
,电池工作原理如图所示。正极的电极反应式为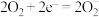 、
、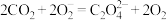 。
。
 ”或“多孔碳”)电极流出,电池的负极反应式为
”或“多孔碳”)电极流出,电池的负极反应式为
您最近一年使用:0次
8 . 一种染料敏化太阳能电池如图,其成本便宜且对环境无污染。敏化染料(S)吸附在 纳米空心球表面。光照时:
纳米空心球表面。光照时: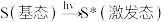 ,
,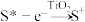 。下列说法正确的是
。下列说法正确的是

 纳米空心球表面。光照时:
纳米空心球表面。光照时: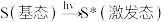 ,
,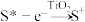 。下列说法正确的是
。下列说法正确的是
A.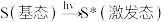 需要释放能量 需要释放能量 |
B.N极的电极反应式为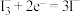 |
C.敏化染料还原过程为 |
| D.该电池工作一段时间后需要补充电解质 |
您最近一年使用:0次
名校
解题方法
9 . 已知氧化性 >Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
>Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
 >Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是
>Fe3+,设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法不正确的是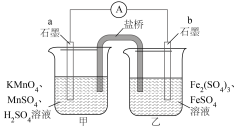
| A.a为电池的负极,b为电池的正极 |
| B.电流从a经过外电路流向b |
C.电池工作时,盐桥中的 移向乙烧杯 移向乙烧杯 |
D.A电极上发生的反应为: +8H++5e- = Mn2++4H2O +8H++5e- = Mn2++4H2O |
您最近一年使用:0次
名校
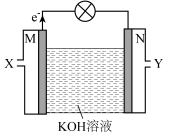
10 . 以肼 为燃料、空气为助燃剂可设计碱性燃料电池,其工作原理如图所示。该电池的优势是能源转化率高,且产物无污染。下列说法错误的是
为燃料、空气为助燃剂可设计碱性燃料电池,其工作原理如图所示。该电池的优势是能源转化率高,且产物无污染。下列说法错误的是
 为燃料、空气为助燃剂可设计碱性燃料电池,其工作原理如图所示。该电池的优势是能源转化率高,且产物无污染。下列说法错误的是
为燃料、空气为助燃剂可设计碱性燃料电池,其工作原理如图所示。该电池的优势是能源转化率高,且产物无污染。下列说法错误的是
| A.空气由Y口通入 |
B.M极的电极反应为 |
C.电池的总反应为 |
| D.电池工作时,溶液的pH增大 |
您最近一年使用:0次
2024-01-15更新
|
431次组卷
|
2卷引用:河北省沧州市部分学校2023-2024学年高三上学期12月联考化学试题