1 . 某研究性学习小组用如图所示的装置进行实验,探究原电池、电解池和电解精炼钴的工作原理。一段时间后装置甲的两极均有气体产生,且X极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。请根据实验现象及所查资料,回答下列问题:
查阅资料:高铁酸根( )在溶液中呈紫红色。
)在溶液中呈紫红色。
(2)装置丙中,若外电路中有0.2 mol电子转移,则有___________ mol  透过隔膜,隔膜右侧溶液质量如何变化:
透过隔膜,隔膜右侧溶液质量如何变化:___________ 。
(3)反应过程中,X极处发生的电极反应为 和
和___________ 。
(4)一段时间后,若X极质量减小1.12 g,Y极收集到2.24 L气体,则在X极收集到的气体为___________ mL(均已折算为标准状况时的气体体积)。
(5)乙池是电解制备金属钴的装置图,理论上Ⅰ室中
___________ (填“变大”“变小”或“不变”),该电解池总反应的化学方程式是___________ 。
(6)若撤掉装置乙中的阳离子交换膜,石墨电极上产生的气体除O2外,还可能有___________ 。
查阅资料:高铁酸根(
 )在溶液中呈紫红色。
)在溶液中呈紫红色。
| A.X(Fe) | B.Y(C) | C.Co | D.Zn |
(2)装置丙中,若外电路中有0.2 mol电子转移,则有
 透过隔膜,隔膜右侧溶液质量如何变化:
透过隔膜,隔膜右侧溶液质量如何变化:(3)反应过程中,X极处发生的电极反应为
 和
和(4)一段时间后,若X极质量减小1.12 g,Y极收集到2.24 L气体,则在X极收集到的气体为
(5)乙池是电解制备金属钴的装置图,理论上Ⅰ室中

(6)若撤掉装置乙中的阳离子交换膜,石墨电极上产生的气体除O2外,还可能有
您最近一年使用:0次
2 . 根据实验目的,下列实验及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 比较金属的活泼性 | Mg、Al做电极,NaOH溶液为离子导体构成原电池,Mg电极附近产生气泡 | Al为正极 |
| B | 探究沉淀的转化 | 向1mL0.01mol•L-1MgCl2溶液中先加入1mL0.05mol•L-1NaOH溶液,再逐滴加入0.1mol•L-1CuSO4溶液,先出现白色沉淀,后又出现蓝色沉淀 | Ksp:Mg(OH)2>Cu(OH)2 |
| C | 探究Mg(OH)2溶于铵盐的原理 | 向Mg(OH)2悬浊液中加入少量NH4Cl固体,溶液变澄清 | NH 水解产生的H+中和Mg(OH)2溶解平衡产生的OH-,使溶解平衡正向移动 水解产生的H+中和Mg(OH)2溶解平衡产生的OH-,使溶解平衡正向移动 |
| D | 比较H2SO3和H2CO3的Ka2 | 测定浓度均为0.1mol•L-1的Na2SO3和Na2CO3溶液的pH值,前者小于后者 | Ka2:H2SO3>H2CO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 用如图所示装置进行相应实验,能达到实验目的的是
| 选项 | A | B | C | D |
| 装置 | 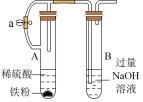 |  | 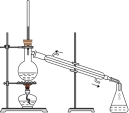 | 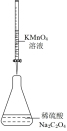 |
| 目的 | 制取 沉淀 沉淀 | 将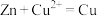 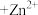 设计成原电池装置 设计成原电池装置 | 分离苯和硝基苯 | 测定 溶液的物质的量浓度 溶液的物质的量浓度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-18更新
|
1279次组卷
|
4卷引用:吉林省洮南市第一中学2022-2023学年高二上学期期末考试化学试题
吉林省洮南市第一中学2022-2023学年高二上学期期末考试化学试题青海省西宁市城西区青海师范大学附属实验中学2022-2023学年高二上学期12月月考化学试题 湖北省2022届高三5月联考化学试题(已下线)专题11 化学实验基础-三年(2020-2022)高考真题分项汇编
4 . 电解工作原理的实际应用非常广泛。
(1)电解精炼银时,粗银作___________ ,阴极反应为___________ 。
(2)工业上为了处理含有Cr2O 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
(3)某同学设计了如图装置进行以下电化学实验。
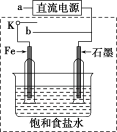
①当开关K与a连接时,两极均有气泡产生,则阴极为___________ 电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为___________ 。请写出此时Fe电极上的电极反应___________ 。
(4)1 L某溶液中含有的离子如下表:
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是___________(填字母)。
(1)电解精炼银时,粗银作
(2)工业上为了处理含有Cr2O
 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。| A.阳极反应:Fe-2e-=Fe2+ | B.阴极反应:2H++2e-=H2↑ |
| C.在电解过程中工业废水由酸性变为碱性 | D.可以将铁电极改为石墨电极 |

①当开关K与a连接时,两极均有气泡产生,则阴极为
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为
(4)1 L某溶液中含有的离子如下表:
| 离子 | Cu2+ | Al3+ | NO | Cl- |
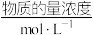 | 1 | 1 | a | 1 |
| A.电解后溶液呈酸性 | B.a=3 |
| C.阳极生成1.5 mol Cl2 | D.阴极析出的金属是铜与铝 |
您最近一年使用:0次
解题方法
5 . 如图是牺牲阳极法保护金属的实验装置图,烧杯内为经过酸化的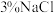 溶液。
溶液。
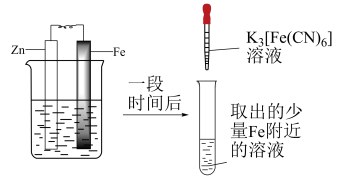
下列关于该装置的叙述错误的是
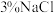 溶液。
溶液。
下列关于该装置的叙述错误的是
| A.铁作正极被保护 |
B.将 换成 换成 ,也可以保护铁不被腐蚀 ,也可以保护铁不被腐蚀 |
C.向试管中加入 溶液,无明显现象 溶液,无明显现象 |
D.正极反应式为 |
您最近一年使用:0次
6 . 科创小组设计下图装置探究铝片做电极材料时的原电池反应并进行实验、记录。
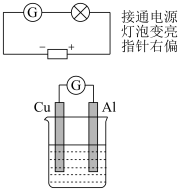
实验1:
实验2:煮沸冷却后的
根据上述实验推测,下列说法错误的是

实验1:

实验2:煮沸冷却后的

| 编号 | 实验1 | 实验2 |
| 实验现象 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约10分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约3分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
A.上述两实验中,开始时铜片表面得电子的物质是 |
| B.铜片表面开始产生气泡的时间长短与溶液中溶解氧的多少有关 |
C.铜片表面产生的气泡为 |
| D.若将铜片换成镁条,则电流计指针先向左偏转后向右偏转,镁条表面有气泡逸出 |
您最近一年使用:0次
7 . 氧化还原反应可拆分为氧化和还原两个“半反应”,某小组同学从“半反应”的角度探究反应规律。
(1)已知: 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。
①该转化的还原半反应是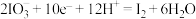 ,则相应的氧化半反应是
,则相应的氧化半反应是___________ 。
②分析上述还原半反应可知:增大 可促进
可促进 得到电子,使其
得到电子,使其___________ 性增强,进而与 发生反应。
发生反应。
(2)探究 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。
①有同学认为 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是___________ 。
用如下装置进行实验【硫酸与浓盐酸中 接近】。
接近】。
②甲实验的目的是___________ 。
③a.丙中气球变鼓是因为生成了___________ 气体(填化学式)。
b.经检测,丙中反应后溶液中存在 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:___________ 。
(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧 电极表面有
电极表面有 析出。
析出。
①该装置中左侧  电极作
电极作___________ (填“正”或“负”)极。
②写出该装置右侧 烧杯中的电极反应式___________ 。
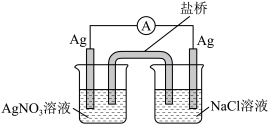
对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池__________ 。
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
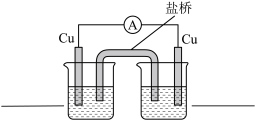
a.若能,在右装置图中填写烧杯中的试剂,并标出电子的移动方向 。
b.若不能,说明原因。
(1)已知:
 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。①该转化的还原半反应是
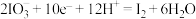 ,则相应的氧化半反应是
,则相应的氧化半反应是②分析上述还原半反应可知:增大
 可促进
可促进 得到电子,使其
得到电子,使其 发生反应。
发生反应。(2)探究
 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。①有同学认为
 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是用如下装置进行实验【硫酸与浓盐酸中
 接近】。
接近】。| 装置 | 序号 | 试管内药品 | 现象 |
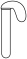 | 甲 | 浓盐酸 | 24小时后仍无明显变化 |
| 乙 |  粉+硫酸 粉+硫酸 | 24小时后仍无明显变化 | |
| 丙 |  粉+浓盐酸 粉+浓盐酸 | 24小时后气球变鼓 |
③a.丙中气球变鼓是因为生成了
b.经检测,丙中反应后溶液中存在
 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧
 电极表面有
电极表面有 析出。
析出。①该装置中
 电极作
电极作②写出该装置

对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
a.若能,在右装置图中填写烧杯中的试剂,
b.若不能,说明原因。
您最近一年使用:0次
8 . 应用电化学原理,回答下列问题:

(1)上述三个装置中,负极反应物化学性质上的共同特点是___________ 。
(2)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是___________ 。
(3)乙中正极反应式为___________ ;若将 换成
换成 ,则负极反应式为
,则负极反应式为___________ 。
(4)丙中正极的电极反应式为___________ 。
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。按下图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:
ⅰ.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ⅱ.随后向U型管左侧逐渐加入浓 溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
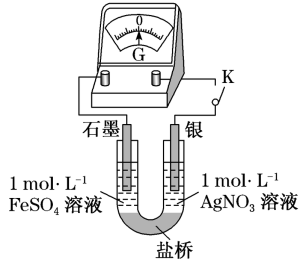
①实验ⅰ中银作___________ 极。
②综合实验ⅰ、ⅱ的现象,得出 和
和 反应的离子方程式是
反应的离子方程式是___________

(1)上述三个装置中,负极反应物化学性质上的共同特点是
(2)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是
(3)乙中正极反应式为
 换成
换成 ,则负极反应式为
,则负极反应式为(4)丙中正极的电极反应式为
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。按下图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:
ⅰ.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ⅱ.随后向U型管左侧逐渐加入浓
 溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
①实验ⅰ中银作
②综合实验ⅰ、ⅱ的现象,得出
 和
和 反应的离子方程式是
反应的离子方程式是
您最近一年使用:0次
2022-12-02更新
|
321次组卷
|
2卷引用:广东省广州大学附中2023-2024学年高二上学期期末化学模拟试卷
解题方法
9 . 为了探究原电池和电解池的工作原理,某研究性学习小组分别用下图所示的装置进行实验。据图回答问题。
Ⅰ.用图甲所示装置进行第一组实验时:
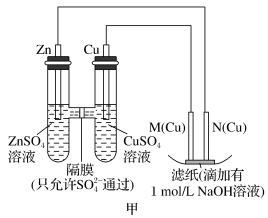
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是_______(填字母)。
(2)实验过程中,
_______ (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象是_______ 。
Ⅱ.该小组同学用图乙所示装置打算进行二组实验时发现,两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根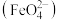 在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
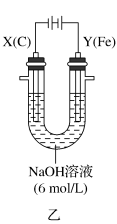
(3)电解过程中,X极处溶液的 浓度
浓度_______ (填“增大”“减小”或“不变)。
(4)电解过程中,Y极发生的电极反应为 和
和_______ 。
(5)电解进行一段时间后,若在X极收集到672mL气体,Y电板(铁电极)质量减小0.28g,则在Y极收集到气体为_______ mL(均已折算为标准状况时气体体积)。
(6)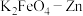 也可以组成碱性电池,
也可以组成碱性电池, 在电池中作为正极材料,其电池反应总反应式为
在电池中作为正极材料,其电池反应总反应式为 ,该电池正极发生的电极反应式为
,该电池正极发生的电极反应式为_______ 。
Ⅰ.用图甲所示装置进行第一组实验时:

(1)在保证电极反应不变的情况下,不能替代Cu作电极的是_______(填字母)。
| A.石墨 | B.镁 | C.银 | D.铂 |

Ⅱ.该小组同学用图乙所示装置打算进行二组实验时发现,两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根
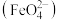 在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
(3)电解过程中,X极处溶液的
 浓度
浓度(4)电解过程中,Y极发生的电极反应为
 和
和(5)电解进行一段时间后,若在X极收集到672mL气体,Y电板(铁电极)质量减小0.28g,则在Y极收集到气体为
(6)
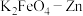 也可以组成碱性电池,
也可以组成碱性电池, 在电池中作为正极材料,其电池反应总反应式为
在电池中作为正极材料,其电池反应总反应式为 ,该电池正极发生的电极反应式为
,该电池正极发生的电极反应式为
您最近一年使用:0次
名校
解题方法
10 . 某小组同学为探究 和
和 反应的程度,进行以下实验。已知:相关物质的
反应的程度,进行以下实验。已知:相关物质的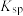 (25℃) AgCl:
(25℃) AgCl:
 :
:
(1)甲同学的实验如下:
注:经检验黑色固体为Ag。
①白色沉淀的化学式是___________ 。
②甲同学得出 氧化了
氧化了 的依据是
的依据是___________ 。
(2)乙同学为探究 和
和 反应的程度,进行实验Ⅱ。
反应的程度,进行实验Ⅱ。
a.按下图连接装置并加入药品(盐桥中的物质不参与反应),发现电压表指针偏移。
偏移的方向表明:电子由石墨经导线流向银。放置一段时间后,指针偏移减小。
b.随后向甲烧杯中逐渐加入浓 溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
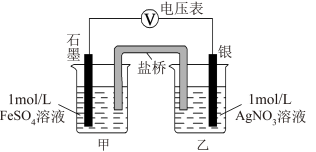
①a中甲烧杯里的电极反应式是___________ 。
②b中电压表指逆向偏移后,银为极___________ (填“正”或“负”)。
③由实验得出 和
和 反应的离子方程式是
反应的离子方程式是___________ 。
 和
和 反应的程度,进行以下实验。已知:相关物质的
反应的程度,进行以下实验。已知:相关物质的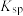 (25℃) AgCl:
(25℃) AgCl:
 :
:
(1)甲同学的实验如下:
序号 | 操作 | 现象 |
实验1 | 将2mL | 产生白色沉淀,随后有黑色固体产生 |
取上层清液,滴加KSCN溶液 | 溶液变红 |
①白色沉淀的化学式是
②甲同学得出
 氧化了
氧化了 的依据是
的依据是(2)乙同学为探究
 和
和 反应的程度,进行实验Ⅱ。
反应的程度,进行实验Ⅱ。a.按下图连接装置并加入药品(盐桥中的物质不参与反应),发现电压表指针偏移。
偏移的方向表明:电子由石墨经导线流向银。放置一段时间后,指针偏移减小。
b.随后向甲烧杯中逐渐加入浓
 溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
①a中甲烧杯里的电极反应式是
②b中电压表指逆向偏移后,银为极
③由实验得出
 和
和 反应的离子方程式是
反应的离子方程式是
您最近一年使用:0次
2022-12-04更新
|
130次组卷
|
2卷引用:山西省大同市2022-2023学年高二上学期期末考试化学试题

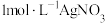 溶液加入到
溶液加入到 溶液中
溶液中

