1 . 化学电池的发明,是贮能和供能技术的巨大进步。______ (填“正极”或“负极”)。
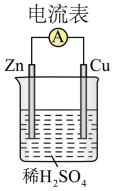
(2)装置中锌片上发生_____ (“氧化”或“还原”)反应,写出负极发生的电极反应式______ 。
(3)电子流动的方向是________ (“Zn→Cu”或“Cu→Zn”)。
(4)上图所示装置可将_______ (写离子方程式)反应释放的能量 直接转变为电能;能证明产生电能的实验现象是________ 。
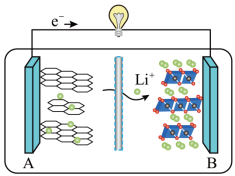
(5)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。___________ (填序号)。
①A为电池的正极 ②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
(2)装置中锌片上发生
(3)电子流动的方向是
(4)上图所示装置可将
(5)2019 年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。
①A为电池的正极 ②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
您最近一年使用:0次
2024-01-06更新
|
32次组卷
|
2卷引用:黑龙江省海林市朝鲜族中学2023-2024学年高二上学期第三次考试(期末)化学试卷
名校
2 . 回答下列问题
(1)依据反应: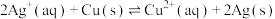 设计的原电池如下图甲所示。
设计的原电池如下图甲所示。
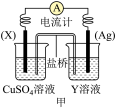
①电极 的材料是
的材料是_______ ;Y溶液可以是_______ ;
②银电极上发生的电极反应式是_______ , 电极上发生的电极反应为
电极上发生的电极反应为_______ 反应(填“氧化”或“还原”);外电路中的电子_______ (填“流出”或“流向”)Ag电极。
(2)次磷酸 是一种精细化工产品,已知
是一种精细化工产品,已知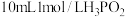 与
与 的
的 溶液充分反应后生成组成为
溶液充分反应后生成组成为 的盐,则:
的盐,则:
①次磷酸 属于
属于_______ (填“一元酸”“二元酸”或“无法确定”)。
②设计实验方案,证明次磷酸是弱酸:_______ 。
(3)某课外兴趣小组用 的
的 标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
①该小组同学选用酚酞做指示剂,滴定终点的现象为_______ 。
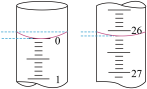
②该小组某一次滴定操作中,酸式滴定管的始终液面如图所示,则本次滴入的盐酸体积为_______  。
。
③下列操作中,可能使所测盐酸溶液的浓度值偏低的是_______
A.碱式滴定管末用标准氢氧化钠溶液润洗就直接注入标准溶液
B.碱式滴定管在滴定前有气泡,滴定后气泡消失
C.读取氢氧化钠体积时,滴定结束时俯视读数
D.滴定前盛放盐酸溶液的锥形瓶用蒸馏水洗净后没有干燥
(1)依据反应:
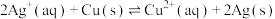 设计的原电池如下图甲所示。
设计的原电池如下图甲所示。
①电极
 的材料是
的材料是②银电极上发生的电极反应式是
 电极上发生的电极反应为
电极上发生的电极反应为(2)次磷酸
 是一种精细化工产品,已知
是一种精细化工产品,已知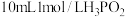 与
与 的
的 溶液充分反应后生成组成为
溶液充分反应后生成组成为 的盐,则:
的盐,则:①次磷酸
 属于
属于②设计实验方案,证明次磷酸是弱酸:
(3)某课外兴趣小组用
 的
的 标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。
标准溶液滴定未知浓度的盐酸溶液,实验操作如下,请完成以下问题。①该小组同学选用酚酞做指示剂,滴定终点的现象为
②该小组某一次滴定操作中,酸式滴定管的始终液面如图所示,则本次滴入的盐酸体积为
 。
。
③下列操作中,可能使所测盐酸溶液的浓度值偏低的是
A.碱式滴定管末用标准氢氧化钠溶液润洗就直接注入标准溶液
B.碱式滴定管在滴定前有气泡,滴定后气泡消失
C.读取氢氧化钠体积时,滴定结束时俯视读数
D.滴定前盛放盐酸溶液的锥形瓶用蒸馏水洗净后没有干燥
您最近一年使用:0次
2023-01-08更新
|
179次组卷
|
2卷引用:广东省广州中学2022-2023学年高二上学期期末考试化学试题
解题方法
3 . Ⅰ、某小组同学用下列试剂研究将 转化为
转化为 。(已知:
。(已知: ,
, )
)
(1)实验操作:所用试剂: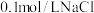 溶液,
溶液, 溶液,
溶液,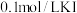 溶液;向盛有
溶液;向盛有 溶液的试管中滴加2滴
溶液的试管中滴加2滴 溶液,充分振荡后,
溶液,充分振荡后, ___________ (将操作补充完整)。
(2)实验现象:上述实验中,沉淀由白色变为___________ 色现象可证明 转化为
转化为 。
。
(3)分析及讨论
①该沉淀转化反应的离子方程式是___________ 。
②定量分析。由上述沉淀转化反应的化学平衡常数表达式可推导:
___________ (列式即可,不必计算结果)。
③同学们结合②中的分析方法,认为教材中的表述:“一般来说,溶解度小的沉淀转化为溶解度更小的沉淀容易实现”,可进一步表述为对于组成形式相同的沉淀,
___________ (填“小”或者“大”)的沉淀转化为
___________ (填“更小”或者“更大”)的沉淀容易实现。
Ⅱ、某同学设计如图实验装置研究 溶液和
溶液和 溶液间的反应(a、b均为石墨)。
溶液间的反应(a、b均为石墨)。
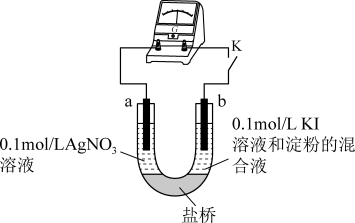
(4)当K闭合后,发现电流计指针偏转,b极附近溶液变蓝。
①b极发生的是___________ (填“氧化”或“还原”)反应。
②a极上的电极反应式是___________ 。
(5)事实证明: 溶液与
溶液与 的溶液混合只能得到
的溶液混合只能得到 沉淀,对比(4)中反应,从反应原理的角度解释产生该事实的可能原因是
沉淀,对比(4)中反应,从反应原理的角度解释产生该事实的可能原因是 与
与 之间发生沉淀反应比氧化还原反应的速率或限度
之间发生沉淀反应比氧化还原反应的速率或限度___________ (填“小”或者“大”)。
 转化为
转化为 。(已知:
。(已知: ,
, )
)(1)实验操作:所用试剂:
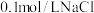 溶液,
溶液, 溶液,
溶液,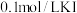 溶液;向盛有
溶液;向盛有 溶液的试管中滴加2滴
溶液的试管中滴加2滴 溶液,充分振荡后,
溶液,充分振荡后, (2)实验现象:上述实验中,沉淀由白色变为
 转化为
转化为 。
。(3)分析及讨论
①该沉淀转化反应的离子方程式是
②定量分析。由上述沉淀转化反应的化学平衡常数表达式可推导:

③同学们结合②中的分析方法,认为教材中的表述:“一般来说,溶解度小的沉淀转化为溶解度更小的沉淀容易实现”,可进一步表述为对于组成形式相同的沉淀,


Ⅱ、某同学设计如图实验装置研究
 溶液和
溶液和 溶液间的反应(a、b均为石墨)。
溶液间的反应(a、b均为石墨)。
(4)当K闭合后,发现电流计指针偏转,b极附近溶液变蓝。
①b极发生的是
②a极上的电极反应式是
(5)事实证明:
 溶液与
溶液与 的溶液混合只能得到
的溶液混合只能得到 沉淀,对比(4)中反应,从反应原理的角度解释产生该事实的可能原因是
沉淀,对比(4)中反应,从反应原理的角度解释产生该事实的可能原因是 与
与 之间发生沉淀反应比氧化还原反应的速率或限度
之间发生沉淀反应比氧化还原反应的速率或限度
您最近一年使用:0次
解题方法
4 . 实验室中,学生利用下图装置制作一个简单燃料电池。步骤如下:

①检验装置气密性后向U形管中注入适量的6 mol·L-1稀H2SO4溶液,至接近橡胶塞底部。
②接通学生电源K1,观察实验现象,当一端玻璃导管内的液柱接近溢出时,切断学生电源K1。
③将石英钟内的干电池取出,用导线与石英钟的正负极相连,接入装置中。接通学生电源K2,观察石英钟指针。
回答下列问题:
(1)接通学生电源K1,在右侧石墨棒表面观察到_______ 。
(2)观察到左侧的玻璃导管内的液柱先接近溢出,说明左侧石墨棒所连的是学生电源的_______ (填“正极”或“负极”),该石墨表面的电极方程式是_______ 。
(3)用导线与石英钟的正负极相连接入装置时,石英钟的正极应与_______ (填“左”或“右”)侧的石墨棒连接的导线相连。
(4)出现_______ 的现象,证明该燃料电池制作成功。燃料电池正极的电极方程式是_______ 。

①检验装置气密性后向U形管中注入适量的6 mol·L-1稀H2SO4溶液,至接近橡胶塞底部。
②接通学生电源K1,观察实验现象,当一端玻璃导管内的液柱接近溢出时,切断学生电源K1。
③将石英钟内的干电池取出,用导线与石英钟的正负极相连,接入装置中。接通学生电源K2,观察石英钟指针。
回答下列问题:
(1)接通学生电源K1,在右侧石墨棒表面观察到
(2)观察到左侧的玻璃导管内的液柱先接近溢出,说明左侧石墨棒所连的是学生电源的
(3)用导线与石英钟的正负极相连接入装置时,石英钟的正极应与
(4)出现
您最近一年使用:0次
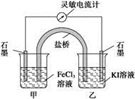
5 . 控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是
 2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是
| A.为证明反应的发生,可取甲中溶液加入铁氰化钾溶液 |
| B.反应开始时,甲中石墨电极上Fe3+被还原,乙中石墨电极上发生氧化反应 |
| C.电流计读数为零时,在甲中溶入FeCl2固体时,甲中的石墨电极为正极 |
| D.此反应正反应方向若为放热,电流计读数为零时,降低温度后乙中石墨电极为负极 |
您最近一年使用:0次
2018-03-01更新
|
263次组卷
|
2卷引用:天津市静海县第一中学2017-2018学年高二上学期期末终结性检测化学试题
名校
6 . 利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。T℃时反应
2SO2(g)+O2(g) 2SO3(g)过程中的能量变化如图所示,回答下列问题。
2SO3(g)过程中的能量变化如图所示,回答下列问题。
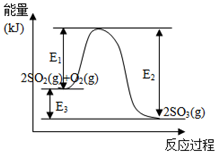
(1)T℃时将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。2min时反应达到平衡,此时测得反应物O2还剩余0.1mol,则达到平衡时SO2的转化率为_______ ,反应放出_____________ 热量。(用E1、E2或E3表示)
(2)下列叙述能证明该反应已达化学平衡状态的是__________________ (填序号)
①SO2的体积分数不再发生变化
②容器内压强不再发生变化
③容器内气体原子总数不再发生变化
④相同时间内消耗2n molSO2的同时生成n molO2
⑤相同时间内消耗2n molSO2的同时生成2n molSO3
(3)在反应体系中加入催化剂,反应速率增大, E3的变化是: E3____________ (填“增大”“减小”或“不变”)
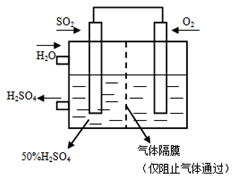
(4)若以下图所示装置,用电化学原理生产硫酸,将SO2、O2以一定压强喷到活性电极上反应。写出通SO2电极的电极反应式:______________ 。
(5) SOCl2是一种无色液体,可与碳共同构成锂电池的正极材料,且其放电时也有SO2气体产生。写出SOCl2在电池中放电时的电极反应式_________________ 。
2SO2(g)+O2(g)
 2SO3(g)过程中的能量变化如图所示,回答下列问题。
2SO3(g)过程中的能量变化如图所示,回答下列问题。
(1)T℃时将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。2min时反应达到平衡,此时测得反应物O2还剩余0.1mol,则达到平衡时SO2的转化率为
(2)下列叙述能证明该反应已达化学平衡状态的是
①SO2的体积分数不再发生变化
②容器内压强不再发生变化
③容器内气体原子总数不再发生变化
④相同时间内消耗2n molSO2的同时生成n molO2
⑤相同时间内消耗2n molSO2的同时生成2n molSO3
(3)在反应体系中加入催化剂,反应速率增大, E3的变化是: E3
(4)若以下图所示装置,用电化学原理生产硫酸,将SO2、O2以一定压强喷到活性电极上反应。写出通SO2电极的电极反应式:

(5) SOCl2是一种无色液体,可与碳共同构成锂电池的正极材料,且其放电时也有SO2气体产生。写出SOCl2在电池中放电时的电极反应式
您最近一年使用:0次
解题方法
7 . 天然气报警器可及时检测到空气中甲烷浓度的变化,当甲烷达到一定浓度时,传感器随之产生电信号并联动报警,其工作原理如图所示,下列说法错误的是
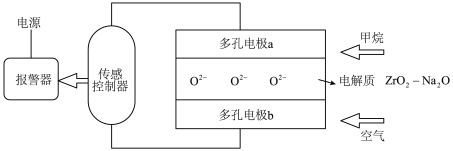
| A.报警器触发时,装置将化学能转化为电能 |
| B.多孔电极a为负极,电势低于多孔电极b |
| C.电流方向由多孔电极a经导线流向多孔电极b |
| D.当电极a有11.2mL甲烷(标况)参与反应时,电路中有0.004mol电子转移 |
您最近一年使用:0次
解题方法
8 . 一种电池装置如图所示,它能溶解辉铜矿石(主要成分是Cu2S)制得硫酸铜。下列说法不正确 的是
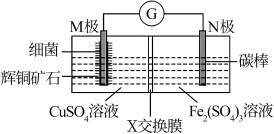
| A.N极为正极 |
| B.X交换膜为阴离子交换膜 |
C.M极产生的Cu2+和SO 的物质的量之比为2:1 的物质的量之比为2:1 |
| D.外电路上每通过2mol电子,左室溶液增重32g |
您最近一年使用:0次
名校
解题方法
9 . 下列有关说法中错误 的是(盐桥是浸满饱和 溶液的琼脂)
溶液的琼脂)
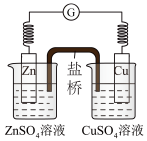
 溶液的琼脂)
溶液的琼脂)
| A.锌是负极,发生氧化反应 |
B.铜电极的电极反应式为: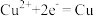 |
| C.电子经盐桥从锌电极流向铜电极 |
D.盐桥中 流向右侧烧杯 流向右侧烧杯 |
您最近一年使用:0次
名校
10 . 大气中过量的 和水体中过量的
和水体中过量的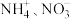 均是污染物。利用钒电池电解含
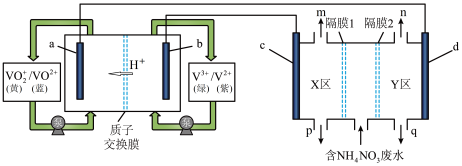
均是污染物。利用钒电池电解含 的废水制备硝酸和氨水的原理如下图所示,
的废水制备硝酸和氨水的原理如下图所示,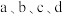 均为惰性电极。下列说法中正确的是
均为惰性电极。下列说法中正确的是
 和水体中过量的
和水体中过量的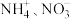 均是污染物。利用钒电池电解含
均是污染物。利用钒电池电解含 的废水制备硝酸和氨水的原理如下图所示,
的废水制备硝酸和氨水的原理如下图所示, 均为惰性电极。下列说法中正确的是
均为惰性电极。下列说法中正确的是
A.用钒电池处理废水时, 电极区溶液由绿色变成紫色 电极区溶液由绿色变成紫色 |
B. 为阴极, 为阴极, 为阳极 为阳极 |
| C.隔膜1为阴离子交换膜 |
D.当钒电池有 通过质子交换膜时,共处理含 通过质子交换膜时,共处理含 的废水 的废水 |
您最近一年使用:0次



