名校
解题方法
1 . 对右图所示的装置中实验现象的描述正确的是
| 选项 | a电极 | b电极 | X溶液 | 实验现象 | 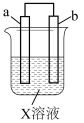 |
| A | 石墨 | 石墨 | CuCl2溶液 | a极质量增加,b极放出无色气体 | |
| B | Cu | Fe | KNO3溶液 | a极质量增加,b极放出无色气体 | |
| C | 石墨 | Fe |  溶液 溶液 | a极质量增加,b极质量减小 | |
| D | 石墨 | Zn | HCl溶液 | a放出无色气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是
| 装置 |  | 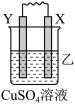 | 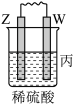 |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
| A.装置甲中X作原电池正极 |
| B.装置乙中Y电极上的反应式为Cu2++2e−=Cu |
| C.装置丙中溶液的c(H+)不变 |
| D.四种金属的活动性强弱顺序为Z>W>X>Y |
您最近一年使用:0次
2020-04-30更新
|
189次组卷
|
2卷引用:江西省上饶市2018-2019学年高一下学期期末教学质量测试化学试题
名校
解题方法
3 . 由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是
| 装置 | 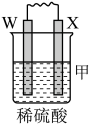 | 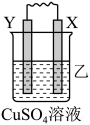 | 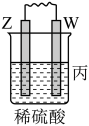 |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
| A.装置甲中X作原电池正极 |
| B.装置乙中Y电极上的反应式为Cu2++2e−=Cu |
| C.装置丙中溶液的c(H+)不变 |
| D.四种金属的活动性强弱顺序为Z>W>X>Y |
您最近一年使用:0次
2020-06-16更新
|
470次组卷
|
2卷引用:江西省南昌市第二中学2019-2020学年高一下学期第二次月考化学试题
解题方法
4 . 某同学设计实验探究构成原电池的条件,装置如图所示:
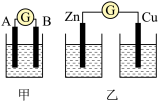
实验一:探究电极的构成。图甲中,①A、B两极均选用石墨作电极,发现电流计指针不偏转;②A、B两极均选用铜片作电极,发现电流计指针不偏转;③A极用锌片,B极用铜片,发现电流计指针向左偏转;④A极用锌片,B极用石墨,发现电流计指针向左偏转。
(1)结论一:________________________ ;
实验二:探究溶液的构成。图甲中,A极用锌片,B极用铜片,①液体采用无水乙醇,发现电流计指针不偏转;②改用硫酸溶液,发现电流计指针偏转,B极上有气体产生。
(2)结论二:________________________ ;
实验三:探究图乙装置能否构成原电池。将锌、铜两电极分别放入稀硫酸中,发现锌片上有气泡产生,铜片上无明显现象,电流计指针不发生偏转。
(3)结论三:________________________ ;
思考:对该同学的实验,有同学提出了如下疑问,请你帮助解决。
(4)在图甲装置中,若A为镁片,B为铝片,电解质溶液为 溶液;负极为
溶液;负极为________ (填“A”或“B”);电流计的指针应向________ (填“右”或“左”)偏转。

实验一:探究电极的构成。图甲中,①A、B两极均选用石墨作电极,发现电流计指针不偏转;②A、B两极均选用铜片作电极,发现电流计指针不偏转;③A极用锌片,B极用铜片,发现电流计指针向左偏转;④A极用锌片,B极用石墨,发现电流计指针向左偏转。
(1)结论一:
实验二:探究溶液的构成。图甲中,A极用锌片,B极用铜片,①液体采用无水乙醇,发现电流计指针不偏转;②改用硫酸溶液,发现电流计指针偏转,B极上有气体产生。
(2)结论二:
实验三:探究图乙装置能否构成原电池。将锌、铜两电极分别放入稀硫酸中,发现锌片上有气泡产生,铜片上无明显现象,电流计指针不发生偏转。
(3)结论三:
思考:对该同学的实验,有同学提出了如下疑问,请你帮助解决。
(4)在图甲装置中,若A为镁片,B为铝片,电解质溶液为
 溶液;负极为
溶液;负极为
您最近一年使用:0次
2020-04-07更新
|
454次组卷
|
3卷引用:课时1 化学能与电能的相互转化——A学习区 夯实基础(人教版必修2)
名校
解题方法
5 . 在下图所示的装置中,试管A、B中的电极为多孔的惰性电极;C、D为两个铂夹,夹在被Na2SO4溶液浸湿的滤纸条上,滤纸条的中部滴有一滴KMnO4;电源有a、b两极。若在A、B中充满0.01 mol/L 的KOH溶液后倒立于同浓度的KOH溶液的水槽中,断开K1,闭合K2、K3,通直流电,实验现象如下图所示,则:
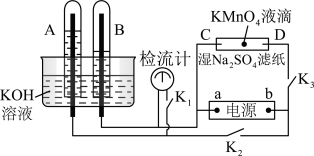
(1)断开K1,闭合K2、K3,通直流电,试管B中产生的气体为_________ (填化学式)。
(2)在Na2SO4溶液浸湿的滤纸条中部的KMnO4处现象为_____________ 。
(3)断开K1,闭合K2、K3,通直流电较长一段时间后,KOH溶液pH变__________ (填“变大”“变小”或“不变”)。
(4)电解一段时间后,A、B中均有气体包围电极。此时切断K2、K3,闭合K1,检流计有指数,此时该装置A试管中电极上发生的反应为_____________

(1)断开K1,闭合K2、K3,通直流电,试管B中产生的气体为
(2)在Na2SO4溶液浸湿的滤纸条中部的KMnO4处现象为
(3)断开K1,闭合K2、K3,通直流电较长一段时间后,KOH溶液pH变
(4)电解一段时间后,A、B中均有气体包围电极。此时切断K2、K3,闭合K1,检流计有指数,此时该装置A试管中电极上发生的反应为
您最近一年使用:0次
2019-11-20更新
|
157次组卷
|
2卷引用:山东省师范大学附属中学2019-2020学年高二上学期第五次学分认定考试化学试题
名校
解题方法
6 . 某化学小组的同学为探究原电池原理,设计如图所示装置,将锌、铜通过导线相连,置于稀硫酸中
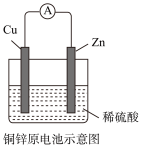
(1)外电路,电子从__________ 极流出。溶液中,阳离子向_______ 极移动。
(2)锌为____ 极,电极上发生的_______________ 反应(“氧化”或“还原”),电极反应式_______________ 锌片上观察到的现象为_____________________ ;铜为__________ 极,电极上发生的是_______________ 反应(“氧化”或“还原”), 电极反应式____________________________________ ,铜片上观察到现象的为__________
(3)若反应过程中有0.2 mol电子发生转移,则生成的气体在标准状况下的体积为______________ 。
(4)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是_____ (填序号)。
A.无水乙醇 B.醋酸溶液 C.CuSO4溶液 D.苯
(5)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是____________ (填字母代号)。
A. NaOH+HCl=NaCl+H2O B. 2H2+O2=2H2O
C. Fe+2FeCl3=3FeCl2 D. 2H2O=2H2↑+O2↑

(1)外电路,电子从
(2)锌为
(3)若反应过程中有0.2 mol电子发生转移,则生成的气体在标准状况下的体积为
(4)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是
A.无水乙醇 B.醋酸溶液 C.CuSO4溶液 D.苯
(5)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是
A. NaOH+HCl=NaCl+H2O B. 2H2+O2=2H2O
C. Fe+2FeCl3=3FeCl2 D. 2H2O=2H2↑+O2↑
您最近一年使用:0次
名校
7 . Ⅰ.(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流表。原电池工作时电子是从_____ 到______ (填锌片或银片),锌片电极上发生的是_______________ 反应(“氧化”或“还原”)。电极反应式为_________________________________ ,锌片上观察到的现象为___________
(2)银片上发生的是____________ 反应(“氧化”或“还原”),电极反应式是__________ ,银片上观察到的现象是______________________ 溶液中的C(H+)____________ (填“增大”或“减小”)。
(3)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:产生氢气的体积为________ L(标准状况);导线中通过的电子数为______ 。
Ⅱ.根据反应:CuCl2 + Fe= FeCl2 + Cu 设计原电池:
(1)在该原电池中,以__________ (写名称)为电解质溶液,铁为______ 极,电极反应式为_______ ,
(2)在该原电池中,选__________ (写名称)作正极,电极反应式是__________________________
(3)画出装置图,标出正、负极材料及电解质溶液名称____________________ 。
(2)银片上发生的是
(3)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:产生氢气的体积为
Ⅱ.根据反应:CuCl2 + Fe= FeCl2 + Cu 设计原电池:
(1)在该原电池中,以
(2)在该原电池中,选
(3)画出装置图,标出正、负极材料及电解质溶液名称
您最近一年使用:0次
名校
解题方法
8 . (1)我国是世界上最早使用湿法炼铜的国家。湿法炼铜的原理是Fe+CuSO4=FeSO4+Cu,其中铁被__________ (填“氧化”或“还原”),CuSO4作________ (填“氧化”或“还原”)剂。在该反应中,若生成了1 mol Cu,消耗Fe的物质的量是_________ 。
(2)某学习小组设计下图所示装置观察氧化还原反应中电子的转移。
①实验Ⅰ中,Fe与CuSO4溶液反应的离子方程式是______________ 。
②根据实验Ⅰ的原理,推测实验Ⅱ中:锌片上发生_________ (填“氧化”或“还原”)反应;铜片上的实验现象是__________ 。
(2)某学习小组设计下图所示装置观察氧化还原反应中电子的转移。
| 实验Ⅰ | 实验Ⅱ | |
| 装置 | 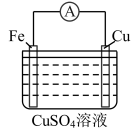 | 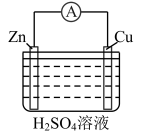 |
| 现象 | 电流计指针向右偏转;铁片溶解; 铜片上有红色物质(铜)析出,铜片质量增加 | 电流计指针向右偏转;…… |
①实验Ⅰ中,Fe与CuSO4溶液反应的离子方程式是
②根据实验Ⅰ的原理,推测实验Ⅱ中:锌片上发生
您最近一年使用:0次
名校
9 . 某同学做了如下实验:
下列说法中不正确的是
| 装置 | 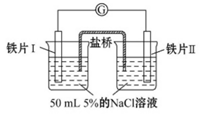 |  |
| 现象 | 电流计指针未发生偏转 | 电流计指针发生偏转 |
| A.往铁片Ⅰ所在烧杯加入蒸馏水,电流表指针会发生偏转 |
| B.用K3[Fe(CN)3]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断电池的正、负极 |
| C.铁片Ⅰ、Ⅲ的腐蚀速率不相等 |
| D.“电流计指针未发生偏转”,铁片Ⅰ、铁片Ⅱ均未被腐蚀 |
您最近一年使用:0次
10 . (1)下列装置属于原电池的是___________ ;
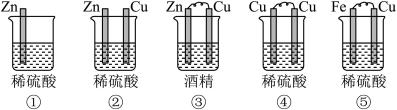
(2)在选出的原电池中,______ 是负极,发生______ (氧化、还原) 反应 ,______ 是正极 ,该极的现象___________________________ ;
(3)在该原电池的内电路中,硫酸根离子移向_________ (正、负)极。
(4)此原电池反应的化学方程式为___________________________ 。

(2)在选出的原电池中,
(3)在该原电池的内电路中,硫酸根离子移向
(4)此原电池反应的化学方程式为
您最近一年使用:0次



