名校
解题方法
1 . 下列说法中正确的是
A.一定温度下,向体积不变的反应体系 中通入CO2,平衡后 中通入CO2,平衡后 增大 增大 |
| B.常温常压下能发生自发反应的两种物质,在常温常压下一定不能大量共存 |
C.金属的化学腐蚀实质是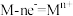 ,电子直接转移给氧化剂 ,电子直接转移给氧化剂 |
D.在KMnO4酸性溶液做电解质的原电池中, 一定向负极移动 一定向负极移动 |
您最近一年使用:0次
解题方法
2 . 已知在1×105Pa,298 K时断裂1 mol H—H键吸收的能量为436kJ ,断裂l mol N—H键吸收的能量为391kJ,断裂1 mol N≡N键吸收的能量是945kJ。
(1)根据以上数据判断工业合成氨的反应N2(g)+3H2(g) 2NH3(g)是
2NH3(g)是________ (填“吸热”或“放热”)反应。该反应的能量变化可用图______ 表示(填"甲”或”乙“)。
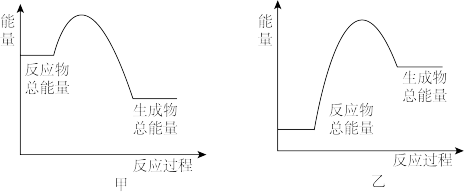
(2)H2还原CO电化学法制备甲醇(CO +2H2 CH3OH)的工作原理如图所示。
CH3OH)的工作原理如图所示。

①通入H2的一端是电池的____ 极(填”正”或“负”),电池工作过程中H+通过质子交换膜向______ (填”左”或"右”)移动,通入CO的一端发生的电极反应为_______ 。
②若电池中氢气(H2)通入量为224 mL(标准状况),且反应完全,则理论上通过电流表的电量为______ C(法拉第常数F=9.65×104C/mol)。
(1)根据以上数据判断工业合成氨的反应N2(g)+3H2(g)
 2NH3(g)是
2NH3(g)是
(2)H2还原CO电化学法制备甲醇(CO +2H2
 CH3OH)的工作原理如图所示。
CH3OH)的工作原理如图所示。
①通入H2的一端是电池的
②若电池中氢气(H2)通入量为224 mL(标准状况),且反应完全,则理论上通过电流表的电量为
您最近一年使用:0次
名校
解题方法
3 . 根据下图,下列判断中正确的是( )
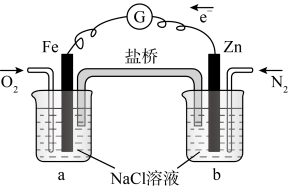

| A.向烧杯a中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀生成 |
| B.烧杯a中发生反应O2+4H++4e-=2H2O,溶液pH降低 |
| C.电子从Zn极流出,流入Fe极,经盐桥回到Zn极 |
| D.烧杯b中发生反应为Zn-2e-=Zn2+ |
您最近一年使用:0次
2016-06-30更新
|
274次组卷
|
3卷引用:河南省安阳市第一中学2023届高三第四次全真模拟化学试题
解题方法
4 . 原电池原理广泛应用于科技、生产和生活中。
(1)一种处理垃圾渗透液并用其发电的装置工作示意图如下。

①在空气中,微生物将垃圾渗透液硝化,该反应的离子方程式为___________ 。
②Y电极的电极反应式为___________ 。
③盐桥中 移向
移向___________ (填“X或Y”)极;当转移0.15mol电子时,生成标准状况下 的体积为
的体积为___________ L。
(2)用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。
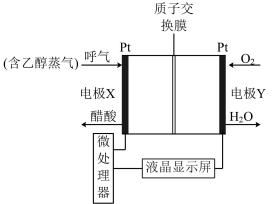
①电极X是该电池的___________ (填“正”或“负”)极,电池总反应式为___________ 。
②电池工作时,质子通过交换膜___________ (填“从左向右”或“从右向左”)迁移。
(1)一种处理垃圾渗透液并用其发电的装置工作示意图如下。

①在空气中,微生物将垃圾渗透液硝化,该反应的离子方程式为
②Y电极的电极反应式为
③盐桥中
 移向
移向 的体积为
的体积为(2)用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。

①电极X是该电池的
②电池工作时,质子通过交换膜
您最近一年使用:0次
名校
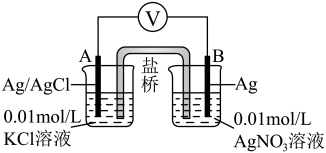
5 . 根据溶液中相关离子浓度对电池电动势产生的影响,通过设计原电池,可间接测量难溶电解质的溶度积常数 .某研究小组设计了如下图所示的原电池装置,已知该电池的电动势
.某研究小组设计了如下图所示的原电池装置,已知该电池的电动势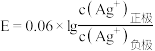 ,测得实验开始时
,测得实验开始时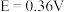 。下列说法正确的是
。下列说法正确的是
 .某研究小组设计了如下图所示的原电池装置,已知该电池的电动势
.某研究小组设计了如下图所示的原电池装置,已知该电池的电动势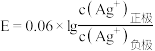 ,测得实验开始时
,测得实验开始时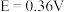 。下列说法正确的是
。下列说法正确的是
A.电流方向为 |
B.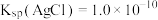 |
C. 极电极反应为 极电极反应为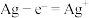 |
| D.随着反应进行,该电池的电动势会逐渐增大 |
您最近一年使用:0次
解题方法
6 . 原电池工作原理:电源是将___________ 能转化为___________ 能的实用装置。发生氧化反应的一极为___________ ,发生还原反应的一极为___________ ;电子流向:___________ →___________ ;电流流向:___________ →___________ ;离子流向:阳离子→___________ ,阴离子→___________ 。
您最近一年使用:0次



