1 . 无水氯化铝是有机化工中常用的催化剂,178℃时升华,极易潮解。某化学兴趣小组设计了下列实验。根据所学知识,回答下列问题:
【实验1】利用置换反应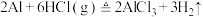 制备少量无水氯化铝,实验装置如图。
制备少量无水氯化铝,实验装置如图。
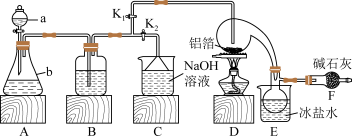
(1)a中盛放浓硫酸,b中盛放浓盐酸。将a中液体逐滴加入b中。B装置中的试剂为_______ 。
(2)实验时,检验装置气密性后,向D装置的曲颈瓶中加入铝箔,连接好装置,接下来对 、
、 进行的操作是
进行的操作是_______ ,然后加热D装置。
(3)F中干燥管内碱石灰的作用是_______ 。
【实验2】利用原电池反应检测金属的活动性顺序,甲、乙两组均使用镁片和铝片作电极,但甲组将电极放入 的硫酸中,乙组将电极放入
的硫酸中,乙组将电极放入 的氢氧化钠溶液中,装置如图所示。
的氢氧化钠溶液中,装置如图所示。
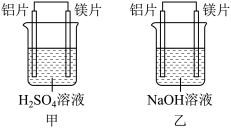
(4)写出甲电池中正极的电极反应式:_______ 。在标准状况下,正极产生 气体,得
气体,得_______ mol电子。
(5)乙电池中负极为_______ ,总反应的离子方程式为_______ 。
(6)由此实验,可得到的正确结论有_______(填标号)。
【实验1】利用置换反应
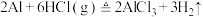 制备少量无水氯化铝,实验装置如图。
制备少量无水氯化铝,实验装置如图。
(1)a中盛放浓硫酸,b中盛放浓盐酸。将a中液体逐滴加入b中。B装置中的试剂为
(2)实验时,检验装置气密性后,向D装置的曲颈瓶中加入铝箔,连接好装置,接下来对
 、
、 进行的操作是
进行的操作是(3)F中干燥管内碱石灰的作用是
【实验2】利用原电池反应检测金属的活动性顺序,甲、乙两组均使用镁片和铝片作电极,但甲组将电极放入
 的硫酸中,乙组将电极放入
的硫酸中,乙组将电极放入 的氢氧化钠溶液中,装置如图所示。
的氢氧化钠溶液中,装置如图所示。
(4)写出甲电池中正极的电极反应式:
 气体,得
气体,得(5)乙电池中负极为
(6)由此实验,可得到的正确结论有_______(填标号)。
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属活动性不一定比铝的强 |
| C.该实验说明金属活动性顺序表已过时,已没有利用价值 |
| D.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析 |
您最近一年使用:0次
名校
解题方法
2 . 盐酸羟胺(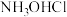 )是一种常见的还原剂和显像剂,其化学性质类似
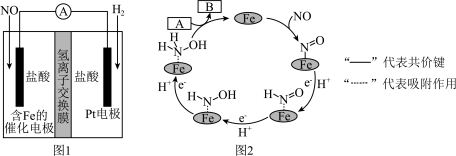
)是一种常见的还原剂和显像剂,其化学性质类似 。工业上主要采用图1所示的方法制备。电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
。工业上主要采用图1所示的方法制备。电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
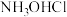 )是一种常见的还原剂和显像剂,其化学性质类似
)是一种常见的还原剂和显像剂,其化学性质类似 。工业上主要采用图1所示的方法制备。电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
。工业上主要采用图1所示的方法制备。电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
| A.电池工作时,Pt电极作正极 |
B.图2中,A为 和 和 ,B为 ,B为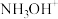 |
| C.电池工作时,每消耗2.24LNO(标准状况下),左室溶液质量增加3.3g |
D.Pt电极发生的电极方程式为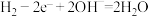 |
您最近一年使用:0次
3 . 锌铜——稀硫酸原电池的装置如图所示,下列叙述错误的是
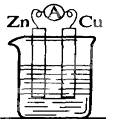

| A.电流从锌片经导线流向铜片 | B.锌是负极,其质量逐渐减小 |
| C.氢离子在铜表面被还原,产生气泡 | D.依据该实验现象可判断锌比铜活泼 |
您最近一年使用:0次
2018-07-04更新
|
114次组卷
|
2卷引用:新疆皮山县高级中学2022-2023学年高一下学期4月期中考试化学试题
名校
4 . 浓差电池是一种利用电解质溶液浓度差产生电势差而形成的电池,理论上当电解质溶液的浓度相等时停止放电。图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电池为电源完成电渗析法制备磷酸二氢钠。下列说法正确的是
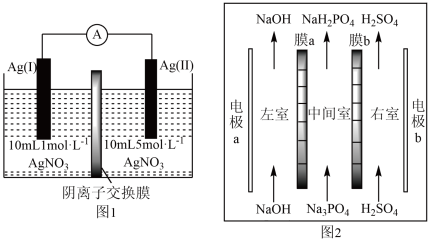
| A.电极Ag(II)的电极反应式为:Ag-e-=Ag+ |
| B.电渗析装置中膜a、b均为阳离子交换膜 |
| C.电渗析过程中左室中NaOH浓度增大,右室H2SO4的浓度减小 |
| D.电池从开始到停止放电,理论上可制备2.4gNaH2PO4 |
您最近一年使用:0次
2024-03-11更新
|
273次组卷
|
2卷引用:四川省成都外国语学校2023-2024学年高三上学期期末考试理科综合试题-高中化学
名校
5 . 浓差电池是一种利用电解质溶液浓度差产生电势差而形成的电池,理论上当电解质溶液的浓度相等时停止放电。图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电池为电源完成电渗析法制备磷酸二氢钠。下列说法错误的是
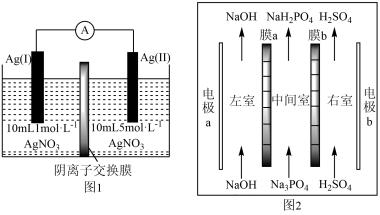

| A.电极a应与Ag(I)相连 |
| B.电渗析装置中膜a为阳离子交换膜 |
C.电渗析过程中左、右室中NaOH和 的浓度均增大 的浓度均增大 |
D.电池从开始到停止放电,理论上可制备2.4g |
您最近一年使用:0次
2024-01-13更新
|
641次组卷
|
4卷引用:陕西省渭南市2023-2024学年高三上学期教学质量检测化学试卷
陕西省渭南市2023-2024学年高三上学期教学质量检测化学试卷 陕西省渭南市2023-2024学年高三教学质量检测(Ⅰ)化学试题 四川省成都市第七中学2023-2024学年高三上学期期末考试理科综合试卷-高中化学(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
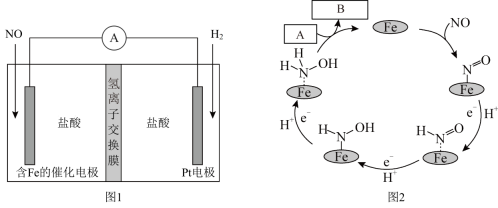
6 . 盐酸羟胺(化学式为NH3OHCl,其中N为 价)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用如图1所示的方法制备,其电池装置中含Fe的催化电极的电极反应机理如图2所示。下列说法错误的是
价)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用如图1所示的方法制备,其电池装置中含Fe的催化电极的电极反应机理如图2所示。下列说法错误的是
 价)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用如图1所示的方法制备,其电池装置中含Fe的催化电极的电极反应机理如图2所示。下列说法错误的是
价)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用如图1所示的方法制备,其电池装置中含Fe的催化电极的电极反应机理如图2所示。下列说法错误的是
| A.含Fe的催化电极为正极 |
| B.图2中,A为H+,B为NH3OH+ |
| C.电池工作时,每消耗2.24L NO(标准状况下),左室溶液质量增加3.0g |
| D.电池工作时,H+从右室穿过氢离子交换膜向左室迁移 |
您最近一年使用:0次
名校
解题方法
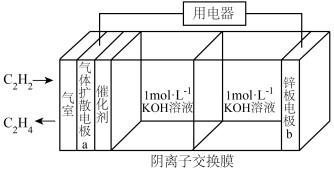
7 . 乙炔制乙烯是煤化工路线的重要途径之一,如图是利用电化学装置制备 的工作原理示意图,下列说法正确的是
的工作原理示意图,下列说法正确的是
 的工作原理示意图,下列说法正确的是
的工作原理示意图,下列说法正确的是
| A.电极电势:a极<b极 |
| B.电子移动方向:电极b→用电器→电极a→KOH溶液→电极b |
C.电极a上的电极反应式为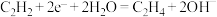 |
| D.放电一段时间后,正极室溶液pH不会发生变化 |
您最近一年使用:0次
2024-01-31更新
|
106次组卷
|
2卷引用:河南省安阳市汤阴一中2023-2024学年高三上学期12月阶段检测化学试题
2023高三上·全国·专题练习
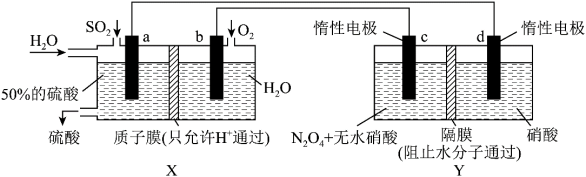
8 . 膜技术原理在化工生产中有着广泛的应用。有人设想利用电化学原理制备少量硫酸和绿色硝化剂 ,装置图如下。下列说法不正确的是
,装置图如下。下列说法不正确的是
 ,装置图如下。下列说法不正确的是
,装置图如下。下列说法不正确的是
A. 是原电池 是原电池 |
B. 池能够生产 池能够生产 |
C.电路中电子流向为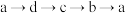 ,形成闭合回路 ,形成闭合回路 |
D. 、 、 中 中 均从左边迁移到右边 均从左边迁移到右边 |
您最近一年使用:0次
名校
解题方法
9 . 根据下列要求回答问题。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
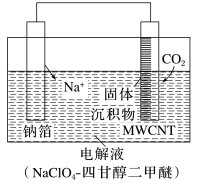
①放电时,正极的电极反应式为___________ 。
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为___________ 。
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是___________ 。
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
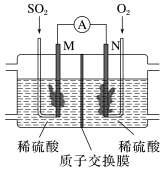
①M极发生的电极反应式为___________ 。
②质子交换膜右侧的溶液在反应后pH___________ (填“增大”“减小”或“不变”)。
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量___________ (填“增大”或“减小”)___________ g。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2
 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
①放电时,正极的电极反应式为
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。

①M极发生的电极反应式为
②质子交换膜右侧的溶液在反应后pH
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量
您最近一年使用:0次
名校
解题方法
10 . 甲烷燃料电池采用铂为电极,作为化学电源进行电解实验

(1)写出燃料电池的正、负极反应式:
负极:___________ ,正极:___________ 。
(2)已知A中两个电极的材料分别为石墨和铁,用该装置可以制备高铁酸钾 。资料显示:
。资料显示: 在溶液中呈紫红色。闭合K,一段时间后,发现A中某电极附近溶液变成紫红色,该电极是
在溶液中呈紫红色。闭合K,一段时间后,发现A中某电极附近溶液变成紫红色,该电极是___________ (填a或b),该电极的电极反应式为:___________ 。
(3)若B中的溶液为饱和 溶液,用该装置模拟氯碱工业。
溶液,用该装置模拟氯碱工业。
①检验C电极产物的方法是:___________ 。
②写出d电极的电极反应式:___________ 。
(4)若用B装置模拟工业粗铜精炼,则c极为___________ ;当燃料电池消耗标准状况下 的体积为
的体积为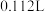 时,理论上可以得到纯铜
时,理论上可以得到纯铜___________ g。

(1)写出燃料电池的正、负极反应式:
负极:
(2)已知A中两个电极的材料分别为石墨和铁,用该装置可以制备高铁酸钾
 。资料显示:
。资料显示: 在溶液中呈紫红色。闭合K,一段时间后,发现A中某电极附近溶液变成紫红色,该电极是
在溶液中呈紫红色。闭合K,一段时间后,发现A中某电极附近溶液变成紫红色,该电极是(3)若B中的溶液为饱和
 溶液,用该装置模拟氯碱工业。
溶液,用该装置模拟氯碱工业。①检验C电极产物的方法是:
②写出d电极的电极反应式:
(4)若用B装置模拟工业粗铜精炼,则c极为
 的体积为
的体积为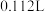 时,理论上可以得到纯铜
时,理论上可以得到纯铜
您最近一年使用:0次



