名校
解题方法
1 . 有X、Y、Z、M四种金属,按如下装置进行实验,实验现象如表中。
下列说法不正确的是
| 装置 | 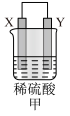 |  | 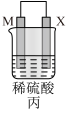 |
| 现象 | 金属X不断溶解 | Z的质量增加 | X上有气体产生 |
| A.装置甲中电子从X极流出,经外电路流入Y极 |
B.装置乙的正极反应式为: |
| C.装置丙溶液中阳离子往M极移动 |
| D.四种金属活动性由强到弱的顺序是:M>X>Y>Z |
您最近一年使用:0次
2023-07-05更新
|
168次组卷
|
2卷引用:四川省眉山市2022-2023学年高一下学期期末考试化学试题
2 . 下列有关实验操作、现象和所得结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向2mL0.1mol/LNaCl溶液中加入过量的 溶液后,再加1mL0.1mol/LNaI,出现黄色沉淀。 溶液后,再加1mL0.1mol/LNaI,出现黄色沉淀。 | Ksp(AgCl)>Ksp(AgI) |
| B | 将镁片和铝片用导线连接后插入NaOH溶液中,镁片表面产生气泡 | 该装置构成了原电池,铝片做负极。 |
| C | 向某溶液中加入稀NaOH溶液,用湿润的红色石蕊试纸检验,无明显现象 | 溶液中一定无 |
| D | 向 溶液中通入 溶液中通入 和X气体,产生白色沉淀 和X气体,产生白色沉淀 | 气体X一定具有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 某化学兴趣小组欲探究a,b,c,d四种金属的活动性大小顺序,利用实验室现有材料和试剂进行实验,组装了如图所示的装置(电流表指针偏向正极,电解质溶液足量)。请回答下列问题:
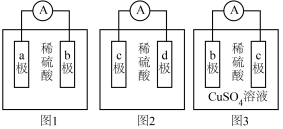
(1)观察到图1装置中的电流表指针偏向b极,说明a极为______ (填“正极”或“负极”),b极上发生的电极反应为______ 。
(2)观察到图2装置中的c极上有气泡生成,可观察到d极上的现象为______ 。
(3)图3装置中的电流表指针偏向c极,若b极为Fe电极,则b极上发生的电极反应为______ ,当该电路中转移0.4mole-时,______ (填“b”或“c”)极质量增重______ g。
(4)通过以上实验装置______ (填“能”或“不能”)比较出四种金属的活动性大小顺序,理由是______ 。

(1)观察到图1装置中的电流表指针偏向b极,说明a极为
(2)观察到图2装置中的c极上有气泡生成,可观察到d极上的现象为
(3)图3装置中的电流表指针偏向c极,若b极为Fe电极,则b极上发生的电极反应为
(4)通过以上实验装置
您最近一年使用:0次
4 . A、B、C、D四种金属按下表中装置进行实验,下列说法不正确的是
装置 | 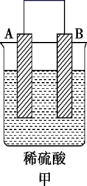 | 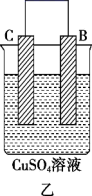 | 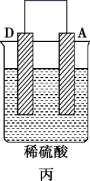 |
现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
| A.装置甲溶液中的阴离子移向B极 |
B.装置乙中C极的电极反应式为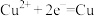 |
| C.装置丙中电流由A→导线→D→电解质溶液→A |
| D.四种金属活动性由强到弱的顺序是D>A>B>C |
您最近一年使用:0次
名校
5 . I.如图是利用电化学装置将SO2转化为重要的化工原料H2SO4的原理示意图。
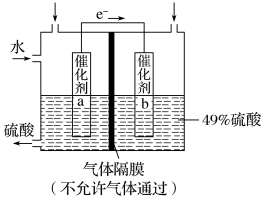
请回答下列问题:
(1)该装置将_______ 能转化为______ 能。
(2)催化剂b表面O2发生_______ 反应,其附近溶液酸性______ (填“增强”、“不变”或“减弱”)。
(3)催化剂a表面的电极反应式:_______ 。
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是______ 。
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是______ 。
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由______ 。
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为______ 。

请回答下列问题:
(1)该装置将
(2)催化剂b表面O2发生
(3)催化剂a表面的电极反应式:
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为
您最近一年使用:0次
2023-05-19更新
|
714次组卷
|
2卷引用:贵州省遵义市仁怀市高中教育联盟2022-2023学年高一下学期5月期中考试化学试题
名校
解题方法
6 . 化学反应与能量变化对人类生产、生活有重要的意义。回答下列问题:
(1)用A、B、C、D四种金属按如表所示的装置进行实验。
①装置甲中负极为___________ (填“A”或“B”)。
②装置乙中正极的电极反应式为___________ 。
③装置丙中溶液的pH___________ (填“变大”“变小”或“不变”)。
④四种金属的活动性由强到弱的顺序是___________ 。
(2)北京冬奥会基本实现100%绿电供应和碳中和,利用CO2和H2在光催化酶作用下可以高效合成甲醇(CH3OH)。
①写出甲醇燃烧的化学方程式:___________ 。
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:
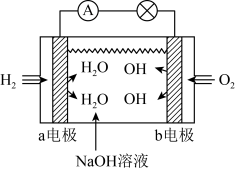
a电极是___________ 极,此时b电极发生反应的电极反应式是___________ , 向
向___________ (填“a”或“b”)电极移动。
(1)用A、B、C、D四种金属按如表所示的装置进行实验。
| 装置 | 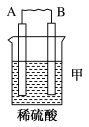 | 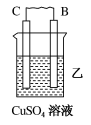 | 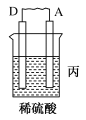 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(2)北京冬奥会基本实现100%绿电供应和碳中和,利用CO2和H2在光催化酶作用下可以高效合成甲醇(CH3OH)。
①写出甲醇燃烧的化学方程式:
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:

a电极是
 向
向
您最近一年使用:0次
名校
7 . 完成下列问题。
(1)下列反应中,属于放热反应的是___________ (填字母,下同),属于吸热反应的是___________ 。
a.盐酸与烧碱溶液反应 b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.葡萄糖在人体内氧化分解
(2)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。
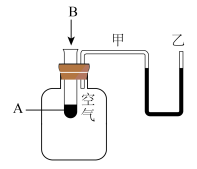
试回答下列问题:
①该反应为___________ 反应(填“放热”或“吸热”)。
②该反应的反应物化学键断裂吸收的能量________ (填“高”或“低”)于生成物化学键形成放出的能量。
(3) A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲溶液中的阴离子移向________ (填“A”或“B”)极。
②装置乙中正极的电极反应式为________ 。
③四种金属活动性由强到弱的顺序是________ 。
(4)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如下图所示:
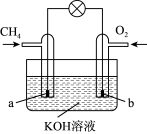
①外电路电子移动方向:___________ (填“a极到b极”或“b极到a极”)。
②a电极的电极方程式为___________ 。
(1)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应 b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.葡萄糖在人体内氧化分解
(2)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。

试回答下列问题:
①该反应为
②该反应的反应物化学键断裂吸收的能量
(3) A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 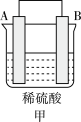 |  |  |
| 现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲溶液中的阴离子移向
②装置乙中正极的电极反应式为
③四种金属活动性由强到弱的顺序是
(4)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如下图所示:

①外电路电子移动方向:
②a电极的电极方程式为
您最近一年使用:0次
8 . 能源是现代文明的原动力,电池与我们的生活和生产密切相关。
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的_____(填字母)。
(2)下图为原电池装置示意图:
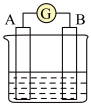
①若A为 片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:
片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:_____ ,反应过程中溶液的酸性_____ (填“增强”、“减弱”或“不变”)。一段时间后,当电池中放出2.24L(标准状况)气体时,电路中有_____ 个电子通过了导线(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
②若A为镁片,B为铝片,电解质为 溶液,则铝片为
溶液,则铝片为_____ (填“正极”或“负极”);写出该电极的电极反应式:_____ 。
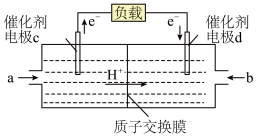
(3)燃料电池是一种具有应用前景的绿色电源, 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是_____ (填“正极”或“负极”),则该燃料电池如下:
(4)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的_____(填字母)。
A. |
B.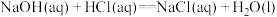 |
C.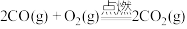 |
D.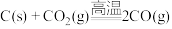 |

①若A为
 片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式:
片,B为石墨棒,电解质溶液为稀硫酸,写出负极的电极反应式: 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。②若A为镁片,B为铝片,电解质为
 溶液,则铝片为
溶液,则铝片为(3)燃料电池是一种具有应用前景的绿色电源,
 和
和 组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许
组合形成的燃料电池的结构如图(电解质溶液是稀硫酸,质子交换膜只允许 通过)。则电极d是
通过)。则电极d是
(4)为证明铁的金属活动性比铜强,某同学设计了如下一些方案。其中能证明铁的金属活动性比铜强的方案是
| 方案 | 现象或产物 |
A.将铁片置于 溶液中 溶液中 | 铁片上有亮红色物质析出 |
| B.将铁丝和铜丝分别在氯气燃烧 | 产物分别为 和 和 |
| C.将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡产生,铜片上无气泡产生 |
| D.将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连 | 铁片溶解,铜片上有气泡产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 某科学探究小组为探究电化学原理,设计了如图所示的装置进行探究实验。下列对实验中观察到的现象或相关结论的叙述不正确的是
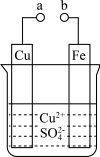
| A.a和b不连接时,铁片上有红色的铜析出,该装置不能形成原电池 |
| B.a和b用导线连接时,铜片为正极 |
C.无论a和b是否连接,反应的本质相同,铁片均会被氧化,溶液中均有 生成 生成 |
D.a和b用导线连接时,溶液中的 应向铁电极移动且能更快地析出铜 应向铁电极移动且能更快地析出铜 |
您最近一年使用:0次
2023-04-18更新
|
256次组卷
|
2卷引用:湖北省武汉市重点中学5G联合体2022-2023学年高一下学期期中考试化学试题
名校
解题方法
10 . 由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是
| 装置 | 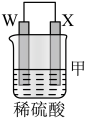 | 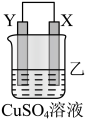 | 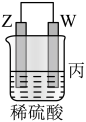 |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
| A.装置甲中W作原电池负极 |
| B.装置乙中Y电极上的反应式为Cu2++2e-=Cu |
| C.装置丙溶液中电子由Z流向W |
| D.四种金属的活动性强弱顺序为Z>W>X>Y |
您最近一年使用:0次
2023-04-11更新
|
750次组卷
|
2卷引用:黑龙江省齐齐哈尔市第八中学校2022-2023学年高一下学期3月月考化学试题



