名校
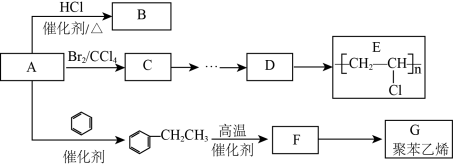
1 . Ⅰ.有机化合物A(相对分子质量为28)是重要的有机化工基础原料,其产量被用作衡量一个国家石油化工产业发展水平的标志。A与其他化合物之间的转化关系如图所示,回答下列问题。________________ 。
(2)上图中的 也可由B与
也可由B与 在
在 作催化剂的条件下合成,反应的化学方程式是
作催化剂的条件下合成,反应的化学方程式是_______________ ,反应类型是_______________ 。
Ⅱ.回答下列问题
(3)CO与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如下:
组合形成的质子交换膜燃料电池的结构示意图如下:__________________ 。若线路中转移2mol电子,则上述 燃料电池,消耗的
燃料电池,消耗的 在标准状况下的体积为
在标准状况下的体积为__________ L。
(4)2023年12月丰城顺利通过了创文明城的验收,文明驾驶就是其中的一条。一种基于碱性燃料电池原理设计的酒精检测仪,负极上的反应为______________________ 。
(2)上图中的
 也可由B与
也可由B与 在
在 作催化剂的条件下合成,反应的化学方程式是
作催化剂的条件下合成,反应的化学方程式是Ⅱ.回答下列问题
(3)CO与
 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如下:
组合形成的质子交换膜燃料电池的结构示意图如下:
 燃料电池,消耗的
燃料电池,消耗的 在标准状况下的体积为
在标准状况下的体积为(4)2023年12月丰城顺利通过了创文明城的验收,文明驾驶就是其中的一条。一种基于碱性燃料电池原理设计的酒精检测仪,负极上的反应为
您最近一年使用:0次
名校
解题方法
2 . 化学实验是科学研究中的重要方法。
(1)用A、B、C、D四种金属按如表所示的装置进行实验。
根据实验现象回答下列问题:
①装置甲中电流的流动方向为:沿导线___________ (请填写“从A流向B”或“从B流向A”)。
②四种金属的活动性由强到弱的顺序是___________ 。
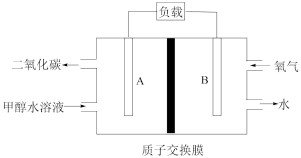
(2)将甲醇( )设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得
)设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得 定向移向A电极,则
定向移向A电极,则___________ (填A或B)处电极入口通 。
。___________ 。
②当消耗3.2g甲醇时,消耗氧气的体积为___________ L(标准状况下)。
(3)常温下,将除去表面氧化膜的铝片、铜片插入浓 中组成原电池装置(如图甲),测得原电池的电流强度(Ι)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。
中组成原电池装置(如图甲),测得原电池的电流强度(Ι)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。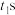 前,原电池的负极是
前,原电池的负极是___________ , 后,外电路中电子流动方向发生改变,原因是
后,外电路中电子流动方向发生改变,原因是___________ 。
(1)用A、B、C、D四种金属按如表所示的装置进行实验。
| 甲 | 乙 | 丙 | |
| 装置 |
|
 溶液 溶液 |
|
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中电流的流动方向为:沿导线
②四种金属的活动性由强到弱的顺序是
(2)将甲醇(
 )设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得
)设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。实验测得 定向移向A电极,则
定向移向A电极,则 。
。
②当消耗3.2g甲醇时,消耗氧气的体积为
(3)常温下,将除去表面氧化膜的铝片、铜片插入浓
 中组成原电池装置(如图甲),测得原电池的电流强度(Ι)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。
中组成原电池装置(如图甲),测得原电池的电流强度(Ι)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。
 前,原电池的负极是
前,原电池的负极是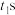 后,外电路中电子流动方向发生改变,原因是
后,外电路中电子流动方向发生改变,原因是
您最近一年使用:0次
名校
3 . 原电池和电解池都能实现能量的转换。回答下列问题:
(1)银锌电池广泛用作各种电子仪器的电源,它的充电、放电过程可表示为2Ag+Zn(OH)2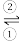 Ag2O+Zn+H2O,电池的放电过程是
Ag2O+Zn+H2O,电池的放电过程是___________ (填“①”或“②”),Ag2O电极发生的反应是___________ (填“氧化反应”或“还原反应”)。
(2)科学家预言,燃料电池将是21世纪获得电力的重要途径,在稀硫酸电解质中直接加入纯化后的甲醇 ,同时向一个电极通入空气制得燃料电池,此电池的正极发生的电极反应为
,同时向一个电极通入空气制得燃料电池,此电池的正极发生的电极反应为___________ 。
(3) Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是___________ ,欲除去Cu2+,最好选用下列试剂中的___________ (填字母)。
A.NaOH B.Zn C.Fe D.NH3·H2O
(1)银锌电池广泛用作各种电子仪器的电源,它的充电、放电过程可表示为2Ag+Zn(OH)2
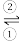 Ag2O+Zn+H2O,电池的放电过程是
Ag2O+Zn+H2O,电池的放电过程是(2)科学家预言,燃料电池将是21世纪获得电力的重要途径,在稀硫酸电解质中直接加入纯化后的甲醇
 ,同时向一个电极通入空气制得燃料电池,此电池的正极发生的电极反应为
,同时向一个电极通入空气制得燃料电池,此电池的正极发生的电极反应为(3) Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
A.NaOH B.Zn C.Fe D.NH3·H2O
您最近一年使用:0次
2024-04-25更新
|
110次组卷
|
2卷引用:江苏省扬州中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
4 . 以分子中只含一个碳原子的化合物为原料,用化工方法制造产品的化学体系总称为“一碳化学”。回答下列问题:
(1)CO(g)与H2O(g)在恒容密闭容器中反应:CO(g)+H2O(g) CO2(g)+H2(g)。
CO2(g)+H2(g)。
①该反应的氧化剂是_______ (填化学式)。
②下列说法正确的是_______ (填字母)。
A.升高反应温度,可使CO完全转化
B.充入He,可加快反应速率
C.反应达到平衡后,反应速率为零
D.使用合适催化剂可以加快反应速率
③下列描述中能说明该反应达到平衡状态的是_______ 。
A.CO、H2和CO2三种物质的浓度相等
B.混合气体的密度不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗2molH2的同时消耗2molCO
(2)在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。反应过程中测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。
CH3OH(g)+H2O(g)。反应过程中测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。
①3~6min内,v(H2)=_______ 。
②第3min时
_______ 第9min时 (填“>”、“<”或“=”),第12min时,
(填“>”、“<”或“=”),第12min时,
_______  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
③求12min末时,混合气体中CH3OH的物质的量分数__________ 。(写出计算过程,要求列出三段式)【已知:B的物质的量分数=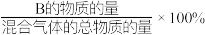 】
】
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为CH3OH+8OH﹣﹣6e﹣= +6H2O。则下列说法正确的是
+6H2O。则下列说法正确的是_______ (填序号)。
①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH3OH转移1.2mol电子
(1)CO(g)与H2O(g)在恒容密闭容器中反应:CO(g)+H2O(g)
 CO2(g)+H2(g)。
CO2(g)+H2(g)。①该反应的氧化剂是
②下列说法正确的是
A.升高反应温度,可使CO完全转化
B.充入He,可加快反应速率
C.反应达到平衡后,反应速率为零
D.使用合适催化剂可以加快反应速率
③下列描述中能说明该反应达到平衡状态的是
A.CO、H2和CO2三种物质的浓度相等
B.混合气体的密度不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内消耗2molH2的同时消耗2molCO
(2)在容积为2L的恒温密闭容器中,充入1molCO2和3molH2,发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。反应过程中测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。
CH3OH(g)+H2O(g)。反应过程中测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。| 时间 | 0min | 3min | 6min | 9min | 12min |
| n(CH3OH)/mol | 0 | 0.50 | a | 0.75 | 0.75 |
| n(CO2)/mol | 1 | 0.50 | 0.35 | 0.25 | 0.25 |
②第3min时

 (填“>”、“<”或“=”),第12min时,
(填“>”、“<”或“=”),第12min时,
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)③求12min末时,混合气体中CH3OH的物质的量分数
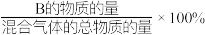 】
】(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。其中负极反应式为CH3OH+8OH﹣﹣6e﹣=
 +6H2O。则下列说法正确的是
+6H2O。则下列说法正确的是①电池放电时通入空气的电极为负极
②电池放电时,电解质溶液的碱性逐渐减弱
③电池放电时每消耗6.4gCH3OH转移1.2mol电子
您最近一年使用:0次
名校
解题方法
5 . 将CO合成甲醇是实现“碳达峰、碳中和”的一项重要措施,在此过程中可能涉及以下物质:
①H2②O2③CO④He⑤H2O2⑥Na2O2⑦KOH⑧CH3OH⑨K2CO3
请判断:
(1)含有极性共价键的离子化合物有___________ (填编号)。
(2)含有非极性共价键的共价化合物有___________ (填编号)。
(3)在实验室中模拟CO合成甲醇的反应,在2L密闭容器内,400℃时发生反应:CO(g)+2H2(g)⇌CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
已知每生成1molCH3OH(g),放出的热量为116kJ。计算上述反应达到平衡时放出的热量Q=___________ kJ(保留2位有效数字)。
(4)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的总反应式为:2CH3OH+3O2+4OH-=2 +6H2O。则电池放电时通入空气的电极为
+6H2O。则电池放电时通入空气的电极为___________ (“正”或“负”)极;从电极反应来看,每消耗1molCH3OH转移的电子数为___________ NA。
①H2②O2③CO④He⑤H2O2⑥Na2O2⑦KOH⑧CH3OH⑨K2CO3
请判断:
(1)含有极性共价键的离子化合物有
(2)含有非极性共价键的共价化合物有
(3)在实验室中模拟CO合成甲醇的反应,在2L密闭容器内,400℃时发生反应:CO(g)+2H2(g)⇌CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CH3OH)(mol) | 0 | 0.009 | 0.012 | 0.013 | 0.013 |
(4)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的总反应式为:2CH3OH+3O2+4OH-=2
 +6H2O。则电池放电时通入空气的电极为
+6H2O。则电池放电时通入空气的电极为
您最近一年使用:0次
2023-08-10更新
|
230次组卷
|
2卷引用:山东省菏泽市定陶区第一中学2023-2024学年高一下学期第一次月考化学试题
名校
6 . 人们应用原电池原理制作了多种电池,以满足不同的需要。以下是几种不同形式的原电池装置,请根据题中提供的信息,填写空格。
(1)某原电池的装置如图1所示。若需将反应 设计成如图1所示的原电池装置,则A(负极)极材料为
设计成如图1所示的原电池装置,则A(负极)极材料为______________ (填化学式),B(正极)极的电极反应式为_____________________________ ,溶液C为______________ 。
(3)甲醇是重要的化工原料,又可作为燃料使用,用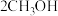 和
和 组合形成的质子交换膜燃料电池的结构示意图如图3。电池总反应为
组合形成的质子交换膜燃料电池的结构示意图如图3。电池总反应为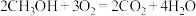 ,则a处充入的是
,则a处充入的是______ (填化学式),电极c的电极反应式为___________ ;若线路中转移3mol电子,则上述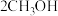 燃料电池消耗的
燃料电池消耗的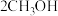 的质量为
的质量为________ g。
(1)某原电池的装置如图1所示。若需将反应
 设计成如图1所示的原电池装置,则A(负极)极材料为
设计成如图1所示的原电池装置,则A(负极)极材料为

A.盐桥中的阴离子向 溶液移动 溶液移动 | B.电子流动方向为Zn→盐桥→Cu |
| C.铜片作电池的正极 | D.该电池比单液原电池的电流更稳定 |
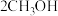 和
和 组合形成的质子交换膜燃料电池的结构示意图如图3。电池总反应为
组合形成的质子交换膜燃料电池的结构示意图如图3。电池总反应为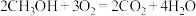 ,则a处充入的是
,则a处充入的是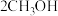 燃料电池消耗的
燃料电池消耗的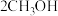 的质量为
的质量为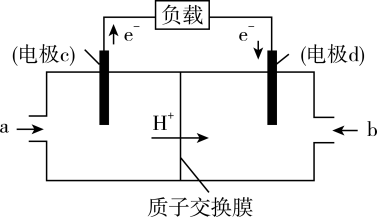
您最近一年使用:0次
2023-07-21更新
|
167次组卷
|
3卷引用:综合突破02 期末压轴80题之非选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
(已下线)综合突破02 期末压轴80题之非选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)辽宁省朝阳市建平县实验中学2022-2023学年高一下学期7月期末化学试题辽宁省本溪市第一中学2023-2024学年高二上学期11月期中考试化学试题
解题方法
7 . 甲醇 是一种重要的化工原料和新型燃料。甲醇、空气和
是一种重要的化工原料和新型燃料。甲醇、空气和 溶液组成的燃料电池的简易装置如图所示。下列有关说法正确的是
溶液组成的燃料电池的简易装置如图所示。下列有关说法正确的是
 是一种重要的化工原料和新型燃料。甲醇、空气和
是一种重要的化工原料和新型燃料。甲醇、空气和 溶液组成的燃料电池的简易装置如图所示。下列有关说法正确的是
溶液组成的燃料电池的简易装置如图所示。下列有关说法正确的是
A. 为电源的负极 为电源的负极 |
B. 电极反应式为 电极反应式为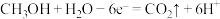 |
C. 极每消耗 极每消耗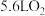 ,电路中则转移 ,电路中则转移 电子 电子 |
D.电池工作一段时间后,电解质溶液的 值变小 值变小 |
您最近一年使用:0次
名校
解题方法
8 . 甲醇( )的合成与应用具有广阔的发展前景。
)的合成与应用具有广阔的发展前景。
(1)工业上通过 和
和 化合来制备
化合来制备 :
:
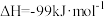 ,若将
,若将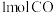 和
和 混合后充分反应,放出的热量
混合后充分反应,放出的热量_______ (填“大于”、“等于”或“小于”)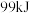 。
。
(2)工业上还可以通过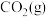 与
与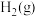 反应制备
反应制备 :
:
 。
。
①保持温度不变,向 恒容密闭容器中充入
恒容密闭容器中充入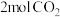 和
和 ,能说明该反应已达平衡状态的是
,能说明该反应已达平衡状态的是_______ (填字母)。
a.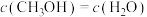 b.
b.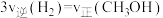 c.容器内压强保持不变
c.容器内压强保持不变
②在 恒容密闭容器中,反应过程中反应物和生成物的物质的量数据见下表:
恒容密闭容器中,反应过程中反应物和生成物的物质的量数据见下表:
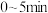 内的平均反应速率
内的平均反应速率
_______ 。反应达平衡时,
_______ 。
③向恒容密闭容器中充入一定量CO2和 ,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态),CO2的转化率随反应温度的变化如图所示。其中a点CO2的转化率高于b点的原因是
,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态),CO2的转化率随反应温度的变化如图所示。其中a点CO2的转化率高于b点的原因是_______ 。_______ (填“A”或“B”)极区移动。
②线路中通过1mol电子时,B区生成水的质量为_______  。
。
 )的合成与应用具有广阔的发展前景。
)的合成与应用具有广阔的发展前景。(1)工业上通过
 和
和 化合来制备
化合来制备 :
:
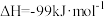 ,若将
,若将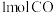 和
和 混合后充分反应,放出的热量
混合后充分反应,放出的热量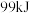 。
。(2)工业上还可以通过
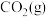 与
与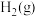 反应制备
反应制备 :
:
 。
。①保持温度不变,向
 恒容密闭容器中充入
恒容密闭容器中充入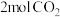 和
和 ,能说明该反应已达平衡状态的是
,能说明该反应已达平衡状态的是a.
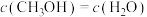 b.
b.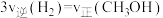 c.容器内压强保持不变
c.容器内压强保持不变②在
 恒容密闭容器中,反应过程中反应物和生成物的物质的量数据见下表:
恒容密闭容器中,反应过程中反应物和生成物的物质的量数据见下表:| 反应时间 | 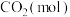 |  | 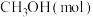 |
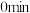 | 2 | 6 | 0 |
 | 1 | ||
 | 1.5 | ||
 | 1.5 |
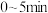 内的平均反应速率
内的平均反应速率

③向恒容密闭容器中充入一定量CO2和
 ,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态),CO2的转化率随反应温度的变化如图所示。其中a点CO2的转化率高于b点的原因是
,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态),CO2的转化率随反应温度的变化如图所示。其中a点CO2的转化率高于b点的原因是
②线路中通过1mol电子时,B区生成水的质量为
 。
。
您最近一年使用:0次
2021-07-07更新
|
414次组卷
|
6卷引用:重难点01 化学反应速率的计算及平衡图像分析-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
(已下线)重难点01 化学反应速率的计算及平衡图像分析-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)江苏省徐州市2020-2021学年高一下学期期末抽测化学试题江苏省徐州市第七中学2021-2022学年高一下学期4月学情调研化学试题江苏省泰州中学2022-2023学年高一下学期期中考试化学试题江苏省徐州市第一中学2022-2023学年高一下学期期中考试化学试题江苏省响水中学2022-2023学年高一下学期7月学情调研考试化学试题
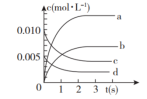
9 . 近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。现在实验室中模拟甲醇合成反应,在2 L密闭容器内,400℃时发生反应:CO(g)+2H2(g) CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
(1)图中表示CH3OH的浓度变化的曲线是_______ (填字母)。_______ 。随着反应的进行,该反应的速率逐渐减慢的原因是_______ 。
(3)该反应是一个放热反应,说明该反应中破坏1 mol CO和2 mol H2的化学键吸收的能量_______ 形成1mol CH3OH释放的能量(填“<”、“=”或“>”)。
(4)已知在400℃时,反应CO(g)+2H2(g) CH3OH(g)生成1 mol CH3OH(g),放出的热量为116 kJ。计算上述反应达到平衡时放出的热量Q=
CH3OH(g)生成1 mol CH3OH(g),放出的热量为116 kJ。计算上述反应达到平衡时放出的热量Q=_______ kJ。
(5)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的总反应式为:2CH3OH+3O2+4OH-=2 +6H2O
+6H2O
则电池放电时通入空气的电极为_______ (“正”或“负”)极;从电极反应来看,每消耗1 mol CH3OH转移_______ mol电子。
 CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CH3OH)(mol) | 0 | 0.009 | 0.012 | 0.013 | 0.013 |
(3)该反应是一个放热反应,说明该反应中破坏1 mol CO和2 mol H2的化学键吸收的能量
(4)已知在400℃时,反应CO(g)+2H2(g)
 CH3OH(g)生成1 mol CH3OH(g),放出的热量为116 kJ。计算上述反应达到平衡时放出的热量Q=
CH3OH(g)生成1 mol CH3OH(g),放出的热量为116 kJ。计算上述反应达到平衡时放出的热量Q=(5)甲醇燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的总反应式为:2CH3OH+3O2+4OH-=2
 +6H2O
+6H2O则电池放电时通入空气的电极为
您最近一年使用:0次
2021-06-15更新
|
422次组卷
|
3卷引用:重难点01 热能与电能综合题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
(已下线)重难点01 热能与电能综合题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)山东省临沂市兰陵县2020-2021学年高一下学期期中教学质量检测化学试题北京市第二十中学2020-2021学年高一下学期期末考试化学试题
名校
解题方法
10 . 氢氧燃料电池已用于航天飞机,其工作原理如图所示。关于该燃料电池的说法不正确 的是
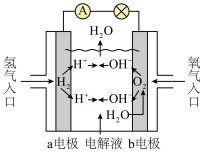
| A.氢氧燃料电池中,当转移4 mol电子时消耗2 mol氢气 |
| B.电子从a电极经外电路流向b电极 |
| C.供电时的总反应为:2H2 + O2 = 2H2O |
| D.甲烷燃料电池中,通入氧气的一极为负极 |
您最近一年使用:0次
2021-05-06更新
|
327次组卷
|
2卷引用:北京市第三中学2023-2024学年高一下学期期中考试化学试题






