解题方法
1 . 《自然》杂志报道,科学家设计出了“空气燃料实验系统”,其过程分三步:
第一步,利用太阳能收集空气中的 和
和 ;
;
第二步,在太阳能作用下将 和
和 转化成合成气(CO、H2);
转化成合成气(CO、H2);
第三步,利用合成气合成液态烃和甲醇。
Ⅰ.模拟制备合成气的装置如图所示。
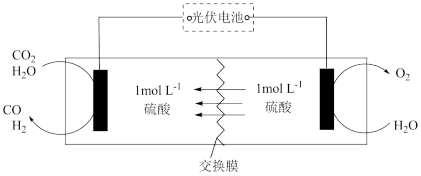
回答下列问题:
(1)交换膜是_______ (填“阴离子”或“阳离子”)交换膜。b极是_______ (填“正极”或“负极”)。
Ⅱ.利用合成气合成甲醇、甲烷等。已知:
反应ⅰ:
反应ⅱ:
(2)在 和一定温度下,由最稳定单质生成
和一定温度下,由最稳定单质生成 纯物质的热效应,称为该物质的标准生成热(
纯物质的热效应,称为该物质的标准生成热(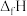 )。相关物质的标准生成热数据如表所示:
)。相关物质的标准生成热数据如表所示:

_______  。
。
(3)在某温度、催化剂作用下,仅发生反应ⅱ,该反应的速率方程为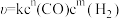 (k为速率常数,与温度、催化剂有关,与浓度无关)。测得速率与CO、H2的浓度关系如表所示:
(k为速率常数,与温度、催化剂有关,与浓度无关)。测得速率与CO、H2的浓度关系如表所示:
下列推断正确的是_______ (填标号)。
A. B.
B. C.其他条件不变,升高温度,速率增大
C.其他条件不变,升高温度,速率增大
(4)在一定温度下,向某恒容密闭容器中充入CO和H2,仅发生反应ⅰ,测得平衡体系中 的体积分数
的体积分数 与
与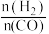 的关系如图1所示。
的关系如图1所示。

在a、b、c三点中,CO的平衡转化率最大的是_______ 。(填标号)
(5)向1L恒容密闭容器中充入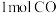 和
和 ,在催化剂作用下同时发生反应ⅰ和反应ⅱ,测得产物甲醇、甲烷的选择性(甲醇或甲烷的物质的量占两者总物质的量的百分数)与温度的关系如图2所示。
,在催化剂作用下同时发生反应ⅰ和反应ⅱ,测得产物甲醇、甲烷的选择性(甲醇或甲烷的物质的量占两者总物质的量的百分数)与温度的关系如图2所示。

①当温度高于 时,该催化剂选择性较大的产物是
时,该催化剂选择性较大的产物是_______ 。(填化学式)
② 时反应达到平衡,此时
时反应达到平衡,此时 ,
, 的选择性为80%,则该温度下反应ⅰ的平衡常数K=
的选择性为80%,则该温度下反应ⅰ的平衡常数K=_______ 。(结果取整数)
第一步,利用太阳能收集空气中的
 和
和 ;
;第二步,在太阳能作用下将
 和
和 转化成合成气(CO、H2);
转化成合成气(CO、H2);第三步,利用合成气合成液态烃和甲醇。
Ⅰ.模拟制备合成气的装置如图所示。

回答下列问题:
(1)交换膜是
Ⅱ.利用合成气合成甲醇、甲烷等。已知:
反应ⅰ:

反应ⅱ:

(2)在
 和一定温度下,由最稳定单质生成
和一定温度下,由最稳定单质生成 纯物质的热效应,称为该物质的标准生成热(
纯物质的热效应,称为该物质的标准生成热(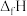 )。相关物质的标准生成热数据如表所示:
)。相关物质的标准生成热数据如表所示:| 物质 |  |  |  |  |  |
 | 0 | −75 | −110 | −201 | −242 |

 。
。(3)在某温度、催化剂作用下,仅发生反应ⅱ,该反应的速率方程为
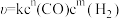 (k为速率常数,与温度、催化剂有关,与浓度无关)。测得速率与CO、H2的浓度关系如表所示:
(k为速率常数,与温度、催化剂有关,与浓度无关)。测得速率与CO、H2的浓度关系如表所示:| 实验 |  |  | 速率 |
| Ⅰ | 0.10 | 0.10 | υ |
| Ⅱ | 0.20 | 0.10 | 2υ |
| Ⅲ | 0.20 | 0.20 | 8υ |
| Ⅳ | 0.40 | x | 36υ |
下列推断正确的是
A.
 B.
B. C.其他条件不变,升高温度,速率增大
C.其他条件不变,升高温度,速率增大(4)在一定温度下,向某恒容密闭容器中充入CO和H2,仅发生反应ⅰ,测得平衡体系中
 的体积分数
的体积分数 与
与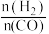 的关系如图1所示。
的关系如图1所示。
在a、b、c三点中,CO的平衡转化率最大的是
(5)向1L恒容密闭容器中充入
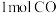 和
和 ,在催化剂作用下同时发生反应ⅰ和反应ⅱ,测得产物甲醇、甲烷的选择性(甲醇或甲烷的物质的量占两者总物质的量的百分数)与温度的关系如图2所示。
,在催化剂作用下同时发生反应ⅰ和反应ⅱ,测得产物甲醇、甲烷的选择性(甲醇或甲烷的物质的量占两者总物质的量的百分数)与温度的关系如图2所示。
①当温度高于
 时,该催化剂选择性较大的产物是
时,该催化剂选择性较大的产物是②
 时反应达到平衡,此时
时反应达到平衡,此时 ,
, 的选择性为80%,则该温度下反应ⅰ的平衡常数K=
的选择性为80%,则该温度下反应ⅰ的平衡常数K=
您最近一年使用:0次
名校
解题方法
2 . 《自然》杂志报道,科学家们设计出了利用合成气合成液态烃和甲醇,模拟制备合成气的装置如图所示。下列说法不正确的是


| A.交换膜是阳离子交换膜 |
| B.a极是正极,发生还原反应 |
C.由 合成 合成 的电极反应式为 的电极反应式为 |
D.当装置中产生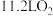 (标准状态)时,理论上迁移的离子为 (标准状态)时,理论上迁移的离子为 |
您最近一年使用:0次
解题方法
3 . 制造尼龙 的原料已二腈用量很大,工业采用丙烯腈
的原料已二腈用量很大,工业采用丙烯腈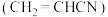 电解合成已二腈
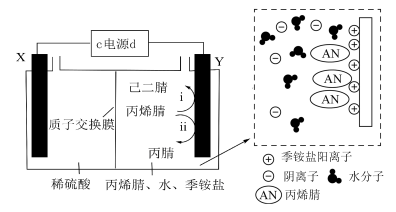
电解合成已二腈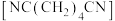 ,电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈
,电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈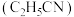 等副产物,向
等副产物,向 极区电解液中加入少量季铵盐,当溶液的
极区电解液中加入少量季铵盐,当溶液的 时,已二腈的产率最高。下列说法不正确的是
时,已二腈的产率最高。下列说法不正确的是
 的原料已二腈用量很大,工业采用丙烯腈
的原料已二腈用量很大,工业采用丙烯腈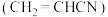 电解合成已二腈
电解合成已二腈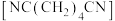 ,电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈
,电解原理如图所示(两极均为惰性电极),电解过程会产生丙腈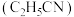 等副产物,向
等副产物,向 极区电解液中加入少量季铵盐,当溶液的
极区电解液中加入少量季铵盐,当溶液的 时,已二腈的产率最高。下列说法不正确的是
时,已二腈的产率最高。下列说法不正确的是
A.电源 极的电势高于 极的电势高于 极 极 |
B.电极 上 上 的电极反应式为: 的电极反应式为: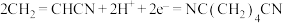 |
C.生成 已二腈和丙腈的混合物,则 已二腈和丙腈的混合物,则 极区溶液的质量理论上减少 极区溶液的质量理论上减少 |
| D.季铵盐可增强电解液的电导率,抑制ⅱ反应的发生,提高已二腈的选择性 |
您最近一年使用:0次
解题方法
4 . 我国科技工作者设计了如图所示的电化学装置(隔膜a只允许OH-通过),实现了两电极体系中二氧化碳和辛胺【CH3(CH2)7NH2】制备甲酸和辛腈【 】的高选择性合成。下列说法正确的是
】的高选择性合成。下列说法正确的是

 】的高选择性合成。下列说法正确的是
】的高选择性合成。下列说法正确的是
A.理论上有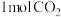 参与反应,会有2mol辛腈生成 参与反应,会有2mol辛腈生成 |
B.电解过程中,In/In2O3-x电极区的反应为 |
C.电解过程中,溶液中的 从右边移向左边 从右边移向左边 |
| D.每消耗xmol的CO2理论上通过隔膜a的OH-也为2xmol |
您最近一年使用:0次
5 . 研究氨的制备、应用及氨氮的去除有重要意义。
(1)电解法制氨。
如图所示的电解池电解 溶液可制得氨。工作时,
溶液可制得氨。工作时, 在双极膜(由阴、阳离子膜复合而成)界面处解离成
在双极膜(由阴、阳离子膜复合而成)界面处解离成 和
和 ,分别通过阴、阳离子膜分别进入两侧极室。
,分别通过阴、阳离子膜分别进入两侧极室。

①进入a极室的离子是___________ (填“ ”或“
”或“ ”)。
”)。
②产生 的电极反应式为
的电极反应式为___________ 。
③电解池工作时,在电极b可得到副产品___________ 。
(2)氨的应用。以 和
和 为原料在一定温度和压强下合成尿素的反应分两步:
为原料在一定温度和压强下合成尿素的反应分两步:
Ⅰ. 和
和 生成
生成 ;
;
Ⅱ. 分解生成
分解生成 。
。
反应过程中能量变化如图所示。

①总反应的速率取决于第___________ 步。
② 反应的
反应的
___________ (用图中能量数据表示)。
(3)氨氮的去除。
用 溶液模拟氨氮废水,以镁作阳极、不锈钢作阴极进行电解,可将废水中的
溶液模拟氨氮废水,以镁作阳极、不锈钢作阴极进行电解,可将废水中的 转化为
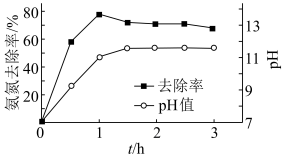
转化为 沉淀而除去。调节溶液初始
沉淀而除去。调节溶液初始 ,氨氮去除率和溶液
,氨氮去除率和溶液 随时间的变化情况如图所示。
随时间的变化情况如图所示。
①电解时两极反应式分别为: ,
,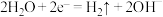 。写出废水中生成
。写出废水中生成 沉淀的离子方程式:
沉淀的离子方程式:___________ 。
②反应 以后,氨氮去除率随时间的延长反而下降的原因是
以后,氨氮去除率随时间的延长反而下降的原因是___________ 。
(1)电解法制氨。
如图所示的电解池电解
 溶液可制得氨。工作时,
溶液可制得氨。工作时, 在双极膜(由阴、阳离子膜复合而成)界面处解离成
在双极膜(由阴、阳离子膜复合而成)界面处解离成 和
和 ,分别通过阴、阳离子膜分别进入两侧极室。
,分别通过阴、阳离子膜分别进入两侧极室。
①进入a极室的离子是
 ”或“
”或“ ”)。
”)。②产生
 的电极反应式为
的电极反应式为③电解池工作时,在电极b可得到副产品
(2)氨的应用。以
 和
和 为原料在一定温度和压强下合成尿素的反应分两步:
为原料在一定温度和压强下合成尿素的反应分两步:Ⅰ.
 和
和 生成
生成 ;
;Ⅱ.
 分解生成
分解生成 。
。反应过程中能量变化如图所示。

①总反应的速率取决于第
②
 反应的
反应的
(3)氨氮的去除。
用
 溶液模拟氨氮废水,以镁作阳极、不锈钢作阴极进行电解,可将废水中的
溶液模拟氨氮废水,以镁作阳极、不锈钢作阴极进行电解,可将废水中的 转化为
转化为 沉淀而除去。调节溶液初始
沉淀而除去。调节溶液初始 ,氨氮去除率和溶液
,氨氮去除率和溶液 随时间的变化情况如图所示。
随时间的变化情况如图所示。
①电解时两极反应式分别为:
 ,
,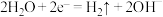 。写出废水中生成
。写出废水中生成 沉淀的离子方程式:
沉淀的离子方程式:②反应
 以后,氨氮去除率随时间的延长反而下降的原因是
以后,氨氮去除率随时间的延长反而下降的原因是
您最近一年使用:0次
2024-02-04更新
|
90次组卷
|
2卷引用:江苏省苏州市2023-2024学年高二上学期期末学业质量阳光指标调研化学试卷
名校
6 . 过渡元素的金属及其氧化物常用作反应的催化剂。
(1) 和
和 催化合成
催化合成 的反应如下:
的反应如下: (未配平)
(未配平)
①该反应的催化历程可简化为两步:第Ⅰ步: ;第Ⅱ步的方程式为
;第Ⅱ步的方程式为___________ 。第Ⅰ步反应决定了总反应达到平衡的时间,两步反应的活化能EI___________ EⅡ。(填“>”、“=”或“<”)
②加入Ga可以增大催化剂的表面积。Ga的基态原子核外电子排布式为___________ 。
(2)我国科学家以 和
和 为原料,熔融
为原料,熔融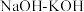 为离子导体,通过催化电解法制备
为离子导体,通过催化电解法制备 ,装置如图1所示,其中在电极B上的反应过程如图2所示。
,装置如图1所示,其中在电极B上的反应过程如图2所示。

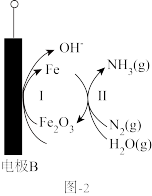
①参与电极B上反应的催化剂是___________ ,
②描述在电极B上催化生成 的过程
的过程___________ 。
(3)富氧条件下, 和NO在钒基催化作用下发生脱硝反应,方程式可表示为
和NO在钒基催化作用下发生脱硝反应,方程式可表示为
主反应: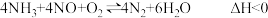
副反应:Ⅰ.
Ⅱ.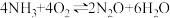
…… ……
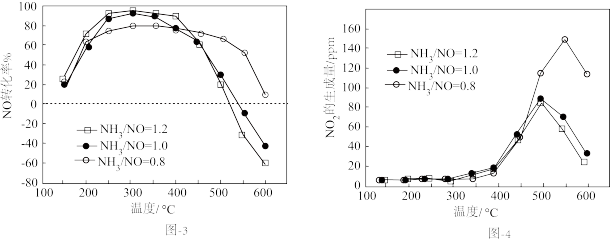
不同氨氮比[ ]下,NO的转化率和
]下,NO的转化率和 的生成量随温度的变化曲线如图3和图4所示,测得300℃后,
的生成量随温度的变化曲线如图3和图4所示,测得300℃后, 转化率基本不变。
转化率基本不变。
①上述脱硝的主反应中,分别被NO和 氧化的
氧化的 的质量之比为
的质量之比为___________ ,
②超过400℃:温度升高,NO转化率下降,可能原因是___________ ;氨氮比越大,NO转化率越小,可能原因是___________ 。
(1)
 和
和 催化合成
催化合成 的反应如下:
的反应如下: (未配平)
(未配平)①该反应的催化历程可简化为两步:第Ⅰ步:
 ;第Ⅱ步的方程式为
;第Ⅱ步的方程式为②加入Ga可以增大催化剂的表面积。Ga的基态原子核外电子排布式为
(2)我国科学家以
 和
和 为原料,熔融
为原料,熔融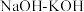 为离子导体,通过催化电解法制备
为离子导体,通过催化电解法制备 ,装置如图1所示,其中在电极B上的反应过程如图2所示。
,装置如图1所示,其中在电极B上的反应过程如图2所示。

①参与电极B上反应的催化剂是
②描述在电极B上催化生成
 的过程
的过程(3)富氧条件下,
 和NO在钒基催化作用下发生脱硝反应,方程式可表示为
和NO在钒基催化作用下发生脱硝反应,方程式可表示为主反应:
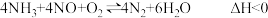
副反应:Ⅰ.

Ⅱ.
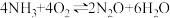
…… ……
不同氨氮比[
 ]下,NO的转化率和
]下,NO的转化率和 的生成量随温度的变化曲线如图3和图4所示,测得300℃后,
的生成量随温度的变化曲线如图3和图4所示,测得300℃后, 转化率基本不变。
转化率基本不变。
①上述脱硝的主反应中,分别被NO和
 氧化的
氧化的 的质量之比为
的质量之比为②超过400℃:温度升高,NO转化率下降,可能原因是
您最近一年使用:0次
2022-01-23更新
|
367次组卷
|
2卷引用:江苏省泰州市2021-2022学年高二上学期期末考试化学试卷
名校
解题方法
7 . -芳硒基酮作为重要的中间体在有机合成方面具有重要应用, 电化学氧化-碘促进法采用丙酮和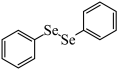 为原料,最终得到硒基丙酮化合物(
为原料,最终得到硒基丙酮化合物( ),其工作原理如图所示(A、B均为惰性电极)。下列说法正确的是
),其工作原理如图所示(A、B均为惰性电极)。下列说法正确的是

 为原料,最终得到硒基丙酮化合物(
为原料,最终得到硒基丙酮化合物( ),其工作原理如图所示(A、B均为惰性电极)。下列说法正确的是
),其工作原理如图所示(A、B均为惰性电极)。下列说法正确的是
A.该装置发生的总反应方程式为:2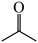 + +  2 2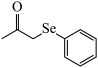 +H2↑ +H2↑ |
| B.该装置将电能转化为化学能,C为电源的负极 |
| C.阴极发生的电极反应为:I2+2e-=2I- |
| D.装置工作时,阴离子移向B电极 |
您最近一年使用:0次
2021-08-04更新
|
304次组卷
|
2卷引用:重庆南开中学2020-2021学年高二下学期期末考试化学试题
解题方法
8 . 最近我国科学家以 与己二胺为原料实现了甲酸盐和己二腈的高选择性合成,该合成的原理如下图所示。
与己二胺为原料实现了甲酸盐和己二腈的高选择性合成,该合成的原理如下图所示。
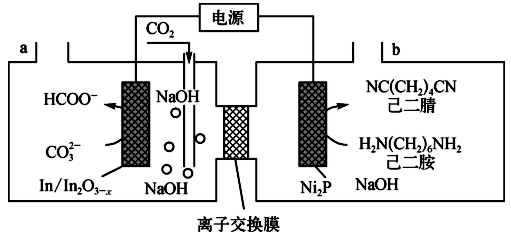
下列说法正确的是
 与己二胺为原料实现了甲酸盐和己二腈的高选择性合成,该合成的原理如下图所示。
与己二胺为原料实现了甲酸盐和己二腈的高选择性合成,该合成的原理如下图所示。
下列说法正确的是
A. 电极与电源负极相连 电极与电源负极相连 |
| B.当离子交换膜为阳离子选择性交换膜时,b中氢氧化钠的物质的量不变 |
C.在 电极上发生的反应为: 电极上发生的反应为: |
D. 电极上可能有副产物 电极上可能有副产物 生成 生成 |
您最近一年使用:0次
2022-01-29更新
|
87次组卷
|
4卷引用:湖南省湖湘名校联盟2021-2022学年高二上学期期末考试化学试题
湖南省湖湘名校联盟2021-2022学年高二上学期期末考试化学试题湖南省湘潭县2021-2022学年高二上学期期末考试化学试题(已下线)黄金卷6-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)(已下线)押江苏卷第12题 电化学及其应用 -备战2022年高考化学临考题号押题(江苏卷)
名校
解题方法
9 . 近期,天津大学化学团队以CO2与辛胺为原料实现了甲酸和辛腈的高选择性合成,装置工作原理如图。下列说法正确 的是

| A.Ni2P电极与电源负极相连 |
| B.辛胺转化为辛腈发生了还原反应 |
| C.In/In2O3-x电极上可能有副产物H2生成 |
| D.在In/In2O3-x电极上发生的反应为CO2+H2O-2e-=HCOO-+OH- |
您最近一年使用:0次
2021-01-22更新
|
1318次组卷
|
10卷引用:北京市海淀区2021届高三上学期期末考试化学试题
北京市海淀区2021届高三上学期期末考试化学试题天津市南开区2021届高三下学期一模化学试题山西省太原市第五中学2021届高三下学期第二次模拟考试理科综合化学试题第34届(2021年)高中化学奥林匹克竞赛浙江省预赛试题(已下线)第19讲 电解池 金属的电化学腐蚀与防护(精练)-2022年高考化学一轮复习讲练测(已下线)北京市第四中学2021-2022学年高二上学期期中考试化学试题北京市北京师范大学燕化附中2022-2023学年高二上学期10月月考化学试题北京市第二十中学2022-2023学年高三上学期12月月考化学试题北京市海淀区2023-2024学年高二上学期期中考试化学试题北京一零一中学2023-2024学年高二下学期期中考试化学试题
解题方法
10 . (1)二氧化碳是主要的温室气体,对二氧化碳的研究和利用在生产和生活中有重要意义。
(1)二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。
①在恒温恒容的密闭容器中通入一定量的CO2和H2发生反应,生成乙烯和水蒸气,下列能说明该反应达到平衡状态的是__ 。
A.容器内的压强不发生变化
B.生成的乙烯和水蒸气物质的量比为1∶4
C.断裂3molH—H键的同时断裂4molH—O键
D.v(CO2)正=3v(H2)逆
当反应达到平衡时,若在容器中通入氩气以增大压强,则n(C2H4)__ (填“变大”、“变小”或“不变”)。
②理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1Mpa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图1所示。

图1中,表示C2H4、CO2变化的曲线分别是___ 、___ 。CO2催化加氢合成C2H4反应的△H___ 0(填“大于”或“小于”)。
(2)电解法转化CO2可实现CO2资源化利用。电解CO2制HCOOH的原理示意图见图2。
①写出阴极CO2还原为HCOO-的电极反应式:___ 。
②电解一段时间后,阳极区的KHCO3溶液浓度降低,其原因是:___ 。
(1)二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。
①在恒温恒容的密闭容器中通入一定量的CO2和H2发生反应,生成乙烯和水蒸气,下列能说明该反应达到平衡状态的是
A.容器内的压强不发生变化
B.生成的乙烯和水蒸气物质的量比为1∶4
C.断裂3molH—H键的同时断裂4molH—O键
D.v(CO2)正=3v(H2)逆
当反应达到平衡时,若在容器中通入氩气以增大压强,则n(C2H4)
②理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1Mpa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图1所示。

图1中,表示C2H4、CO2变化的曲线分别是
(2)电解法转化CO2可实现CO2资源化利用。电解CO2制HCOOH的原理示意图见图2。
①写出阴极CO2还原为HCOO-的电极反应式:
②电解一段时间后,阳极区的KHCO3溶液浓度降低,其原因是:
您最近一年使用:0次



