(1)二氧化碳是主要的温室气体,对二氧化碳的研究和利用在生产和生活中有重要意义。
(1)二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。
①在恒温恒容的密闭容器中通入一定量的CO2和H2发生反应,生成乙烯和水蒸气,下列能说明该反应达到平衡状态的是__ 。
A.容器内的压强不发生变化
B.生成的乙烯和水蒸气物质的量比为1∶4
C.断裂3molH—H键的同时断裂4molH—O键
D.v(CO2)正=3v(H2)逆
当反应达到平衡时,若在容器中通入氩气以增大压强,则n(C2H4)__ (填“变大”、“变小”或“不变”)。
②理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1Mpa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图1所示。

图1中,表示C2H4、CO2变化的曲线分别是___ 、___ 。CO2催化加氢合成C2H4反应的△H___ 0(填“大于”或“小于”)。
(2)电解法转化CO2可实现CO2资源化利用。电解CO2制HCOOH的原理示意图见图2。
①写出阴极CO2还原为HCOO-的电极反应式:___ 。
②电解一段时间后,阳极区的KHCO3溶液浓度降低,其原因是:___ 。
(1)二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。
①在恒温恒容的密闭容器中通入一定量的CO2和H2发生反应,生成乙烯和水蒸气,下列能说明该反应达到平衡状态的是
A.容器内的压强不发生变化
B.生成的乙烯和水蒸气物质的量比为1∶4
C.断裂3molH—H键的同时断裂4molH—O键
D.v(CO2)正=3v(H2)逆
当反应达到平衡时,若在容器中通入氩气以增大压强,则n(C2H4)
②理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1Mpa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图1所示。

图1中,表示C2H4、CO2变化的曲线分别是
(2)电解法转化CO2可实现CO2资源化利用。电解CO2制HCOOH的原理示意图见图2。
①写出阴极CO2还原为HCOO-的电极反应式:
②电解一段时间后,阳极区的KHCO3溶液浓度降低,其原因是:
更新时间:2021-06-30 13:37:09
|
相似题推荐
【推荐1】CO2的资源化利用能有效减少CO2排放,充分利用碳资源。
(1)研究表明CO2与CH4在催化剂存在下可发生反应制得合成气:
①此反应的活化能Ea(正)___________ Ea(逆)(填“>”、“=”或“<”)。
②某温度下,向一恒容密闭容器中充入CO2和CH4发生上述反应,初始时CO2和CH4的分压分别为15kPa、20kPa,一段时间达到平衡后,测得体系压强增加了10kPa,则该反应的平衡常数Kp=_______ (kPa)2(结果保留两位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)电解法转化CO2可实现CO2资源化利用。电解CO2制HCOOH的原理如图。
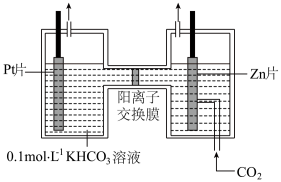
①写出阴极CO2还原为 的电极反应式:
的电极反应式:___________ 。
②电解一段时间后,溶液中的K+向_______ 极区移动(填“阳”或“阴”),阳极区溶液的 浓度
浓度________ (填“升高”、“降低”或“不变”)。
(3)CO2催化加氢合成二甲醚是一种CO2转化方法,其过程中主要发生下列反应:
反应I:
反应II:
在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。其中:
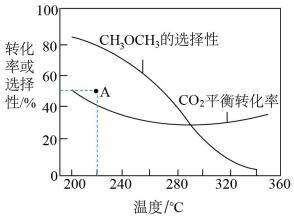
CH3OCH3的选择性=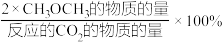
①温度高于300℃,CO2平衡转化率随温度升高而上升的原因是___________ 。
②220℃时,在催化剂作用下CO2与H2反应一段时间后,测得CH3OCH3的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高CH3OCH3选择性的措施有___________ 。(填一条即可)
(1)研究表明CO2与CH4在催化剂存在下可发生反应制得合成气:

①此反应的活化能Ea(正)
②某温度下,向一恒容密闭容器中充入CO2和CH4发生上述反应,初始时CO2和CH4的分压分别为15kPa、20kPa,一段时间达到平衡后,测得体系压强增加了10kPa,则该反应的平衡常数Kp=
(2)电解法转化CO2可实现CO2资源化利用。电解CO2制HCOOH的原理如图。

①写出阴极CO2还原为
 的电极反应式:
的电极反应式:②电解一段时间后,溶液中的K+向
 浓度
浓度(3)CO2催化加氢合成二甲醚是一种CO2转化方法,其过程中主要发生下列反应:
反应I:

反应II:

在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。其中:

CH3OCH3的选择性=
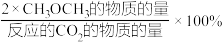
①温度高于300℃,CO2平衡转化率随温度升高而上升的原因是
②220℃时,在催化剂作用下CO2与H2反应一段时间后,测得CH3OCH3的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高CH3OCH3选择性的措施有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】甲基丙烯酸甲酯[ ]是有机玻璃的单体,其一种实验室制备方法如下:
]是有机玻璃的单体,其一种实验室制备方法如下:
Ⅰ.向 烧瓶中依次加入:
烧瓶中依次加入: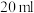 甲基丙烯酸、
甲基丙烯酸、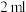 浓硫酸,冷却至室温,再加入
浓硫酸,冷却至室温,再加入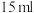 甲醇和几粒碎瓷片;
甲醇和几粒碎瓷片;
Ⅱ.按图示连接装置加热烧瓶中混合液,通过分水器分离出水,当分水器中水位不再增加时停止加热;冷却。
Ⅲ.纯化产品
粗产品依次用水洗、试剂Y溶液洗、水洗,在油层中加入无水硫酸镁,再经蒸馏得到较纯净的甲基丙烯酸甲酯17.6 g。
已知:
回答下列问题:
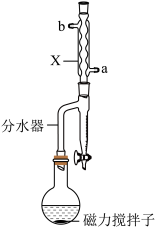
(1)图中仪器X的名称为___________ 。
(2)制备甲基丙烯酸甲酯的化学方程式为___________ 。
(3)每隔一段时间,打开油水分离器,将下层水放出来。从分水器中及时分离出水的目的是___________ 。
(4)纯化过程中,试剂Y是___________ ,其作用有___________ 。
(5)蒸馏提纯产品时温度应控制在___________ ℃。
(6)本实验中甲基丙烯酸甲酯的产率为___________ (保留三位有效数字)。
 ]是有机玻璃的单体,其一种实验室制备方法如下:
]是有机玻璃的单体,其一种实验室制备方法如下:Ⅰ.向
 烧瓶中依次加入:
烧瓶中依次加入: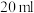 甲基丙烯酸、
甲基丙烯酸、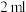 浓硫酸,冷却至室温,再加入
浓硫酸,冷却至室温,再加入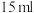 甲醇和几粒碎瓷片;
甲醇和几粒碎瓷片;Ⅱ.按图示连接装置加热烧瓶中混合液,通过分水器分离出水,当分水器中水位不再增加时停止加热;冷却。
Ⅲ.纯化产品
粗产品依次用水洗、试剂Y溶液洗、水洗,在油层中加入无水硫酸镁,再经蒸馏得到较纯净的甲基丙烯酸甲酯17.6 g。
已知:
| 药品 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度( ) ) | 相对分子质量 |
| 甲醇 | -98 | 64.5 | 与水混溶,易溶于有机溶剂 | 0.79 | 32 |
| 甲基丙烯酸 | 15 | 161 | 溶于热水,易溶于有机剂 | 1.01 | 86 |
| 甲基丙烯酸甲酯 | -48 | 100 | 微溶于水,易溶于有机溶剂 | 0.944 | 100 |

(1)图中仪器X的名称为
(2)制备甲基丙烯酸甲酯的化学方程式为
(3)每隔一段时间,打开油水分离器,将下层水放出来。从分水器中及时分离出水的目的是
(4)纯化过程中,试剂Y是
(5)蒸馏提纯产品时温度应控制在
(6)本实验中甲基丙烯酸甲酯的产率为
您最近一年使用:0次
【推荐3】随着石油资源的日益枯竭,天然气的廾发利用越来越受到重视。CH4/CO2催化重整制备合成气(CO和H2)是温室气体CO2和CH4资源化利用的重要途径之一,并受了国内外研究人员的高度重视。回答下列问题:
(1)已知:①CH4(g)+H2O(g) CO(g)+3H2(g)△H1=+205.9 kJ·mol-1
CO(g)+3H2(g)△H1=+205.9 kJ·mol-1
②CO(g)+H2O(g) CO2(g)+H2(g)△H2=-41.2 kJ·mol-1
CO2(g)+H2(g)△H2=-41.2 kJ·mol-1
CH4/CO2催化重整反应为CH4(g)+CO2(g) 2CO(g)+2H2(g)△H
2CO(g)+2H2(g)△H
该催化重整反应的△H=______ kJ·mol-1。要缩短该反应达到平衡的时间并提高H2的产率可采取的措施为_____ 。
(2)向2L刚性密闭容器中充入2molCH4和2mol CO2进行催化重整反应,不同温度下平衡体系中CH4和CO的体积分数( )随温度变化如下表所示。
)随温度变化如下表所示。
已知b>a>c,则T1______ T2(填“>”“<”或“=”)。T1下该反应的平衡常数K=_______ (mol2·L-2)
(3)实验研究表明,载体对催化剂性能起着极为重要的作用,在压强0.03MPa,温度750℃条件下,载体对镍基催化剂性能的影响相关数据如下表:
由上表判断,应选择载体为_______ (填化学式),理由是________ 。
(4)现有温度相同的I、Ⅱ、Ⅲ三个恒压密闭容器,均充入2mol CH4(g)和2 molCO2(g)进行反应,三个容器的反应压强分别为p1atm、p2atm、p3atm,在其他条件相同的情况下,反应均进行到tmin时,CO2的体积分数如图所示,此时I、Ⅱ、Ⅲ个容器中一定处于化学平衡状态的是_______ 。

(5)利用合成气为原料合成甲醇,其反应为CO(g)+2H2(g) CH3OH(g),在一定温度下查得该反应的相关数据如下表所示:
CH3OH(g),在一定温度下查得该反应的相关数据如下表所示:
该反应速率的通式为ν正=k正cm(CO)·cn(H2)(k正是与温度有关的速率常数)。由表中数据可确定反应速率的通式中n=____ (取正整数)。若该温度下平衡时组别1的产率为25%,则组别1平衡时的v正=______ (保留1位小数)。
(1)已知:①CH4(g)+H2O(g)
 CO(g)+3H2(g)△H1=+205.9 kJ·mol-1
CO(g)+3H2(g)△H1=+205.9 kJ·mol-1②CO(g)+H2O(g)
 CO2(g)+H2(g)△H2=-41.2 kJ·mol-1
CO2(g)+H2(g)△H2=-41.2 kJ·mol-1CH4/CO2催化重整反应为CH4(g)+CO2(g)
 2CO(g)+2H2(g)△H
2CO(g)+2H2(g)△H该催化重整反应的△H=
(2)向2L刚性密闭容器中充入2molCH4和2mol CO2进行催化重整反应,不同温度下平衡体系中CH4和CO的体积分数(
 )随温度变化如下表所示。
)随温度变化如下表所示。φ 温度 | CH4 | CO |
| T1 | a | a |
| T2 | c | b |
(3)实验研究表明,载体对催化剂性能起着极为重要的作用,在压强0.03MPa,温度750℃条件下,载体对镍基催化剂性能的影响相关数据如下表:
催化剂 | 载体 | 转化率/% | 尾气组成/% | ||||
CH4 | CO2 | CH4 | CO2 | CO | H2 | ||
Ni | MgO | 99.3 | 87.7 | 0.8 | 6.8 | 50.3 | 42.1 |
CaO | 58.8 | 45.8 | 17.7 | 18.8 | 33.7 | 29.8 | |
CeO2 | 62.9 | 57.6 | 17.2 | 19.1 | 34.0 | 29.7 | |
(4)现有温度相同的I、Ⅱ、Ⅲ三个恒压密闭容器,均充入2mol CH4(g)和2 molCO2(g)进行反应,三个容器的反应压强分别为p1atm、p2atm、p3atm,在其他条件相同的情况下,反应均进行到tmin时,CO2的体积分数如图所示,此时I、Ⅱ、Ⅲ个容器中一定处于化学平衡状态的是

(5)利用合成气为原料合成甲醇,其反应为CO(g)+2H2(g)
 CH3OH(g),在一定温度下查得该反应的相关数据如下表所示:
CH3OH(g),在一定温度下查得该反应的相关数据如下表所示:组别 | 起始浓度/(mol·L-1) | 初始速率/(mol·L-1·min-1) | |
CO | H2 | ||
1 | 0.24 | 0.48 | 0.361 |
2 | 0.24 | 0.96 | 0.720 |
3 | 0.48 | 0.48 | 0.719 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】我国力争于2030年前做到碳达峰,2060 年前实现碳中和。CH4与CO2重整是CO2利用的研究热点之一、该重整反应体系主要涉及以下反应:
a)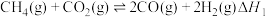
b)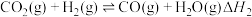
c)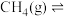
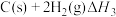
d)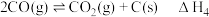
e)
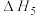
(1)根据盖斯定律,反应a的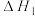 =
=_______ (写 出一个代数式即可)。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
(3)氨是最重要的化工产品之一、合成氨使用的氢气可以由反应a获得。
①与反应a有关化学反应的能量变化如图所示,则CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为_______ 。

②以上反应的产物在工业中有很多用处,例如制备高纯硅,甲醇、氨气等。根据有关键能数据,写出对应的热化学方程式。
I.工业上二氧化硅和碳(石墨)制备粗硅的热化学反应方程式:_______ 。
Ⅱ.一氧化碳和2mol氢气反应得到甲醇的热化学方程式:_______ 。
Ⅲ.工业上制备氨气的热化学反应方程式:_______ 。
Ⅳ.甲醇燃烧的热化学反应方程式:_______ 。
a)
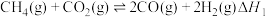
b)
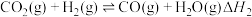
c)
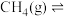
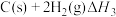
d)
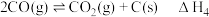
e)

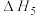
(1)根据盖斯定律,反应a的
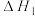 =
=(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
| A.增大CO2与CH4的浓度,反应a、b、c的正反应速率都增加 |
| B.碳的质量不再改变能作为反应c、d、e的平衡的标志 |
| C.如果只发生反应a,恒温恒容条件下,密度、压强不变,平均摩尔质量可作为平衡标志 |
| D.降低反应温度,反应a~e的正、逆反应速率都减小 |
①与反应a有关化学反应的能量变化如图所示,则CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为

②以上反应的产物在工业中有很多用处,例如制备高纯硅,甲醇、氨气等。根据有关键能数据,写出对应的热化学方程式。
| 化学键 | N—H |  | H—O | H—H | C—H | C—O |
键能( ) ) | 391 | 945 | 463 | 436 | 413 | 343 |
| 化学键 |  | C—C | O=O | C=O | Si—O | Si— Si |
键能( ) ) | 1076 | 346 | 498 | 750 | 460 | 176 |
I.工业上二氧化硅和碳(石墨)制备粗硅的热化学反应方程式:
Ⅱ.一氧化碳和2mol氢气反应得到甲醇的热化学方程式:
Ⅲ.工业上制备氨气的热化学反应方程式:
Ⅳ.甲醇燃烧的热化学反应方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】二氧化碳的排放受到环境和能源领域的关注,其综合利用是研究的重要课题。
I.第19届亚洲运动会使用废碳再生的绿色零碳甲醇作为主火炬塔燃料,实现循环内零碳排放。
(1)已知:反应①: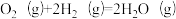
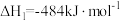
反应②: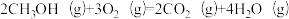
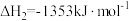
反应③: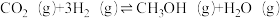 △H3。
△H3。
△H3=__________ kJ·mol-1,下列叙述中能说明反应③达到平衡状态的是________ (填字母)。
A.断裂3molC-H的同时生成1molC=O
B.恒容条件下,体系压强不再变化
C.恒容条件下,气体的密度不再变化
D.v正(CO2)= v正(H2O)
(2)压强为0.1MPa时,在密闭容器中按n(CO2):n(H2)=1:3投料,通过反应③合成甲醇,还发生副反应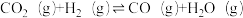
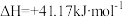 ,得CO2的平衡转化率如图所示。
,得CO2的平衡转化率如图所示。
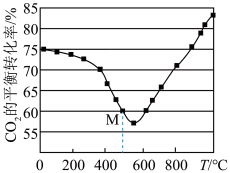
①温度高于570℃后,CO2平衡转化率随温度升高而增大的原因是_______________ 。
②图中M点CO2的平衡转化率为60%,若CH3OH的选择性为 (转化的CO2中生成CH3OH的百分比,则该温度下容器中H2O(g)的平衡分压为
(转化的CO2中生成CH3OH的百分比,则该温度下容器中H2O(g)的平衡分压为_______________ MPa。
Ⅱ.以甲醇和二氧化碳为原料,利用活性催化电极电解制备甲酸(甲酸盐)的原理如图。

(3)该装置中电子流动方向是_______________ :_____→_____,_____→_____。(用“A”“B”“a”“b”表示)
(4)电解过程中阴极的电极反应式为_______________ 。
(5)若有1molH+通过质子交换膜时,装置内生成HCOOˉ和HCOOH的物质的量的差为_______________ mol。
I.第19届亚洲运动会使用废碳再生的绿色零碳甲醇作为主火炬塔燃料,实现循环内零碳排放。
(1)已知:反应①:
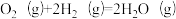
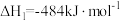
反应②:
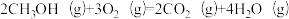
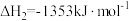
反应③:
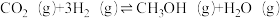 △H3。
△H3。△H3=
A.断裂3molC-H的同时生成1molC=O
B.恒容条件下,体系压强不再变化
C.恒容条件下,气体的密度不再变化
D.v正(CO2)= v正(H2O)
(2)压强为0.1MPa时,在密闭容器中按n(CO2):n(H2)=1:3投料,通过反应③合成甲醇,还发生副反应
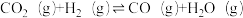
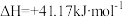 ,得CO2的平衡转化率如图所示。
,得CO2的平衡转化率如图所示。
①温度高于570℃后,CO2平衡转化率随温度升高而增大的原因是
②图中M点CO2的平衡转化率为60%,若CH3OH的选择性为
 (转化的CO2中生成CH3OH的百分比,则该温度下容器中H2O(g)的平衡分压为
(转化的CO2中生成CH3OH的百分比,则该温度下容器中H2O(g)的平衡分压为Ⅱ.以甲醇和二氧化碳为原料,利用活性催化电极电解制备甲酸(甲酸盐)的原理如图。

(3)该装置中电子流动方向是
(4)电解过程中阴极的电极反应式为
(5)若有1molH+通过质子交换膜时,装置内生成HCOOˉ和HCOOH的物质的量的差为
您最近一年使用:0次
【推荐3】回答下列问题:
(1)在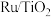 催化下发生反应:
催化下发生反应: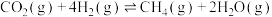 假定未发生其他反应,350℃时向1 L恒容密闭容器中充入1 mol
假定未发生其他反应,350℃时向1 L恒容密闭容器中充入1 mol  和4 mol
和4 mol  ,初始总压强为5a MPa,反应进行到5min时,
,初始总压强为5a MPa,反应进行到5min时, 与
与 分压相等,10min后反应达到平衡,测得
分压相等,10min后反应达到平衡,测得 与
与 的平衡分压比为1:3(分压=总压×组分物质的量分数)。
的平衡分压比为1:3(分压=总压×组分物质的量分数)。
①下列能表明该反应已经达到平衡的有___________ 。
A.气体的密度不再发生变化 B.单位体积内分子总数不变
C.混合气体的平均相对分子质量不变 D. 与
与 的物质的量之和不变
的物质的量之和不变
②0~5min内,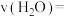
___________ 。该反应的平衡常数
___________  。
。
(2) 与
与 可以直接制备甲醇,其中的主要过程包括以下反应:
可以直接制备甲醇,其中的主要过程包括以下反应:
①


②


在其他条件相同的情况下,用新型催化剂可以显著提高甲醇的选择性,使用该催化剂,按 投料于恒容密闭容器中进行反应,
投料于恒容密闭容器中进行反应, 的平衡转化率和甲醇的选择率随温度的变化趋势如图所示:(忽略温度对催化剂的影响)
的平衡转化率和甲醇的选择率随温度的变化趋势如图所示:(忽略温度对催化剂的影响)
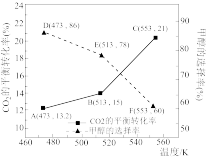
①根据图中数据,温度选择___________ K,达到平衡时,反应体系内甲醇的产量最高。
②随着温度的升高, 的平衡转化率增加但甲醇的选择率降低,请分析其原因
的平衡转化率增加但甲醇的选择率降低,请分析其原因___________ 。
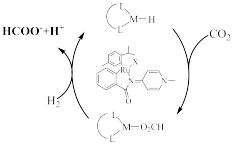
(3)利用 在新型钌配合物催化剂下加氢合成甲酸,反应机理如图所示,图中含Ru配合物的某段结构用M表示。研究表明,极性溶剂有助于促进
在新型钌配合物催化剂下加氢合成甲酸,反应机理如图所示,图中含Ru配合物的某段结构用M表示。研究表明,极性溶剂有助于促进 进入M-H键,使用极性溶剂后极大地提高了整个反应的合成效率,原因是
进入M-H键,使用极性溶剂后极大地提高了整个反应的合成效率,原因是___________
(1)在
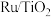 催化下发生反应:
催化下发生反应: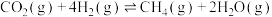 假定未发生其他反应,350℃时向1 L恒容密闭容器中充入1 mol
假定未发生其他反应,350℃时向1 L恒容密闭容器中充入1 mol  和4 mol
和4 mol  ,初始总压强为5a MPa,反应进行到5min时,
,初始总压强为5a MPa,反应进行到5min时, 与
与 分压相等,10min后反应达到平衡,测得
分压相等,10min后反应达到平衡,测得 与
与 的平衡分压比为1:3(分压=总压×组分物质的量分数)。
的平衡分压比为1:3(分压=总压×组分物质的量分数)。①下列能表明该反应已经达到平衡的有
A.气体的密度不再发生变化 B.单位体积内分子总数不变
C.混合气体的平均相对分子质量不变 D.
 与
与 的物质的量之和不变
的物质的量之和不变②0~5min内,
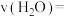

 。
。(2)
 与
与 可以直接制备甲醇,其中的主要过程包括以下反应:
可以直接制备甲醇,其中的主要过程包括以下反应:①



②



在其他条件相同的情况下,用新型催化剂可以显著提高甲醇的选择性,使用该催化剂,按
 投料于恒容密闭容器中进行反应,
投料于恒容密闭容器中进行反应, 的平衡转化率和甲醇的选择率随温度的变化趋势如图所示:(忽略温度对催化剂的影响)
的平衡转化率和甲醇的选择率随温度的变化趋势如图所示:(忽略温度对催化剂的影响)

①根据图中数据,温度选择
②随着温度的升高,
 的平衡转化率增加但甲醇的选择率降低,请分析其原因
的平衡转化率增加但甲醇的选择率降低,请分析其原因(3)利用
 在新型钌配合物催化剂下加氢合成甲酸,反应机理如图所示,图中含Ru配合物的某段结构用M表示。研究表明,极性溶剂有助于促进
在新型钌配合物催化剂下加氢合成甲酸,反应机理如图所示,图中含Ru配合物的某段结构用M表示。研究表明,极性溶剂有助于促进 进入M-H键,使用极性溶剂后极大地提高了整个反应的合成效率,原因是
进入M-H键,使用极性溶剂后极大地提高了整个反应的合成效率,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】中国航空航天事业飞速发展,银铜合金广泛用于航空工业。从银铜合金切割废料中回收银并制备铜化工产品的工艺如下:

注:A1(OH)3和Cu(OH)2分解温度分别为450℃和80℃
(1)在电解精炼银时,阳极材料为___________ 。
(2)加快渣料(含少量银)溶于稀H2SO4速率的措施为___________ (写出两种)。
(3)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,滤渣A与稀HNO3反应的离子方程式为______________________ 。
(4)过滤操作需要的玻璃仪器除烧杯外还有___________ 。
(5)固体混合物B的组成为___________ ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为___________ 。
(6)煅烧阶段通入惰性气体的原因___________ 。

注:A1(OH)3和Cu(OH)2分解温度分别为450℃和80℃
(1)在电解精炼银时,阳极材料为
(2)加快渣料(含少量银)溶于稀H2SO4速率的措施为
(3)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,滤渣A与稀HNO3反应的离子方程式为
(4)过滤操作需要的玻璃仪器除烧杯外还有
(5)固体混合物B的组成为
(6)煅烧阶段通入惰性气体的原因
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】己二腈[NC(CH2)4CN]是制造“尼龙-66”(聚己二酰己二胺)的原料,工业需求量大。其制备工艺很多,发展前景较好的是利用丙烯腈(CH2=CHCN)电合成己二腈。
Ⅰ.制备丙烯腈
以3﹣羟基丙酸乙酯通过腈化反应合成丙烯腈,产率达90%~92%,远高于目前丙烯法。其反应过程如图:___________ (填“高温”“低温”或“任意温度”)条件下可自发进行。
(2)能提高丙烯腈的平衡产率的措施有___________ 。(写两种)
(3)向总压为p0kPa的恒压密闭容器中加入催化剂,按投料比 加入反应物,测得平衡时体系中含碳物质(除乙醇)的物质的量分数随温度的变化如图所示[A的物质的量分数=
加入反应物,测得平衡时体系中含碳物质(除乙醇)的物质的量分数随温度的变化如图所示[A的物质的量分数= ×100%]。
×100%]。___________ 。
②a点对应反应ⅰ的Kp=___________ kPa(用含p0的代数式表示)。
Ⅱ.丙烯腈电合成己二腈: [NC(CH2)4CN]
电解原理如图甲所示(两极均采用惰性电极),电解过程中主要副产物为丙腈(C2H5CN)。实验测得,向B极区电解液中加入少量季铵盐,并调pH为8,此时己二腈的产率最高。___________ 极(填“阳”或“阴”),写出B电极上①的电极反应式:___________ 。
(5)B极区溶液呈酸性会导致己二腈的产率降低,原因可能为___________ 。
(6)己二腈、丙腈的生成速率与加入季铵盐的浓度关系如图乙所示(纵坐标的单位是10-3mol/h)。当季铵盐的浓度为1.5×10-2mol/L时,通过质子交换膜的H+的物质的量为___________ mol。
Ⅰ.制备丙烯腈
以3﹣羟基丙酸乙酯通过腈化反应合成丙烯腈,产率达90%~92%,远高于目前丙烯法。其反应过程如图:
ⅰ.

 +H2O(g) ΔH1>0
+H2O(g) ΔH1>0
ⅱ. +NH3(g)
+NH3(g)
 +H2O(g)+
+H2O(g)+ ΔH2>0
ΔH2>0
(2)能提高丙烯腈的平衡产率的措施有
(3)向总压为p0kPa的恒压密闭容器中加入催化剂,按投料比
 加入反应物,测得平衡时体系中含碳物质(除乙醇)的物质的量分数随温度的变化如图所示[A的物质的量分数=
加入反应物,测得平衡时体系中含碳物质(除乙醇)的物质的量分数随温度的变化如图所示[A的物质的量分数= ×100%]。
×100%]。
②a点对应反应ⅰ的Kp=
Ⅱ.丙烯腈电合成己二腈: [NC(CH2)4CN]
电解原理如图甲所示(两极均采用惰性电极),电解过程中主要副产物为丙腈(C2H5CN)。实验测得,向B极区电解液中加入少量季铵盐,并调pH为8,此时己二腈的产率最高。

(5)B极区溶液呈酸性会导致己二腈的产率降低,原因可能为
(6)己二腈、丙腈的生成速率与加入季铵盐的浓度关系如图乙所示(纵坐标的单位是10-3mol/h)。当季铵盐的浓度为1.5×10-2mol/L时,通过质子交换膜的H+的物质的量为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】粉煤灰的综合利既有利于节约资源又有利于保护环境。某粉煤灰(主要含Al2O3、Fe2O3、CaCO3等)的铝、铁分离工艺流程如下:

(1)①“酸浸”时Al2O3发生反应的离子方程式为___________________________ 。
②当硫酸质量分数大于50%,金属氧化物浸出率明显下降。其原因_____________________ 。
(2)有关金属离子以氢氧化物沉淀时离子浓度随pH变化如图所示。若浸出液不经还原直接与氨水混合,铝、铁元素分离效果较差的原因是____________________________ 。

(3)“再生”过程中,[Fe(NO)2]2+在微生物的作用下与C6H12O6发生反应的离子方程式为______ 。
(4)Al(OH)3经过一系列反应可获得粗铝,利用熔融状态下物质密度不同,通过三层液电解精炼法可由粗铝获得高纯铝(装置如图所示)。

①该装置工作时,电极A作______ 极。
②熔融粗铝时加入铜的作用是_________________________________ 。

(1)①“酸浸”时Al2O3发生反应的离子方程式为
②当硫酸质量分数大于50%,金属氧化物浸出率明显下降。其原因
(2)有关金属离子以氢氧化物沉淀时离子浓度随pH变化如图所示。若浸出液不经还原直接与氨水混合,铝、铁元素分离效果较差的原因是

(3)“再生”过程中,[Fe(NO)2]2+在微生物的作用下与C6H12O6发生反应的离子方程式为
(4)Al(OH)3经过一系列反应可获得粗铝,利用熔融状态下物质密度不同,通过三层液电解精炼法可由粗铝获得高纯铝(装置如图所示)。

①该装置工作时,电极A作
②熔融粗铝时加入铜的作用是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】按要求对下图中两极进行必要的联接并填空:

(1)在A 图中,使铜片上冒H2气泡。请加以必要联接①______ (在答题卡的图中画线),则联接后的装置叫②______ 。电极反应式: 锌板:③_______ ; 铜板:④_______ 。
(2)在B 图中(a、b均为惰性电极),使a 极析出铜,则b析出①______ 。加以必要的联接后,该装置叫②_____ 。电极反应式: a 极:③_______ b 极:④___________ 。经过一段时间后,停止反应并搅匀溶液,溶液的pH 值⑤______ ( 升高、降低、不变),加入一定量的⑥_____ 后,溶液能恢复至与电解前完全一致。

(1)在A 图中,使铜片上冒H2气泡。请加以必要联接①
(2)在B 图中(a、b均为惰性电极),使a 极析出铜,则b析出①
您最近一年使用:0次
【推荐2】二氧化碳与氢气在一定条件下可制备甲醛(HCHO)、甲酸(HCOOH)和甲醇( )等有机物。回答下列问题:
)等有机物。回答下列问题:
(1)制备甲醛:反应机理如下图所示
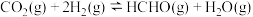

___________ (用 、
、 、
、 、
、 表示)。
表示)。
②将等物质的量的 与
与 充入恒温恒容密闭容器中发生反应
充入恒温恒容密闭容器中发生反应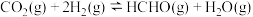 ,下列描述不能说明该反应达到平衡状态的是
,下列描述不能说明该反应达到平衡状态的是___________ (填字母)。
a. 的物质的量保持不变
的物质的量保持不变
b.单位时间内,断裂2molH—H键的同时断裂2molC—H键
C. 不再发生变化
不再发生变化
d.容器内混合气体的密度保持不变
(2)制备甲酸:反应原理为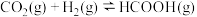
 。已知:
。已知: ,
, ,
, 、
、 为速率常数,
为速率常数,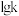 与温度的关系如下图所示。
与温度的关系如下图所示。
___________ (填“增大”“减小”或“不变”);该反应的
___________ (填“ ”“
”“ ”或“
”或“ ”)0。
”)0。
②向某恒容密闭容器中加入物质的量均为1mol的 和
和 发生该反应,
发生该反应, 时平衡常数为20、平衡压强为
时平衡常数为20、平衡压强为 ,若温度为
,若温度为 时,
时, ,则
,则 时的平衡压强
时的平衡压强___________ (填“ ”“
”“ ”或“
”或“ ”)
”) 。
。
(3)近年来,有研究人员用 通过电催化生成
通过电催化生成 ,实现
,实现 的回收利用,其工作原理如下图所示。写出Cu电极上的电极反应式:
的回收利用,其工作原理如下图所示。写出Cu电极上的电极反应式:___________ 。 用于制备苯乙烯有助于实现“碳中和”。
用于制备苯乙烯有助于实现“碳中和”。 参与反应的机理如上图所示(
参与反应的机理如上图所示( 、
、 表示乙苯分子中C或H原子的位置;AB为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置;AB为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。根据元素电负性的变化规律,上图所示的反应机理中步骤Ⅰ和步骤Ⅱ可描述为乙苯
位点带部分负电荷)。根据元素电负性的变化规律,上图所示的反应机理中步骤Ⅰ和步骤Ⅱ可描述为乙苯 带部分正电荷,被带部分负电荷的
带部分正电荷,被带部分负电荷的 位点吸引,随后解离出
位点吸引,随后解离出 并吸附在
并吸附在 位点上;
位点上;___________ 。
②保持混合气体总压(p)等其他条件不变, 的分压
的分压 与乙苯转化率的关系如下图所示。
与乙苯转化率的关系如下图所示。 时,乙苯转化率下降的原因是
时,乙苯转化率下降的原因是___________ 。
 )等有机物。回答下列问题:
)等有机物。回答下列问题:(1)制备甲醛:反应机理如下图所示


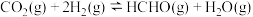

 、
、 、
、 、
、 表示)。
表示)。②将等物质的量的
 与
与 充入恒温恒容密闭容器中发生反应
充入恒温恒容密闭容器中发生反应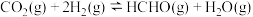 ,下列描述不能说明该反应达到平衡状态的是
,下列描述不能说明该反应达到平衡状态的是a.
 的物质的量保持不变
的物质的量保持不变b.单位时间内,断裂2molH—H键的同时断裂2molC—H键
C.
 不再发生变化
不再发生变化d.容器内混合气体的密度保持不变
(2)制备甲酸:反应原理为
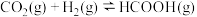
 。已知:
。已知: ,
, ,
, 、
、 为速率常数,
为速率常数,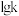 与温度的关系如下图所示。
与温度的关系如下图所示。


 ”“
”“ ”或“
”或“ ”)0。
”)0。②向某恒容密闭容器中加入物质的量均为1mol的
 和
和 发生该反应,
发生该反应, 时平衡常数为20、平衡压强为
时平衡常数为20、平衡压强为 ,若温度为
,若温度为 时,
时, ,则
,则 时的平衡压强
时的平衡压强 ”“
”“ ”或“
”或“ ”)
”) 。
。(3)近年来,有研究人员用
 通过电催化生成
通过电催化生成 ,实现
,实现 的回收利用,其工作原理如下图所示。写出Cu电极上的电极反应式:
的回收利用,其工作原理如下图所示。写出Cu电极上的电极反应式:
 用于制备苯乙烯有助于实现“碳中和”。
用于制备苯乙烯有助于实现“碳中和”。
 参与反应的机理如上图所示(
参与反应的机理如上图所示( 、
、 表示乙苯分子中C或H原子的位置;AB为催化剂的活性位点,其中A位点带部分正电荷,
表示乙苯分子中C或H原子的位置;AB为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。根据元素电负性的变化规律,上图所示的反应机理中步骤Ⅰ和步骤Ⅱ可描述为乙苯
位点带部分负电荷)。根据元素电负性的变化规律,上图所示的反应机理中步骤Ⅰ和步骤Ⅱ可描述为乙苯 带部分正电荷,被带部分负电荷的
带部分正电荷,被带部分负电荷的 位点吸引,随后解离出
位点吸引,随后解离出 并吸附在
并吸附在 位点上;
位点上;②保持混合气体总压(p)等其他条件不变,
 的分压
的分压 与乙苯转化率的关系如下图所示。
与乙苯转化率的关系如下图所示。 时,乙苯转化率下降的原因是
时,乙苯转化率下降的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】氨气广泛应用于化肥、制药、合成纤维等领域。
Ⅰ.工业上可由氢气和氮气合成氨气。若用 、
、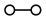 、
、 、
、 分别表示N2、H2、NH3和催化剂,则在催化剂表面合成氨的过程如下图所示:
分别表示N2、H2、NH3和催化剂,则在催化剂表面合成氨的过程如下图所示:

(1)吸附后,能量状态最高的是_______ (填序号)。
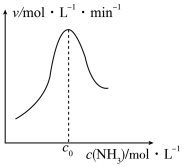
(2)结合上述过程,一定温度下在固体催化剂表面进行NH3的分解实验,发现NH3的分解速率与浓度的关系如下图所示。从吸附和解吸过程分析 ,c0前反应速率增加的原因可能是_______ ;c0之后反应速率降低的原因可能是_______ 。
Ⅱ.利用NH3在催化剂(V2O5-WO3/TiO2)作用下将NOx还原为N2是目前应用最为广泛的氮氧化物NOx的净化方法,其原理是:
主反应:4NH3(g) +4NO(g)+O2(g) 4N2(g)+6H2O(g) ΔH1
4N2(g)+6H2O(g) ΔH1
副反应:4NH3(g)+ 3O2(g) 2N2(g)+6H2O(g) ΔH2
2N2(g)+6H2O(g) ΔH2
(3)根据盖斯定律可得:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) ΔH3。则ΔH3=
5N2(g)+6H2O(g) ΔH3。则ΔH3=_______ (用含ΔH1、ΔH2的式子表示)。
(4)向脱硝反应的体系中添加NH4NO3可显著提高NO脱除率,原因可用一组离子方程式表示,请补充其中的1个离子方程式。(已知含氮微粒最终转化为N2)
① NO + NO = NO2 + NO
+ NO = NO2 + NO
② NO2 + 2NH = NO2(NH
= NO2(NH )2;
)2;_______
③ NO2(NH )2 + NO = 2N2 +3H2O + 2H+
)2 + NO = 2N2 +3H2O + 2H+
④ NH3 + H+ = NH
(5)化学反应的浓度商(用符号Qc表示)是可逆反应进行到一定程度,产物浓度的系数次方的乘积与反应物浓度系数次方的乘积之比;达平衡时,浓度商就等于平衡常数K。若反应容器的体积固定不变,在坐标系中画出从常温时通入4 mol NH3和6 mol NO开始(仅发生反应:4NH3(g)+6NO(g) 5N2(g) + 6H2O(g) ΔH3<0),随温度(T/K)不断升高,浓度商Qc的变化趋势图
5N2(g) + 6H2O(g) ΔH3<0),随温度(T/K)不断升高,浓度商Qc的变化趋势图_______ 。
(6)氮氧化物脱除还可以利用电化学原理处理,利用如下图装置可同时吸收SO2和NO。已知:H2S2O4是一种弱酸。

阴极的电极反应式为_______ ,若没有能量损失,相同条件下,SO2和NO的体积比为_______ 时,两种气体都能被完全处理。
Ⅰ.工业上可由氢气和氮气合成氨气。若用
 、
、 、
、 、
、 分别表示N2、H2、NH3和催化剂,则在催化剂表面合成氨的过程如下图所示:
分别表示N2、H2、NH3和催化剂,则在催化剂表面合成氨的过程如下图所示:
(1)吸附后,能量状态最高的是
(2)结合上述过程,一定温度下在固体催化剂表面进行NH3的分解实验,发现NH3的分解速率与浓度的关系如下图所示。从

Ⅱ.利用NH3在催化剂(V2O5-WO3/TiO2)作用下将NOx还原为N2是目前应用最为广泛的氮氧化物NOx的净化方法,其原理是:
主反应:4NH3(g) +4NO(g)+O2(g)
 4N2(g)+6H2O(g) ΔH1
4N2(g)+6H2O(g) ΔH1副反应:4NH3(g)+ 3O2(g)
 2N2(g)+6H2O(g) ΔH2
2N2(g)+6H2O(g) ΔH2(3)根据盖斯定律可得:4NH3(g)+6NO(g)
 5N2(g)+6H2O(g) ΔH3。则ΔH3=
5N2(g)+6H2O(g) ΔH3。则ΔH3=(4)向脱硝反应的体系中添加NH4NO3可显著提高NO脱除率,原因可用一组离子方程式表示,请补充其中的1个离子方程式。(已知含氮微粒最终转化为N2)
① NO
 + NO = NO2 + NO
+ NO = NO2 + NO
② NO2 + 2NH
 = NO2(NH
= NO2(NH )2;
)2;③ NO2(NH
 )2 + NO = 2N2 +3H2O + 2H+
)2 + NO = 2N2 +3H2O + 2H+④ NH3 + H+ = NH

(5)化学反应的浓度商(用符号Qc表示)是可逆反应进行到一定程度,产物浓度的系数次方的乘积与反应物浓度系数次方的乘积之比;达平衡时,浓度商就等于平衡常数K。若反应容器的体积固定不变,在坐标系中画出从常温时通入4 mol NH3和6 mol NO开始(仅发生反应:4NH3(g)+6NO(g)
 5N2(g) + 6H2O(g) ΔH3<0),随温度(T/K)不断升高,浓度商Qc的变化趋势图
5N2(g) + 6H2O(g) ΔH3<0),随温度(T/K)不断升高,浓度商Qc的变化趋势图
(6)氮氧化物脱除还可以利用电化学原理处理,利用如下图装置可同时吸收SO2和NO。已知:H2S2O4是一种弱酸。

阴极的电极反应式为
您最近一年使用:0次



