名校
解题方法
1 . 电池的发明和应用是化学家们对人类社会的重要贡献之一、每一次化学电池技术的突破,都带来了电子设备革命性的发展。最近,我国在甲烷燃料电池的相关技术上获得了新突破,原理如下图所示:

(1)通甲烷燃料一极的电极反应式为_______ 。
(2)以石墨做电极电解Na2SO4溶液,如图2所示,电解开始后先出现红色的一极的电极反应式为_______ 。
(3)随着电池使用范围的日益扩大,废旧电池潜在的污染已引起社会各界的广泛关注。工业上为了处理含有 的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
①氧化还原过程的离子方程式为_______ 。
②常温下,Cr(OH)3的溶度积Ksp=1×10-32 mol4·L-4,溶液的pH至少为_______ ,才能使Cr3+沉淀完全(溶液中离子浓度小于10-5 mol/L时,可视为完全沉淀)。
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。
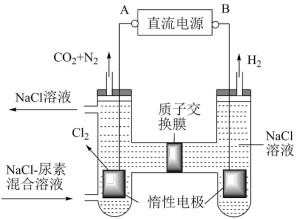
①电源的正极为_______ (填“A”或“B”)。
②电解结束后,阴极室溶液的pH与电解前相比将_______ (填“增大”、“减小”、“不变”);若收集到H2 2.24L(标准状况),则通过质子交换膜的H+数目为_______ (忽略气体的溶解)。

(1)通甲烷燃料一极的电极反应式为
(2)以石墨做电极电解Na2SO4溶液,如图2所示,电解开始后先出现红色的一极的电极反应式为
(3)随着电池使用范围的日益扩大,废旧电池潜在的污染已引起社会各界的广泛关注。工业上为了处理含有
 的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。①氧化还原过程的离子方程式为
②常温下,Cr(OH)3的溶度积Ksp=1×10-32 mol4·L-4,溶液的pH至少为
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。

①电源的正极为
②电解结束后,阴极室溶液的pH与电解前相比将
您最近一年使用:0次
名校
解题方法
2 . 按照要求回答下列问题。
(1)工业上,在强碱性条件下用电解法除去废水中的 ,装置如图所示,依次发生的反应有:
,装置如图所示,依次发生的反应有:
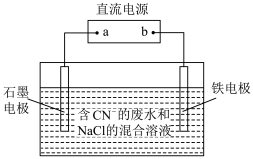
i.
ii.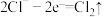
iii.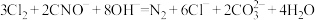
①a为电源_______ 极。
②通电过程中溶液pH不断_______ (填“增大”“减小”或“不变”)。
③除去1mol ,外电路中至少需要转移
,外电路中至少需要转移_______ mol电子。
④为了使电解池连续工作,需要不断补充_______ 。
(2)用NaOH溶液吸收烟气中的 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到
溶液进行电解,可循环再生NaOH,同时得到 ,其原理如图所示(电极材料为石墨)。
,其原理如图所示(电极材料为石墨)。
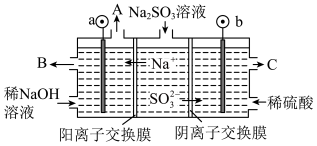
① C口流出的物质是_______ 。
② 放电的电极反应式为
放电的电极反应式为_______ 。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因:_______ 。
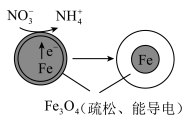
(3)用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一、Fe还原水体中的
)已成为环境修复研究的热点之一、Fe还原水体中的 的反应原理如图所示。正极的电极反应式是
的反应原理如图所示。正极的电极反应式是_______ 。
(1)工业上,在强碱性条件下用电解法除去废水中的
 ,装置如图所示,依次发生的反应有:
,装置如图所示,依次发生的反应有:
i.

ii.
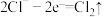
iii.
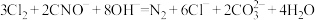
①a为电源
②通电过程中溶液pH不断
③除去1mol
 ,外电路中至少需要转移
,外电路中至少需要转移④为了使电解池连续工作,需要不断补充
(2)用NaOH溶液吸收烟气中的
 ,将所得的
,将所得的 溶液进行电解,可循环再生NaOH,同时得到
溶液进行电解,可循环再生NaOH,同时得到 ,其原理如图所示(电极材料为石墨)。
,其原理如图所示(电极材料为石墨)。
① C口流出的物质是
②
 放电的电极反应式为
放电的电极反应式为③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因:
(3)用零价铁(Fe)去除水体中的硝酸盐(
 )已成为环境修复研究的热点之一、Fe还原水体中的
)已成为环境修复研究的热点之一、Fe还原水体中的 的反应原理如图所示。正极的电极反应式是
的反应原理如图所示。正极的电极反应式是
您最近一年使用:0次
解题方法
3 . 某课外活动小组用如图所示装置进行实验,试回答下列问题:
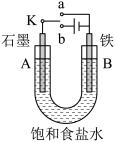
(1)若开始时开关K与a连接,则B极的电极反应式为_______ 。
(2)若开始时开关K与b极连接,此装置为______ (原电池或电解池)总反应的离子方程式为_______ 。
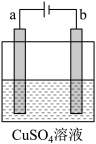
(3)如图所示用惰性电极电解100 mL 0.5 mol·L 硫酸铜溶液,a电极上的电极反应式为
硫酸铜溶液,a电极上的电极反应式为_______ ,若a电极产生56 mL(标准状况)气体,则所得溶液的
_______ (不考虑溶液体积变化)。

(1)若开始时开关K与a连接,则B极的电极反应式为
(2)若开始时开关K与b极连接,此装置为
(3)如图所示用惰性电极电解100 mL 0.5 mol·L
 硫酸铜溶液,a电极上的电极反应式为
硫酸铜溶液,a电极上的电极反应式为

您最近一年使用:0次
名校
解题方法
4 . 利用氧化还原反应可以解决很多实际问题:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O
(1)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol/L盐桥中装有饱和溶液。K2SO4回答下列问题:
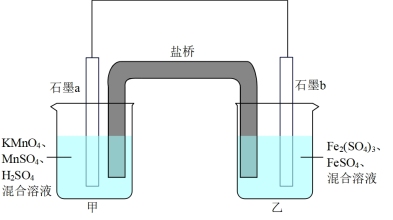
①发生氧化反应的烧杯是_______ (填“甲”或“乙”)。
②外电路的电流方向为:从_______ 。(用“a”“b”表示)
③电池工作时,盐桥中的SO 移向
移向_______ (填“甲”或“乙”)烧杯。
④甲烧杯中发生的电极反应_______ 。
(2)工业上处理含Cr2O 的酸性工业废水常用以下方法:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准。
的酸性工业废水常用以下方法:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准。
①电解时的电极反应:阳极_______ ,阴极_______ 。
②Cr2O 转变成Cr3+的离子反应方程式:
转变成Cr3+的离子反应方程式:_______ 。
(3)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。
①放电时负极的电极反应为:_______ ;放电时电解质溶液的pH逐渐_______ ;(填“增大”或“减小”)
②充电时有CH3OH生成的电极为_______ 极; 填“阴极”或阳极
填“阴极”或阳极 充电时每生成1 molCH3OH转移
充电时每生成1 molCH3OH转移_______ mol电子
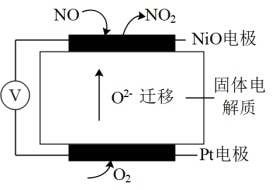
(4)通过NOx传感器可监测NOx的含量,工作原理示意图如图所示,Pt电极上发生的是_______ 反应(填“氧化”或“还原”)。写出NiO电极的电极反应式:_______ 。
(1)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol/L盐桥中装有饱和溶液。K2SO4回答下列问题:

①发生氧化反应的烧杯是
②外电路的电流方向为:从
③电池工作时,盐桥中的SO
 移向
移向④甲烧杯中发生的电极反应
(2)工业上处理含Cr2O
 的酸性工业废水常用以下方法:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准。
的酸性工业废水常用以下方法:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准。①电解时的电极反应:阳极
②Cr2O
 转变成Cr3+的离子反应方程式:
转变成Cr3+的离子反应方程式:(3)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。
①放电时负极的电极反应为:
②充电时有CH3OH生成的电极为
 填“阴极”或阳极
填“阴极”或阳极 充电时每生成1 molCH3OH转移
充电时每生成1 molCH3OH转移(4)通过NOx传感器可监测NOx的含量,工作原理示意图如图所示,Pt电极上发生的是

您最近一年使用:0次
名校
解题方法
5 . 为了探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示的装置进行实验,回答下列问题。
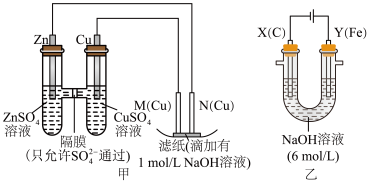
Ⅰ.用甲装置进行第一组实验:
(1)实验过程中,
________ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有___________________ 。
(2)该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子( )在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和
)在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和_________________ 。
II.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,根据要求回答相关问题:
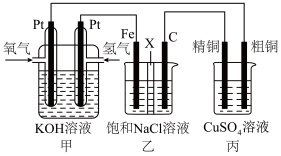
(1)若在标准状况下,甲装置有448mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为____
(2)若用隔膜法电解饱和食盐水生成NaClO,则X应用________ 交换膜(填“阳离子”或“阴离子”)
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将_______ (填“增大”“减 小”或“不变”)
III.以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图.
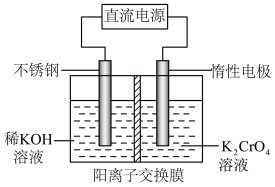
(1)不锈钢作_________ 极
(2)分析阳极区能得到重铬酸钾溶液的原因________________________________________________ 。

Ⅰ.用甲装置进行第一组实验:
(1)实验过程中,

(2)该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(
 )在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和
)在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和II.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,根据要求回答相关问题:

(1)若在标准状况下,甲装置有448mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为
(2)若用隔膜法电解饱和食盐水生成NaClO,则X应用
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
III.以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图.

(1)不锈钢作
(2)分析阳极区能得到重铬酸钾溶液的原因
您最近一年使用:0次
名校
解题方法
6 . 如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。请按要求回答相关问题:
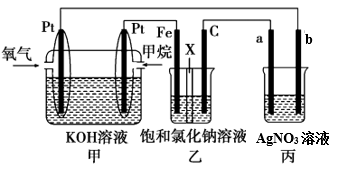
(1)甲装置电池负极发生的电极反应式是:_______
(2)乙中X是_______ (阴、阳)离子交换膜,向乙中加入几滴酚酞溶液,工作一段时间后铁电极附近溶液变红,请用化学用语解释相关原因_______
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成的气体的物质的量为_______
(4)若丙装置中a、b电极均为Cu,则丙中发生的离子反应是_______
(5)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解 的原理如图所示
的原理如图所示
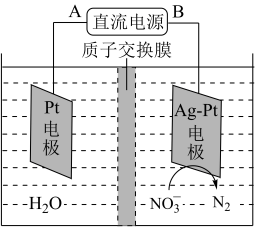
Ag-Pt电极上的电极反应式为_______

(1)甲装置电池负极发生的电极反应式是:
(2)乙中X是
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成的气体的物质的量为
(4)若丙装置中a、b电极均为Cu,则丙中发生的离子反应是
(5)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解
 的原理如图所示
的原理如图所示
Ag-Pt电极上的电极反应式为
您最近一年使用:0次
2021-02-15更新
|
120次组卷
|
2卷引用:宁夏吴忠中学2020-2021学年高二上学期期末考试化学试题
名校
7 . 为探究原电池和电解池的工作原理,某研究性小组分别用如图所示装置进行实验。
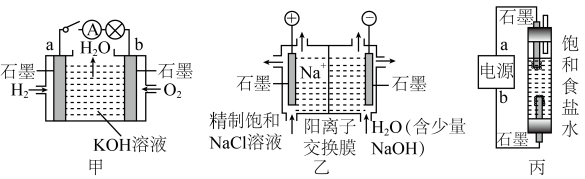
(1)甲装置中,a电极的反应式为_______________________________________ 。
(2)乙装置中,阴极区产物为________ 和_______ 。
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为_______ (填“正”或“负”)极,该装置内,发生的电解方程式为___________________________________ 、生成消毒液的方程式为________________________________________________________ 。
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为___________ (不考虑气体的溶解)。
(5)某工厂采用电解法处理含Cr2O72-的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,Cr2O72-被还原成为Cr3+,Cr3+在阴极区生成Cr(OH)3沉淀除去,工作原理如图:
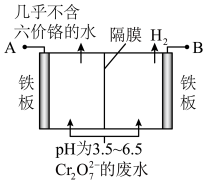
①写出电解时阳极的电极反应式:______________________________________ 。
②写出Cr2O72-被还原为Cr3+的离子方程式:____________________________________ 。

(1)甲装置中,a电极的反应式为
(2)乙装置中,阴极区产物为
(3)丙装置是一种家用环保型消毒液发生器。外接电源a为
(4)若甲装置作为乙装置的电源,一段时间后,甲中消耗气体与乙中产生气体的物质的量之比为
(5)某工厂采用电解法处理含Cr2O72-的废水,耐酸电解槽用铁板作阴、阳极,槽内盛放含铬废水,Cr2O72-被还原成为Cr3+,Cr3+在阴极区生成Cr(OH)3沉淀除去,工作原理如图:

①写出电解时阳极的电极反应式:
②写出Cr2O72-被还原为Cr3+的离子方程式:
您最近一年使用:0次
名校
解题方法
8 . 如图是一个电化学过程的示意图.请回答下列问题:
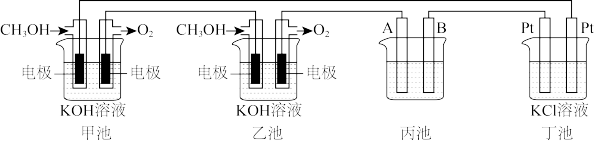
(1)通入CH3OH的电极的电极反应式为_______ .
(2)丙池是铜的精炼池,电解一段时间后烧杯中的溶液浓度会_______ (填“增大、减小、不变”),A电极反应式_______ (已知粗铜中含有Zn,Ag杂质).
(3)丁池中滴有酚酞,实验开始后观察到的现象_______ ,丁池采用无隔膜电解,产生的氯气可能会与KOH溶液接触仅得到KClO和H2,则相应的化学反应方程式为_______ 。
(4)若甲、乙两个电池氧气通入量均为20L(标准状况),且反应完全,则理论上通过丁池的电量为_______ (法拉第常数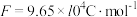 ),丁池最多能产生气体的总体积为
),丁池最多能产生气体的总体积为_______ L(标准状况)。

(1)通入CH3OH的电极的电极反应式为
(2)丙池是铜的精炼池,电解一段时间后烧杯中的溶液浓度会
(3)丁池中滴有酚酞,实验开始后观察到的现象
(4)若甲、乙两个电池氧气通入量均为20L(标准状况),且反应完全,则理论上通过丁池的电量为
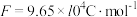 ),丁池最多能产生气体的总体积为
),丁池最多能产生气体的总体积为
您最近一年使用:0次
名校
解题方法
9 . 如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.根据要求回答相关问题:
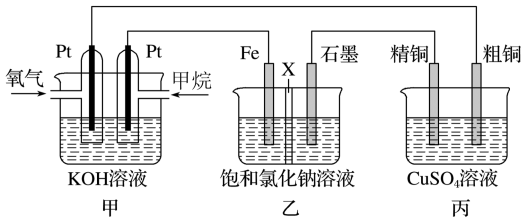
(1)甲烷燃料电池的负极反应式______ .
(2)石墨电极(C)的电极反应式为______ .
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将______ (填“增大”“减小”或“不变”).
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成标况下气体的的体积为______ ;丙装置中阴极析出铜的质量为______ .

(1)甲烷燃料电池的负极反应式
(2)石墨电极(C)的电极反应式为
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
(4)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成标况下气体的的体积为
您最近一年使用:0次



