1 . 化合物X 由两种元素组成,相对分子质量的范围在100~200间,所有数据均为标准状况下测得,部分产物省略。
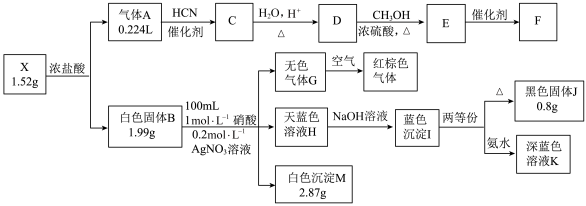
已知:气体A 是一种常见的烃, B 为二元化合物, E→F 为加聚反应。
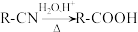
(1)白 色 固 体B 的化学式为_________ ;X 的 化 学 式 为_________ 。
(2)A→C的反应类型为________ ; F的结构简式为_________ 。
(3)下列说法正确的是
(4)①写出由沉淀 I 到深蓝色溶液 K 的离子方程式_________ 。②写出D→E 反应的化学方程式_________ 。
(5)根据H→I→K 的现象,给出相应的三种微粒与阳离子结合由弱到强的排序_________ 。

已知:气体A 是一种常见的烃, B 为二元化合物, E→F 为加聚反应。
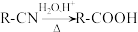
(1)白 色 固 体B 的化学式为
(2)A→C的反应类型为
(3)下列说法正确的是
| A.实验室可用电石和饱和食盐水来制备气体A | B.化合物D 不能使溴水褪色 |
| C.无色气体G 是酸性氧化物 | D.白色沉淀M 中加入氨水后能溶解 |
(5)根据H→I→K 的现象,给出相应的三种微粒与阳离子结合由弱到强的排序
您最近一年使用:0次
解题方法
2 . 有机物A产量可衡量一个国家的石化水平,聚氯乙烯是生活中常用的塑料,工业生产聚氯乙烯的一种工艺路线如下:
(1)A的结构简式为:_______ ;
(2)已知: ,则A与酸性高锰酸钾反应的离子方程式为
,则A与酸性高锰酸钾反应的离子方程式为_______ 。
(3)氯乙烯所含官能团为_______ 。
(4)反应③的化学方程式为_______ ,反应类型为_______ 。
(5)乙烯的一种同系物的键线式为 ,请用系统命名法为其命名
,请用系统命名法为其命名_______ 。
(6)工业上合成聚氯乙烯还可以采用另一种不饱和气态烃与氯化氢为原料,实验室制备该气态烃的方程式为_______ 。

(1)A的结构简式为:
(2)已知:
 ,则A与酸性高锰酸钾反应的离子方程式为
,则A与酸性高锰酸钾反应的离子方程式为(3)氯乙烯所含官能团为
(4)反应③的化学方程式为
(5)乙烯的一种同系物的键线式为
 ,请用系统命名法为其命名
,请用系统命名法为其命名(6)工业上合成聚氯乙烯还可以采用另一种不饱和气态烃与氯化氢为原料,实验室制备该气态烃的方程式为
您最近一年使用:0次
3 . 有机高分子材料PMA可用于制备复合玻璃,其合成路线如图所示。
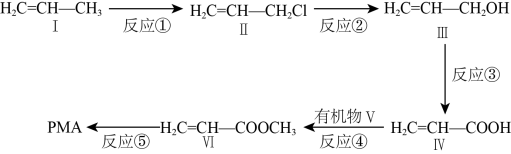
回答下列问题:
(1)反应Ⅰ的试剂和条件是___________
(2)反应②的反应类型为___________ (选填“取代反应”或“加成反应”)。
(3)化合物Ⅲ中所含官能团的名称为___________ 、___________ 。
(4)下列有关化合物的说法正确的是___________。
(5)写出反应④的化学方程式___________ 。
(6)PMA的结构简式为___________ 。

回答下列问题:
(1)反应Ⅰ的试剂和条件是
(2)反应②的反应类型为
(3)化合物Ⅲ中所含官能团的名称为
(4)下列有关化合物的说法正确的是___________。
| A.化合物Ⅰ可以发生聚合反应 |
| B.化合物Ⅰ存在顺反异构 |
| C.化合物Ⅳ可以使酸性高锰酸钾溶液褪色 |
| D.化合物Ⅳ可以使溴的四氯化碳溶液褪色 |
(6)PMA的结构简式为
您最近一年使用:0次
4 . 如图A的产量可以用来衡量一个国家的石油化工发展水平。回答下列问题:
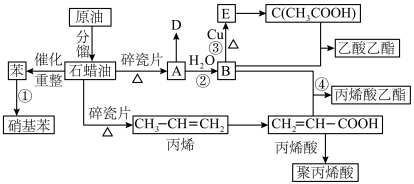
(1)如果用4.6 g B和9.0 g C充分反应制得乙酸乙酯5.28 g,则乙酸乙酯的产率是_______ (产率指的是目标生成物的实际产量与理论产量的比值)。
(2)A的电子式为_______ 。D的分子式为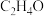 ,且只有一种等效氢,D的结构简式为
,且只有一种等效氢,D的结构简式为_______ 。
(3)丙烯酸→聚丙烯酸的化学方程式:_______ 。
(4)制备乙酸乙酯的化学方程式:_______ 。
(5)有两种气态烃组成的混和气体,对氢气的相对密度为13,取此混和气体4.48 L(标准状况下)通入足量溴水中,溴水增重2.8 g,则此混合气体的组成是_______。
(6)分子式为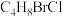 的有机物共有
的有机物共有_______ 种。(不含立体异构)

(1)如果用4.6 g B和9.0 g C充分反应制得乙酸乙酯5.28 g,则乙酸乙酯的产率是
(2)A的电子式为
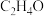 ,且只有一种等效氢,D的结构简式为
,且只有一种等效氢,D的结构简式为(3)丙烯酸→聚丙烯酸的化学方程式:
(4)制备乙酸乙酯的化学方程式:
(5)有两种气态烃组成的混和气体,对氢气的相对密度为13,取此混和气体4.48 L(标准状况下)通入足量溴水中,溴水增重2.8 g,则此混合气体的组成是_______。
A. 与 与 | B. 与 与 |
C. 与 与 | D. 与 与 |
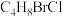 的有机物共有
的有机物共有
您最近一年使用:0次
5 . 已知:A是来自石油的重要有机化工原料,此物质可以用来衡量一个国家石油化工发展水平。E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。
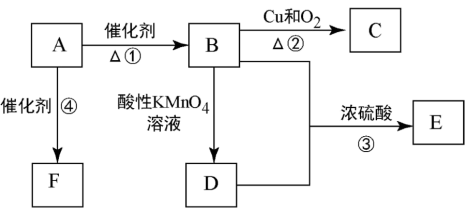
(1)A的结构式为_______ 。C的名称为______ 。
(2)B分子中的官能团名称是______ 。D分子中的官能团名称是______ 。
(3)写出符合下列条件的E的一种同分异构体______ 。
①能与NaHCO3溶液反应产生气体
②其一氯取代物只有2种结构
(4)已知:①CH2=CH2 CH3CH2CN
CH3CH2CN
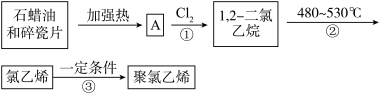
②R-CN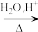 R-COOH(R表示烃基)
R-COOH(R表示烃基)
设计以A为原料制备丙酸乙酯(CH3CH2COOCH2CH3)的合成路线流程图。(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)______ 。

(1)A的结构式为
(2)B分子中的官能团名称是
(3)写出符合下列条件的E的一种同分异构体
①能与NaHCO3溶液反应产生气体
②其一氯取代物只有2种结构
(4)已知:①CH2=CH2
 CH3CH2CN
CH3CH2CN②R-CN
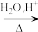 R-COOH(R表示烃基)
R-COOH(R表示烃基)设计以A为原料制备丙酸乙酯(CH3CH2COOCH2CH3)的合成路线流程图。(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)
您最近一年使用:0次
6 . 乙烯是重要的化工原料,以乙烯为原料在不同条件下可合成下列物质(部分条件未标出):
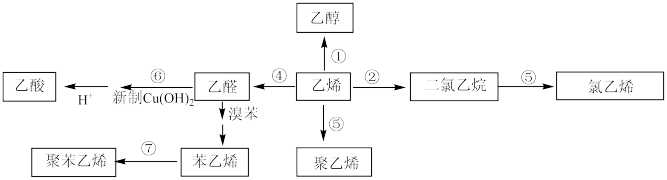
(1)乙醇能与乙酸反应生成有果香味的物质,其名称为_______ 。
(2)写出反应类型:①_______ 、④_______ 。
(3)二氯乙烯中所含官能团的名称_______ 。
(4)反应⑤用NaOH的乙醇溶液处理二氯乙烷制氯乙烯的方程式为:_______ 。
(5)反应⑥的化学方程式_______ ,实验现象是_______ 。
(6)反应⑦的化学方程式_______ 。
(7)以乙醇和苯乙烯为原料合成有机物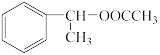 ,写出合成路线图
,写出合成路线图_______ 。
(合成路线常用的表示方式为:A B
B 目标产物)
目标产物)

(1)乙醇能与乙酸反应生成有果香味的物质,其名称为
(2)写出反应类型:①
(3)二氯乙烯中所含官能团的名称
(4)反应⑤用NaOH的乙醇溶液处理二氯乙烷制氯乙烯的方程式为:
(5)反应⑥的化学方程式
(6)反应⑦的化学方程式
(7)以乙醇和苯乙烯为原料合成有机物
 ,写出合成路线图
,写出合成路线图(合成路线常用的表示方式为:A
 B
B 目标产物)
目标产物)
您最近一年使用:0次
解题方法
7 . 室温时,将20mL某气态烃与过量的氧气混合,充分燃烧后冷却至室温,发现混合气体的体积减少60mL,将所得混合气体通过氢氧化钠溶液后,体积又减少80mL。
(1)通过计算确定气态烃分子式_______
(2)已知该烃在一定的温度、压强和催化剂的作用下,可以生成一种高聚物,写出其可能的一种结构_______ 。
(1)通过计算确定气态烃分子式
(2)已知该烃在一定的温度、压强和催化剂的作用下,可以生成一种高聚物,写出其可能的一种结构
您最近一年使用:0次
8 . I.CO2的循环利用是“碳达峰、碳中和”主要措施。
(1)据VSEPR理论可知CO2中心原子价层电子对数为_______
(2)CO2与环氧丙烷 ( )一定条件下反应生成可降解塑料(
)一定条件下反应生成可降解塑料(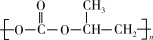 ),写出反应的化学方程式
),写出反应的化学方程式_______
II.工业上用Cu-ZnO作催化剂通过反应①来生产甲醇,同时也会有副反应②发生。
① CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1
②CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
(3)已知298K时,相关物质的能量如图所示,则ΔH1=_______ kJ/mol,(保留三位有效数字),反应①低温_______ 自发进行(填“能”、“不能”)。

(4)在恒温恒容的容器中,充入0.5mol CO2(g)和1.0mol H2(g),起始压强为p kPa,一段时间后达到平衡测得容器中生成0.3mol H2O(g),压强为 p kPa,反应②的平衡常数Kp=
p kPa,反应②的平衡常数Kp=_______ (列出计算式即可)。(分压=物质的量分数×总压,用平衡分压代替平衡浓度计算的平衡常数即为Kp)。
(5)下列说法中不正确的是_______
III.催化加氢合成乙烯是CO2综合利用研究的热点领域,其反应为:2CO2(g)+6H2(g) C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
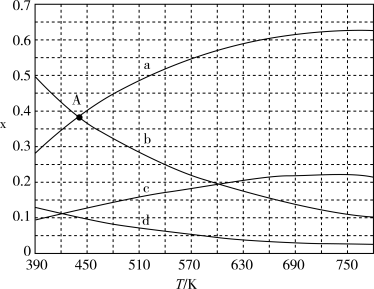
(6)理论计算表明,原料初始组成 ,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是
,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是_______ ,该反应△H _______ 0(填“>”、“<”或“=”)
(1)据VSEPR理论可知CO2中心原子价层电子对数为
(2)CO2与环氧丙烷 (
 )一定条件下反应生成可降解塑料(
)一定条件下反应生成可降解塑料(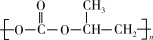 ),写出反应的化学方程式
),写出反应的化学方程式II.工业上用Cu-ZnO作催化剂通过反应①来生产甲醇,同时也会有副反应②发生。
① CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1
CH3OH(g)+H2O(g) ΔH1②CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2(3)已知298K时,相关物质的能量如图所示,则ΔH1=

(4)在恒温恒容的容器中,充入0.5mol CO2(g)和1.0mol H2(g),起始压强为p kPa,一段时间后达到平衡测得容器中生成0.3mol H2O(g),压强为
 p kPa,反应②的平衡常数Kp=
p kPa,反应②的平衡常数Kp=(5)下列说法中不正确的是_______
| A.向容器中充入He,使体系压强增大,可增大反应速率 |
| B.向容器中再充入H2可提高CO2转化率 |
C.当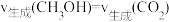 时,说明反应达到了平衡状态 时,说明反应达到了平衡状态 |
| D.选择合适的催化剂,不但可以加快反应速率,还可提高甲醇的平衡产率 |
III.催化加氢合成乙烯是CO2综合利用研究的热点领域,其反应为:2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)(6)理论计算表明,原料初始组成
 ,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是
,在体系压强为0.1MPa条件下反应,反应达到平衡时,四种组分的物质的量分数x与温度T的变化关系如图所示,则图中表示C2H4变化的曲线是
您最近一年使用:0次
9 . 碳原子不仅能与氢、氧、氮、氯等元素原子形成化学键,且碳原子之间还能相互结合,并连接形成直链、支链以及各种环状化合物。
根据下列几种烃的结构式,回答下列问题:
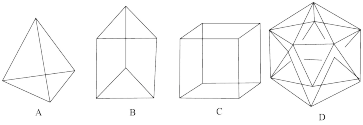
(1)结构D显然是不可能合成的,原因是__________ ;在结构A的每两个碳原子之间插入一个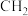 原子团,可以形成金刚烷的结构,则金刚烷的分子式是
原子团,可以形成金刚烷的结构,则金刚烷的分子式是_______________ 。
(2)B的一种同分异构是最简单的芳香烃,能证明该芳香烃中的化学键不是单键和双键交替排列的事实是_________ (填字母)。
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
C的一种同分异构体E是一种重要的化工原料,在一定条件下可以发生如下反应:

已知苯环侧链上的烃基在一定条件下能被氧化成羧基。
(3)下列关于有机化合物E的说法正确的是______ (填字母)。
a.属于芳香烃 b.属于苯的同系物
c.苯环上有烷基 d.侧链中含碳碳双键
(4)有机化合物E的结构简式为____________ 。
(5)请写出E→F反应的化学方程式为__________________ ,反应类型为____________ 。
(6)H具有优良的绝热、绝缘性能,可用作包装材料和建筑材料,在工业上以E为原料生产。请写出相关化学反应方程式________________________ 。
根据下列几种烃的结构式,回答下列问题:

(1)结构D显然是不可能合成的,原因是
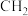 原子团,可以形成金刚烷的结构,则金刚烷的分子式是
原子团,可以形成金刚烷的结构,则金刚烷的分子式是(2)B的一种同分异构是最简单的芳香烃,能证明该芳香烃中的化学键不是单键和双键交替排列的事实是
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
C的一种同分异构体E是一种重要的化工原料,在一定条件下可以发生如下反应:

已知苯环侧链上的烃基在一定条件下能被氧化成羧基。
(3)下列关于有机化合物E的说法正确的是
a.属于芳香烃 b.属于苯的同系物
c.苯环上有烷基 d.侧链中含碳碳双键
(4)有机化合物E的结构简式为
(5)请写出E→F反应的化学方程式为
(6)H具有优良的绝热、绝缘性能,可用作包装材料和建筑材料,在工业上以E为原料生产。请写出相关化学反应方程式
您最近一年使用:0次
10 . 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH2=CH2)与四氯乙烯(CF2=CF2)的共聚物(ETFE)制成。回答下列问题:
(1)F原子最外层轨道表示式为_______ 。
(2)图a、b、c分别表示C、N、O和F的气态原子逐级失去电子所需能量(纵坐标的标度不同)。失去最外层的一个电子所需能量的变化图是_______ (填标号),判断的根据是_______ ,失去三个电子的变化图是_______ (填标号)。

(3)上图四种元素中,原子核外s亚层电子数与p亚层电子数相同的元素在周期表中的位置是_______ ,其形成的氢化物的沸点_______ H2S的沸点(填>、<或=),理由是_______ 。
(4)聚四氯乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
(5)FTFE_______ (填“有”、“没有”)固定熔沸点,其结构简式为:_______ 。
(1)F原子最外层轨道表示式为
(2)图a、b、c分别表示C、N、O和F的气态原子逐级失去电子所需能量(纵坐标的标度不同)。失去最外层的一个电子所需能量的变化图是

(3)上图四种元素中,原子核外s亚层电子数与p亚层电子数相同的元素在周期表中的位置是
(4)聚四氯乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因
(5)FTFE
您最近一年使用:0次



