名校
1 . 航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图___________ 。
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是___________ 。
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为___________ 。
(1)写出高氯酸铵组成元素中,原子核外有三层电子的原子的结构示意图
(2)高氯酸铵对应酸高氯酸HClO4的酸酐是
(3)150℃时高氯酸铵发生分解反应:2NH4ClO4=N2↑+Cl2↑+2O2↑+4H2O↑,其气态生成物组成的混合气的平均相对分子质量为
您最近一年使用:0次
2 . 元素周期表是学习和研究化学的重要工具,下面是元素周期表的部分内容,请根据下表回答问题:
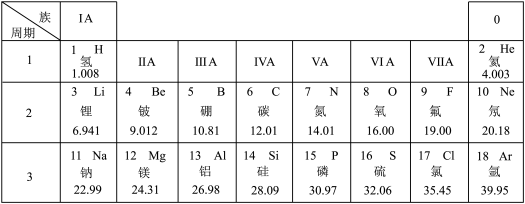
(1)发现了元素周期律并编制出元素周期表的化学家是___________(填字母)。
(2)氟元素是人体必需微量元素之一,能防治龋齿。氟元素的相对原子质量为___________ 。
(3)已知某微粒的结构示意图为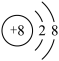 ,请写出该微粒的符号
,请写出该微粒的符号___________ 。
(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式为___________ 。

(1)发现了元素周期律并编制出元素周期表的化学家是___________(填字母)。
| A.门捷列夫 | B.拉瓦锡 | C.道尔顿 | D.阿伏加德罗 |
(3)已知某微粒的结构示意图为
 ,请写出该微粒的符号
,请写出该微粒的符号(4)地壳中含量最多的金属元素和最多的非金属元素组成的化合物的化学式为
您最近一年使用:0次
名校
3 . 近年来,我国航空航天事业成果显著,“北斗三号”导航卫星搭载了精密计时的铷( )原子钟。如图为铷元素在元素周期表中的信息和铷的原子结构示意图(如图)。回答下列问题:
)原子钟。如图为铷元素在元素周期表中的信息和铷的原子结构示意图(如图)。回答下列问题:
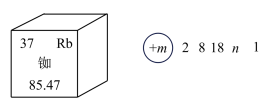
(1)下列说法错误的是_____(填字母)。
(2) 原子第一电子层上电子的能量比最外层上电子的能量
原子第一电子层上电子的能量比最外层上电子的能量_____ (填“低”或“高”)。
(3)如图2中A-E所示粒子共表示种元素;铷元素原子的化学性质与如图中_____ (填字母)的化学性质相似;属于阴离子结构示意图的是_____ (填字母);写出B与D形成化合物的化学式_____ 。
(4)在核电荷数1~10的元素内,列举两个与图2中E电子层结构相同的离子,写出离子的符号_____ 。
A.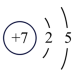 B.
B.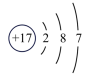 C.
C.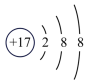 D.
D.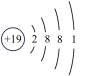 E.
E.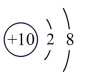
 )原子钟。如图为铷元素在元素周期表中的信息和铷的原子结构示意图(如图)。回答下列问题:
)原子钟。如图为铷元素在元素周期表中的信息和铷的原子结构示意图(如图)。回答下列问题:
(1)下列说法错误的是_____(填字母)。
A.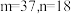 |
| B.铷是金属元素 |
| C.铷的相对原子质量是85.47 |
| D.铷原子有5个电子层,最外层有1个电子 |
(2)
 原子第一电子层上电子的能量比最外层上电子的能量
原子第一电子层上电子的能量比最外层上电子的能量(3)如图2中A-E所示粒子共表示种元素;铷元素原子的化学性质与如图中
(4)在核电荷数1~10的元素内,列举两个与图2中E电子层结构相同的离子,写出离子的符号
A.
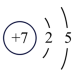 B.
B. C.
C. D.
D. E.
E.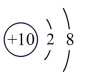
您最近一年使用:0次
名校
解题方法
4 . 下表列出了A~R9种元素在周期表中的位置。请回答下列问题。
(1)在这9种元素中,最外层电子数为1的元素为_____ (填元素符号),化学性质最不活泼的是_____ (填元素符号)。
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应水化物反应的离子方程式是_____ 。
(3)F、A、D三种元素的离子半径由大到小的顺序排列为_____ (填离子符号)。
(4)用电子式表示由C和H组成的化合物的形成过程:_____ 。
(5)由E和F形成的氧化物通入足量的B的氢氧化物中,其离子反应方程式为_____ 。
(6)由E和G所形成的化合物中所含有的化学键为_____ 。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
(2)D元素的最高价氧化物对应的水化物与A元素的最高价氧化物对应水化物反应的离子方程式是
(3)F、A、D三种元素的离子半径由大到小的顺序排列为
(4)用电子式表示由C和H组成的化合物的形成过程:
(5)由E和F形成的氧化物通入足量的B的氢氧化物中,其离子反应方程式为
(6)由E和G所形成的化合物中所含有的化学键为
您最近一年使用:0次
2023-12-24更新
|
440次组卷
|
2卷引用:湖南省长郡中学2023-2024学年高一上学期选科适应性调研检测化学试题
解题方法
5 . 如表为元素周期表中的一部分,请回答下列问题:
(1)写出⑤元素的名称_______ 。
(2)写出③元素的离子结构示意图_______ 。
(3)④单质与水发生反应的离子方程式_______ 。
(4)写出⑥元素在周期表中的位置_______ 。
(5)比较单质氧化性的强弱⑤_______ ⑦(填”>”、”<”或”=”)。
| 项目 | I A | II A | III A | IV A | V A | VI A | VII A |
| 二 | ① | ② | ③ | ||||
| 三 | ④ | ⑤ | |||||
| 四 | ⑥ | ⑦ |
(1)写出⑤元素的名称
(2)写出③元素的离子结构示意图
(3)④单质与水发生反应的离子方程式
(4)写出⑥元素在周期表中的位置
(5)比较单质氧化性的强弱⑤
您最近一年使用:0次
6 . 人体必需的一些元素在周期表中的分布情况如下:

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是___________ 。H2O2是一种绿色氧化剂,电子式为___________ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为___________ 。
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是___________ ,原子序数为___________ 。
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为___________ 。
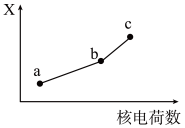
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

| A.若a、b、c表示氧族元素,则X表示对应氢化物的稳定性 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第IA族元素,则X表示对应离子的氧化性 |
| D.若a、b、c表示第IIA族元素,则X表示最高价氧化物对应水化物的碱性 |
您最近一年使用:0次
2023-12-05更新
|
264次组卷
|
3卷引用:河北省石家庄市辛集市2023-2024学年高一上学期2月期末考试化学试题
名校
解题方法
7 . 金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)基态Na原子的原子结构示意图表示式为___________ ,在周期表中的位置是___________ 。
(2)Na2O2的电子式为___________ 。Na2O2可作供氧剂,写出Na2O2与CO2反应的化学方程式___________ 。若有1molNa2O2参加反应则转移电子的物质的量为___________ mol。
(3)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过___________ 、___________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应: ___________MnO +___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式
+___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式_________ ;该反应说明Na2O2具有___________ 性(选填“氧化”,“还原”或“漂白”)。
(5)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1molNa2CO3·NaHCO3·2H2O经充分加热得到Na2CO3的质量为___________ g。
(1)基态Na原子的原子结构示意图表示式为
(2)Na2O2的电子式为
(3)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应: ___________MnO
 +___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式
+___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式(5)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1molNa2CO3·NaHCO3·2H2O经充分加热得到Na2CO3的质量为
您最近一年使用:0次
2023-12-02更新
|
199次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高一上学期12月考试化学试卷
8 . 按要求填空。
(1)已知A原子,其核外电子数为17,则A是_______ (填元素符号)。
(2)已知B原子,L层上的电子数为K层的3倍,则其原子结构示意图是_______ 。
(3)已知C原子,其最外层电子数等于次外层电子数的2倍,则C的元素名称是_______ 。
(4)某元素D的原子得到2个电子后,电子层排布与氖原子相同的,写出该元素的离子结构示意图_______ 。
(1)已知A原子,其核外电子数为17,则A是
(2)已知B原子,L层上的电子数为K层的3倍,则其原子结构示意图是
(3)已知C原子,其最外层电子数等于次外层电子数的2倍,则C的元素名称是
(4)某元素D的原子得到2个电子后,电子层排布与氖原子相同的,写出该元素的离子结构示意图
您最近一年使用:0次
名校
解题方法
9 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)②的最高价氧化物的分子式为_______ ;⑦的最高价氧化物对应水化物的分子式为_______ 。
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:_______ 。
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_______(填字母)。
(4)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为_______ 。
②铯单质与 反应的化学反应方程式为
反应的化学反应方程式为_______ 。
③预测铯单质的还原性比钠单质的还原性_______ (填“弱”或“强”)。
④下列推断正确的是_______ (填字母)。
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_______(填字母)。
| A.在化合物中最高正化合价为+6 | B.单质可以与 气体反应并置换出单质S 气体反应并置换出单质S |
| C.最高价氧化物对应水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |
①铯的原子序数为
②铯单质与
 反应的化学反应方程式为
反应的化学反应方程式为③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
2023-11-10更新
|
895次组卷
|
2卷引用:广西柳州铁一中学2022-2023学年高一上学期期末考试化学试题
名校
10 . 如图是氟元素在元素周期表中的信息及原子结构示意图,回答下列问题:
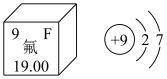
(1)图中“19.00”代表___________ ,请写出氟原子最外层的轨道表示式:___________ 。其最外层有___________ 种运动状态不同的电子,能量最高的能级的原子轨道的形状___________ 。
(2)氟气非常活泼,易与金属和某些非金属反应生成不同的化合物,如 、
、 ,请写出
,请写出 的电子式
的电子式___________ , 中的化学键类型为
中的化学键类型为___________ ; 是
是___________ 化合物, 是10电子微粒,请再写出两个10电子微粒
是10电子微粒,请再写出两个10电子微粒___________ 。

(1)图中“19.00”代表
(2)氟气非常活泼,易与金属和某些非金属反应生成不同的化合物,如
 、
、 ,请写出
,请写出 的电子式
的电子式 中的化学键类型为
中的化学键类型为 是
是 是10电子微粒,请再写出两个10电子微粒
是10电子微粒,请再写出两个10电子微粒
您最近一年使用:0次



