名校
1 . 元素周期表中氢元素的相关信息如图所示,其中“1.008”的含义是指________ ;此外你还能从图中获取氢元素的哪些信息,请简要阐述,_______ 。(任写一个)


您最近一年使用:0次
名校
2 . 下图是某牙膏成分表的一部分,回答下列问题:
(1)牙膏属于___________ (填“混合物”或“纯净物”)。
(2)含氟牙膏能预防龋齿,这里的“氟”指的是___________ (填“分子”“原子”或“元素”)。
(3)二氧化硅(SiO2)中硅元素的化合价为___________ 。
(4)人被有些蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使人产生痛痒感。在叮咬处涂抹牙膏就可减轻痛痒,说明该牙膏呈___________ (填“酸性”“碱性”或“中性”)。
| XX牙膏 成分:二氧化硅、水、 纤维素胶、碳酸钠、 香精、单氟磷酸钠、 碳酸氢钠… |
(2)含氟牙膏能预防龋齿,这里的“氟”指的是
(3)二氧化硅(SiO2)中硅元素的化合价为
(4)人被有些蚊虫叮咬后,蚊虫在人的皮肤内分泌出蚁酸,使人产生痛痒感。在叮咬处涂抹牙膏就可减轻痛痒,说明该牙膏呈
您最近一年使用:0次
名校
3 . 回答下列问题
Ⅰ.有下列物质:① 固体;②熔融的
固体;②熔融的 ;③NH4HCO3晶体;④稀硫酸;⑤
;③NH4HCO3晶体;④稀硫酸;⑤ 胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸
胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸
(1)上述状态下的物质可导电的是______ (填序号,下同),属于电解质的是_______ 。
(2)a个⑥原子的总质量为b g,则⑥的摩尔质量表示为_______ ,13.6g的②中阴阳离子总数为_______ 。
(3)在小烧杯中加入 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,
溶液,_______ ,即制得物质⑤ 胶体。
胶体。
(4)写出向①的水溶液中加入等物质的量的③的离子方程式:_______ 。
(5)向①溶液中通入少量⑨可产生白色沉淀,继续通入⑨可观察到白色沉淀消失,白色沉淀消失的原因为:_______ (离子方程式表示)
Ⅱ.元素周期表对学生学习化学有着重要的作用。其中过渡元素位于周期表中部,请补充以下元素的符号:
(6)原子序数21-25:_______ 、Ti、_______ 、Cr、Mn
元素周期表中同一纵列元素具有相似的化学性质,请补充以下元素的符号:
(7)第IVA族:C、Si、_______ 、_______ 、_______ 、Fl
Ⅰ.有下列物质:①
 固体;②熔融的
固体;②熔融的 ;③NH4HCO3晶体;④稀硫酸;⑤
;③NH4HCO3晶体;④稀硫酸;⑤ 胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸
胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸(1)上述状态下的物质可导电的是
(2)a个⑥原子的总质量为b g,则⑥的摩尔质量表示为
(3)在小烧杯中加入
 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,
溶液, 胶体。
胶体。(4)写出向①的水溶液中加入等物质的量的③的离子方程式:
(5)向①溶液中通入少量⑨可产生白色沉淀,继续通入⑨可观察到白色沉淀消失,白色沉淀消失的原因为:
Ⅱ.元素周期表对学生学习化学有着重要的作用。其中过渡元素位于周期表中部,请补充以下元素的符号:
(6)原子序数21-25:
元素周期表中同一纵列元素具有相似的化学性质,请补充以下元素的符号:
(7)第IVA族:C、Si、
您最近一年使用:0次
4 . 如表是元素周期表的一部分,表中的每个编号代表一种短周期主族元素,请回答下列问题:
(1)元素②的原子结构示意图是______ 。
(2)比较元素原子半径大小:③______ ④(填“>”或“<”)。
(3)元素③位于元素周期表中第______ 周期VA族。
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式______ 。
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为______ 。
| 族 周期 | IA | 0 | ||||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |||
| 2 | ② | ③ | ④ | |||||||
| 3 | ⑤ | ⑥ | ||||||||
(2)比较元素原子半径大小:③
(3)元素③位于元素周期表中第
(4)元素①的单质在元素⑥的单质中燃烧产物的化学式
(5)元素⑤和元素⑥可组成原子个数比为1:1的化合物的化学式为
您最近一年使用:0次
解题方法
5 . NaOH被大量用于制皂、造纸和纺织品生产。回答下列问题。
(1)H元素位于元素周期表的第________ 周期第IA族。
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的______ (填“大”或“小”)。
(3)NaOH所含的两种非金属元素中,非金属性较强的是_______ (填“H”或“O”)。
(1)H元素位于元素周期表的第
(2)Na元素位于第IA族H元素下方,Na的原子半径比H的
(3)NaOH所含的两种非金属元素中,非金属性较强的是
您最近一年使用:0次
名校
解题方法
6 . 中国高铁对实现“一带一路”的战略构想有重要的作用。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是___________ 。
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是___________ ;乘务员使用的无线通话机的芯片材料所含元素在元素周期中的位置___________ 。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式___________ 。
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式___________ 。
(5)硅酸盐材料具有硬度高、难溶于水、耐高温等特点。硅酸盐中常含有Al、K等元素,如钾长石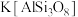 和钠长石
和钠长石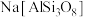 等,
等,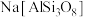 用氧化物形式表示为
用氧化物形式表示为___________ 。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是
(2)高铁上的信息传输系统使用了光导纤维,其主要成分是
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式
(4)高铁上的卫生间没有任何异味,是由于所使用的马桶、地漏和洗手盆下水口都是纳米硅胶的高科技产品,向硅酸钠溶液中加入稀盐酸可产生硅酸胶体,该反应的离子方程式
(5)硅酸盐材料具有硬度高、难溶于水、耐高温等特点。硅酸盐中常含有Al、K等元素,如钾长石
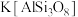 和钠长石
和钠长石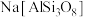 等,
等,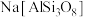 用氧化物形式表示为
用氧化物形式表示为
您最近一年使用:0次
名校
7 . 元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。如表是元素周期表的一部分,请回答下列问题:
(1)元素②、③、⑥的简单离子半径由大到小的排序为___________ (填离子符号)。
(2)②和④组成的物质中含有___________ 键,可以证明该化合物含有此类型化学键的实验事实为___________ 。
(3)⑤的氧化物和⑥的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(4)已知④的单质与①的最高价氧化物A在点燃条件下能反应生成黑色单质,推测③的单质___________ (填“能”或“不能”)与A反应,说明推测的理由___________ 。
| 周期 | IA | 0 | |||||||
| 1 | IIA | … | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | |||||
(2)②和④组成的物质中含有
(3)⑤的氧化物和⑥的最高价氧化物对应的水化物反应的离子方程式为
(4)已知④的单质与①的最高价氧化物A在点燃条件下能反应生成黑色单质,推测③的单质
您最近一年使用:0次
名校
8 . 生活中处处有化学。请回答下列问题:
(1)苏打水是很多人喜爱的饮品,请写出小苏打在水中的电离方程式_______ 。
(2)“84消毒液”与洁厕灵(主要成分是浓盐酸)不能混用,混合会产生黄绿色的有毒气体,请用离子方程式解释原因_______ 。
(3)Na2O2常用作呼吸面罩供氧剂,请写出Na2O2的电子式_______ 。
(4)硅是太阳能电池板的主要原材料,请写出硅元素在周期表的位置_______ 。
(5)4gCO在氧气中燃烧生成CO2,放出9.6kJ热量,写出CO燃烧的热化学方程式_______ 。
(6)已知:①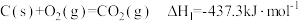
②H2(g)+1/2O2(g)=H2O(g) ∆H2=-285.8kJ·mol-1
③CO(g)+1/2O2(g)=CO2(g) ∆H3=-283.0kJ·mol-1
写出煤气化(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式_______ 。
(1)苏打水是很多人喜爱的饮品,请写出小苏打在水中的电离方程式
(2)“84消毒液”与洁厕灵(主要成分是浓盐酸)不能混用,混合会产生黄绿色的有毒气体,请用离子方程式解释原因
(3)Na2O2常用作呼吸面罩供氧剂,请写出Na2O2的电子式
(4)硅是太阳能电池板的主要原材料,请写出硅元素在周期表的位置
(5)4gCO在氧气中燃烧生成CO2,放出9.6kJ热量,写出CO燃烧的热化学方程式
(6)已知:①
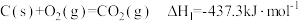
②H2(g)+1/2O2(g)=H2O(g) ∆H2=-285.8kJ·mol-1
③CO(g)+1/2O2(g)=CO2(g) ∆H3=-283.0kJ·mol-1
写出煤气化(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式
您最近一年使用:0次
9 . 联合国将2019年定为“国际化学元素周期表年”,新版周期表包含118种元素,下表代表元素周期表前四周期,回答下列问题:

(1)表中的实线是元素周期表的部分边界,请在图中用实线画出金属元素与非金属元素的分界线,将硼、磷的元素符号填写在上述周期表相应的空格中_____ 。
(2)某元素的原子次外层电子数比最外层电子数多1个,单质常温下为黄绿色气体,该元素的最高价氧化物对应水化物的电离方程式为_____ 。
(3)下列有关性质的比较正确,且能用元素周期律解释的是___________ 。
a.非金属性:O>S b.热稳定性:HF<HCl
c.酸性:HCl>H2SO3 d.碱性:NaOH>Mg(OH)2
(4)某金属单质既可以和强酸反应也可以和强碱溶液反应,写出对应的离子方程式___________ ;___________ 。
(5)硒(Se)是人体必需的微量元素,其原子结构示意图为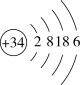 。
。
①Se在元素周期表中的位置是___________ 。
②Se的简单气态氢化物的化学式为___________ 。
③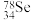 和
和 互称为
互称为___________ 。

(1)表中的实线是元素周期表的部分边界,请在图中用实线画出金属元素与非金属元素的分界线,将硼、磷的元素符号填写在上述周期表相应的空格中
(2)某元素的原子次外层电子数比最外层电子数多1个,单质常温下为黄绿色气体,该元素的最高价氧化物对应水化物的电离方程式为
(3)下列有关性质的比较正确,且能用元素周期律解释的是
a.非金属性:O>S b.热稳定性:HF<HCl
c.酸性:HCl>H2SO3 d.碱性:NaOH>Mg(OH)2
(4)某金属单质既可以和强酸反应也可以和强碱溶液反应,写出对应的离子方程式
(5)硒(Se)是人体必需的微量元素,其原子结构示意图为
 。
。①Se在元素周期表中的位置是
②Se的简单气态氢化物的化学式为
③
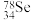 和
和 互称为
互称为
您最近一年使用:0次
解题方法
10 . 表中是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)写出元素符号和名称。
①_____ ,②_____ ,⑧_____ ,⑨_____ 。
(2)写出下列反应的化学方程式。
⑦的单质跟④的氢氧化物溶液反应:_____ 。
⑤的氧化物跟⑥的最高价氧化物的水化物反应:_____ 。
⑥的单质在③的单质中燃烧:_____ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
①
(2)写出下列反应的化学方程式。
⑦的单质跟④的氢氧化物溶液反应:
⑤的氧化物跟⑥的最高价氧化物的水化物反应:
⑥的单质在③的单质中燃烧:
您最近一年使用:0次



