2021高一·全国·专题练习
1 . 请在表中画出元素周期表的轮廓,并在表中按要求完成下列问题:
①标出族序数;②填入1~20元素的元素符号;③)填入稀有气体元素的原子序数以及每周期的元素种类;④画出主族与副族边界线。
_______

①标出族序数;②填入1~20元素的元素符号;③)填入稀有气体元素的原子序数以及每周期的元素种类;④画出主族与副族边界线。

您最近一年使用:0次
2021高一·全国·专题练习
解题方法
2 . 元素在周期表中的位置反映了元素的原子结构和元素的性质,下图是元素周期表的一部分:
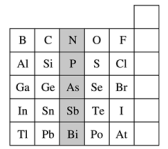
(1)根据元素周期律,请你预测,H3AsO4、H3PO4的酸性强弱:H3AsO4___________ (填“>”“<”或“=”)H3PO4。
(2)根据NaH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第___________ 族。
(3)周期表中有10多种人体所需的微量元素,其中有一种被誉为“生命元素”的主族元素R,对延长人类寿命起着重要作用。已知R元素的原子有4个电子层,其最高价氧化物的分子式为RO3,则R元素的名称为___________ 。

(1)根据元素周期律,请你预测,H3AsO4、H3PO4的酸性强弱:H3AsO4
(2)根据NaH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第
(3)周期表中有10多种人体所需的微量元素,其中有一种被誉为“生命元素”的主族元素R,对延长人类寿命起着重要作用。已知R元素的原子有4个电子层,其最高价氧化物的分子式为RO3,则R元素的名称为
您最近一年使用:0次
21-22高二·全国·单元测试
3 . 下图所示为元素周期表的大致框架:
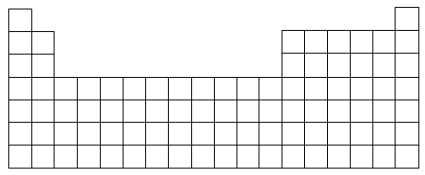
(1)在上图所示元素周期表中画出金属元素与非金属元素的分界线_______ 。
(2)鉴于NaH的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的_______ 族。
(3)现有甲、乙两种元素,甲元素原子核外3p能级上有5个电子,乙元素的焰色实验呈黄色。
①在上图所示的元素周期表中,将甲、乙两元素的元素符号填在元素周期表中的相应位置_______ 。
②甲元素与硫元素相比,非金属性较强的是_______ (填元素名称),写出可以验证该结论的一个化学方程式:_______ 。
(4)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如下图所示。下列叙述不正确的是_______ (填字母)。

A.铊元素在元素周期表中的位置是第六周期第ⅡA族
B.铊原子的中子数为204-81=123
C.6s26p1表示铊原子有6个电子层,最外电子层上有3个电子
D.铊元素的金属性比铝元素的强
E.铊元素是p区元素

(1)在上图所示元素周期表中画出金属元素与非金属元素的分界线
(2)鉴于NaH的存在,有人建议可把氢元素归到第ⅦA族。根据氢元素最高正化合价与最低负化合价的绝对值相等,也可把氢元素归到元素周期表中的
(3)现有甲、乙两种元素,甲元素原子核外3p能级上有5个电子,乙元素的焰色实验呈黄色。
①在上图所示的元素周期表中,将甲、乙两元素的元素符号填在元素周期表中的相应位置
②甲元素与硫元素相比,非金属性较强的是
(4)近年来“铊中毒”事件屡屡发生,铊再次成为公众关注的焦点。铊元素的相关信息如下图所示。下列叙述不正确的是

A.铊元素在元素周期表中的位置是第六周期第ⅡA族
B.铊原子的中子数为204-81=123
C.6s26p1表示铊原子有6个电子层,最外电子层上有3个电子
D.铊元素的金属性比铝元素的强
E.铊元素是p区元素
您最近一年使用:0次
21-22高二·全国·课时练习
4 . 原子结构与元素周期表存在内在联系,按要求回答下列问题:
(1)根据元素在周期表中的位置,写出元素基态原子的价电子排布式。
①第四周期第ⅥB族_______ ;
②第五周期第ⅠB族_______ ;
③第五周期第ⅣA族_______ ;
④第六周期第ⅡA族_______ 。
(2)根据元素电子排布可以确定元素在周期表中的位置。
①具有(n-1)d10ns2电子排布的元素位于周期表中的第_______ 族。
②已知某元素+2价离子的核外电子排布式为1s22s22p63s23p63d3。该元素位于元素周期表_______ (填序号)。
A.第二周期第ⅡB族
B.第四周期第ⅡA族
C.第四周期第ⅤB族
D.第五周期第ⅡB族
③某元素原子的核电荷数为33,则其原子的价电子排布式为_______ ,其位于元素周期表中的_______ ,属于_______ 区的元素。
(3)根据元素核外电子排布可以推知元素的性质。
①被誉为“21世纪金属”的钛(Ti)元素,基态原子价电子轨道表示式为_______ ,Ti元素形成的化合物中,Ti呈现的最高价态为_______ 价。
②日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素基态原子的价电子排布式为3d54s1,该元素的名称是_______ 。
(1)根据元素在周期表中的位置,写出元素基态原子的价电子排布式。
①第四周期第ⅥB族
②第五周期第ⅠB族
③第五周期第ⅣA族
④第六周期第ⅡA族
(2)根据元素电子排布可以确定元素在周期表中的位置。
①具有(n-1)d10ns2电子排布的元素位于周期表中的第
②已知某元素+2价离子的核外电子排布式为1s22s22p63s23p63d3。该元素位于元素周期表
A.第二周期第ⅡB族
B.第四周期第ⅡA族
C.第四周期第ⅤB族
D.第五周期第ⅡB族
③某元素原子的核电荷数为33,则其原子的价电子排布式为
(3)根据元素核外电子排布可以推知元素的性质。
①被誉为“21世纪金属”的钛(Ti)元素,基态原子价电子轨道表示式为
②日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素基态原子的价电子排布式为3d54s1,该元素的名称是
您最近一年使用:0次
5 . 氨硼烷(NH3BH3)含氢量高、热稳定性适中、释氢条件相对温和,是目前最具有潜力的固体储氢材料之一 。
(1)N在元素周期表中的位置是第___________ 周期、第VA族。
(2)写出N的最高价氧化物对应的水化物的化学式:___________ 。
(3)N的非金属性强于B的,用原子结构解释原因: N和B在同一周期,原子核外电子层数相同,___________ ,原子半径N小于B,得电子能力N强于B。
(4)在元素周期表中,砷(As)位于第4周期,与N同主族。下列关于 As的推断中,正确的是___________ (填字母)。
a.原子的最外层电子数为5
b.元素的非金属性: As>N
c.原子半径: As>N
(1)N在元素周期表中的位置是第
(2)写出N的最高价氧化物对应的水化物的化学式:
(3)N的非金属性强于B的,用原子结构解释原因: N和B在同一周期,原子核外电子层数相同,
(4)在元素周期表中,砷(As)位于第4周期,与N同主族。下列关于 As的推断中,正确的是
a.原子的最外层电子数为5
b.元素的非金属性: As>N
c.原子半径: As>N
您最近一年使用:0次
2021-12-25更新
|
328次组卷
|
2卷引用:2021年北京第二次普通高中学业水平合格性考试化学试题
名校
6 . 黑火药爆炸时发生化学反应:S+2KNO3 +3C→ K2S +3CO2↑ +N2↑
(1)上述反应涉及的元素中,属于第二周期的元素有_______ 。
(2)上述反应的生成物中,属于非电解质的是_______ ,其电子式是_______ 。
(3)写出K、N最高价氧化物对应的水化物之间发生反应的化学方程式:_______ 。
(1)上述反应涉及的元素中,属于第二周期的元素有
(2)上述反应的生成物中,属于非电解质的是
(3)写出K、N最高价氧化物对应的水化物之间发生反应的化学方程式:
您最近一年使用:0次
名校
7 . 完成下列填空
(1)元素周期表中有___________ 个周期,___________ 个主族。
(2)某短周期元素原子的核电荷数是其电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图是___________ 。
(3)已知某粒子的结构示意图如图所示。试回答:

①当x-y=10时,该粒子为___________ (填“原子”“阳离子”或“阴离子”)。
②写出y=3与y=7的元素的最高价氧化物对应的水化物发生反应的离子方程式:___________ 。
(1)元素周期表中有
(2)某短周期元素原子的核电荷数是其电子层数的5倍,其质子数是最外层电子数的3倍,该元素的原子结构示意图是
(3)已知某粒子的结构示意图如图所示。试回答:

①当x-y=10时,该粒子为
②写出y=3与y=7的元素的最高价氧化物对应的水化物发生反应的离子方程式:
您最近一年使用:0次
21-22高一上·全国·课前预习
解题方法
8 . 门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下了空位。例如:他认为铝的下方有一个与铝类似的元素“类铝”,并预测了它的性质。1875年,法国化学家布瓦博德朗发现了这种元素,将它命名为“镓”,镓的性质与门捷列夫预测的一样。门捷列夫还预测在硅和锡之间存在一种元素“类硅”,15年后该元素被德国化学家文克勒发现,为了纪念他的祖国,将其命名为“锗”。
2016年国际纯粹与应用化学联合会(IUPAC)正式宣布,元素周期表中将加入4种新元素,原子序数分别为113、115、117和118.这可是件大事,因为这四种元素都是在实验室合成的,放射性强,还特别重。也因此而补齐了元素周期表的第七行。他们的发现也为科学家在未来合成更重要、更有实用价值的元素提供了可能。
问题:元素周期表给科学工作者发现元素提供了哪些依据_____ ?元素周期表中元素的位置和性质之间存在着怎样的内在联系_____ ?
2016年国际纯粹与应用化学联合会(IUPAC)正式宣布,元素周期表中将加入4种新元素,原子序数分别为113、115、117和118.这可是件大事,因为这四种元素都是在实验室合成的,放射性强,还特别重。也因此而补齐了元素周期表的第七行。他们的发现也为科学家在未来合成更重要、更有实用价值的元素提供了可能。
问题:元素周期表给科学工作者发现元素提供了哪些依据
您最近一年使用:0次
名校
9 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
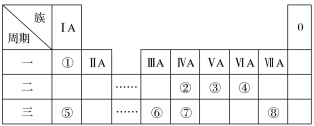
(1)②的元素符号是___________ ;⑦的一种中子数为14的原子符号为___________ 。
(2)①③④三种元素可形成含10个电子的分子分别是___________ 、___________ 。(填化学式)
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为___________ ,该元素在周期表中的位置是___________ 。
(4)⑤的单质与D2O反应的离子方程式为___________ 。
(5)⑥的单质与氢氧化钠溶液反应的离子方程式为___________ 。
(6)实验室制备⑧单质的化学方程式为___________ 。

(1)②的元素符号是
(2)①③④三种元素可形成含10个电子的分子分别是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)⑤的单质与D2O反应的离子方程式为
(5)⑥的单质与氢氧化钠溶液反应的离子方程式为
(6)实验室制备⑧单质的化学方程式为
您最近一年使用:0次
21-22高一上·全国·课前预习
10 . 随着化学科学的不断发展,元素周期表中为未知元素留下的空位先后被填满,周期表的形式也变得更加完美。请认真观察教材最后面的元素周期表,并结合初中所学的有关知识,回答下列问题。
(1)问题一:元素周期表中共有_____ 种底色?分别代表_____ ?分布有什么特点_____ ?周期表中有些元素用红框圈了起来,这些元素是哪类元素_____ ?
(2)问题二:元素周期表中共有_____ 行?_____ 列?周期表中一个横行叫做_____ ?每一行各有_____ 种元素?周期表中一个纵列叫做_____ ?用什么符号表示的_____ ?
(1)问题一:元素周期表中共有
(2)问题二:元素周期表中共有
您最近一年使用:0次



