名校
1 . 下表为元素周期表的一部分,①~⑧分别代表8种不同的元素。
用化学用语 回答下列问题:
(1)②在元素周期表中的位置是___________ 。
(2)③、④、⑤、⑥的离子半径由大到小的顺序是___________ 。
(3)①~⑧的最高价氧化物对应水化物,酸性最强的是___________ 。
(4)①、④、⑤可组成既含离子键,又含共价键的化合物,其电子式为___________ 。
(5)含元素①的某种复盐晶体可以用作净水剂。其化学式是___________ ,用离子方程式表示它能净水的原因___________ 。
| ① | |||||||||
| ② | ③ | ④ | |||||||
| ⑤ | ⑥ | ⑦ | ⑧ |
用
(1)②在元素周期表中的位置是
(2)③、④、⑤、⑥的离子半径由大到小的顺序是
(3)①~⑧的最高价氧化物对应水化物,酸性最强的是
(4)①、④、⑤可组成既含离子键,又含共价键的化合物,其电子式为
(5)含元素①的某种复盐晶体可以用作净水剂。其化学式是
您最近一年使用:0次
2021-11-08更新
|
125次组卷
|
2卷引用:上海市向明中学2021-2022学年高二上学期期中考试化学试题
名校
2 . 下表是元素周期表的一部分。
(1)表中元素③的氢化物的电子式为___________ ;此氢化物的稳定性比元素④的氢化物的稳定性___________ (选填“强”或“弱”);此氢化物与元素⑧的氢化物反应生成的化合物其水溶液呈酸性,用离子方程式表示其原因是___________ 。
(2)③④⑤⑥元素中,原子半径最大的元素是___________ (填元素符号);这四种元素形成的简单离子中离子半径最小的是___________ (填离子符号)。
(3)⑤、⑥两元素相比较,金属性较强是___________ (填元素符号),可以证明该结论的实验是___________ 。
a.比较这两种元素最高价氧化物对应的水化物的碱性
b.比较这两种元素的气态氢化物的稳定性
c.将这两种元素的单质分别放入冷水中
d.比较这两种元素的单质与酸反应时失电子的数目
(4)请用一个化学方程式证明元素⑦和⑧的非金属性强弱关系___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 二 | ① | ② | ③ | ④ | |||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)③④⑤⑥元素中,原子半径最大的元素是
(3)⑤、⑥两元素相比较,金属性较强是
a.比较这两种元素最高价氧化物对应的水化物的碱性
b.比较这两种元素的气态氢化物的稳定性
c.将这两种元素的单质分别放入冷水中
d.比较这两种元素的单质与酸反应时失电子的数目
(4)请用一个化学方程式证明元素⑦和⑧的非金属性强弱关系
您最近一年使用:0次
2021-11-08更新
|
350次组卷
|
2卷引用:上海市南洋模范中学2021-2022学年高二上学期期中考试化学(等级考)试题
解题方法
3 . 我国的食品添加剂有多种,如富硒(Se)酵母、二氧化硅、硫黄等,新品种食品添加剂的安全性需通过审查和测试,食品添加剂包括食品营养强化剂、风味改良剂、结构改善剂、防腐剂等,用于食品生产中能更好地满足吃货们的心愿,丰富舌尖上的营养和美味。请回答下列问题:
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为___________ ;普通玻璃的主要成分为二氧化硅,用氢氟酸蚀刻普通玻璃时,发生反应的化学方程式为___________ 。
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如图所示(已知:a为非金属元素)。
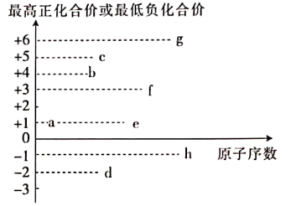
①由a、c、d三种元素形成的离子化合物的化学式为___________ 。
②图中所示元素中金属性最强的是___________ (填元素符号),工业上得到该元素的单质的原理为___________ (填化学方程式)。
③e、f、g元素的简单离子半径由大到小的顺序为___________ (用离子符号回答)。
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为___________ (填化学式)。
⑤a2d2可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,发生反应的离子方程式为___________ 。
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如图所示(已知:a为非金属元素)。

①由a、c、d三种元素形成的离子化合物的化学式为
②图中所示元素中金属性最强的是
③e、f、g元素的简单离子半径由大到小的顺序为
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为
⑤a2d2可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,发生反应的离子方程式为
您最近一年使用:0次
2021-11-05更新
|
417次组卷
|
3卷引用:安徽省部分学校2021-2022学年高三上学期10月联考化学试题
安徽省部分学校2021-2022学年高三上学期10月联考化学试题河北省石家庄市保定市2022届高三10月月考化学试题(已下线)解密05 物质结构 元素周期律(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)
名校
4 . 锶元素的粒子结构示意图和在元素周期表中显示的信息如图所示:
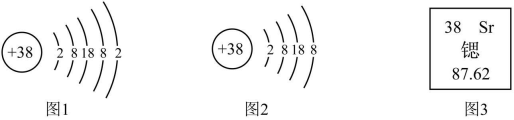
(1)锶属于___________ 元素(填“金属”或“非金属”)。
(2)锶元素的原子序数为___________ ,相对原子质量为___________ 。
(3)图2所表示的粒子的化学符号是___________ 。
(4)它与地壳中含量第一位的元素组成物质的化学式是___________ 。

(1)锶属于
(2)锶元素的原子序数为
(3)图2所表示的粒子的化学符号是
(4)它与地壳中含量第一位的元素组成物质的化学式是
您最近一年使用:0次
解题方法
5 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图 ,汞在第
,汞在第___ 周期。
(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是____ ,其中心原子杂化轨道类型:___ 。
(3)下列有关性质的比较能用元素周期律解释的是__ (填字母,下同)。
a.酸性:HCl>H2SO3
b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2
d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是___ 。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。
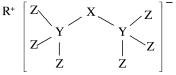
①R的元素符号为___ 。
②X的氢化物的电子式:___ 。
③写出Y的最高价氧化物的一种用途__ 。
(1)据汞的原子结构示意图
 ,汞在第
,汞在第(2)NH3、H2O、H2S分别为氮、氧、硫3种元素对应的氢化物,其中沸点最高的是
(3)下列有关性质的比较能用元素周期律解释的是
a.酸性:HCl>H2SO3
b.非金属性:O>S
c.碱性:NaOH>Mg(OH)2
d.热稳定性:Na2CO3>NaHCO3
(4)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断正确的是
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(5)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层电子数是Y核外电子数的一半。

①R的元素符号为
②X的氢化物的电子式:
③写出Y的最高价氧化物的一种用途
您最近一年使用:0次
6 . “天宫二号”使用的冷原子钟突破人类太空计时精度,三千万年误差小于1秒,攻克了冷原子钟超低噪声微波频率源等关键技术,制作该钟用到了铷。图甲为元素周期表的部分信息,图乙为铷原子的结构示意图。
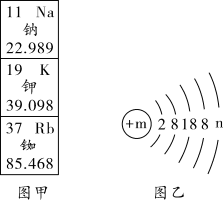
(1)钾的相对原子质量为___ 、质子数为__ 。
(2)乙图中m和n的数值分别为___ 、___ 。
(3)写出11号元素所形成离子的离子符号___ 。

(1)钾的相对原子质量为
(2)乙图中m和n的数值分别为
(3)写出11号元素所形成离子的离子符号
您最近一年使用:0次
名校
解题方法
7 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,如图是元素周期表的一部分,回答下列问题:
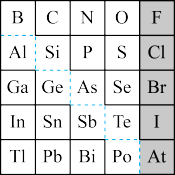
(1)元素Ga在元素周期表中的位置为:___ 。
(2)Sn的最高正价为___ ,Cl的最高价氧化物对应水化物的化学式为___ 。
(3)根据元素周期律,推断
①阴影部分元素形成的氢化物中热稳定性最高的是___ 。(写化学式)
②原子半径比较:N___ Si(填“>”、“<”、“=”或“无法比较”)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断
①阴影部分元素形成的氢化物中热稳定性最高的是
②原子半径比较:N
您最近一年使用:0次
8 . 完成下列问题
(1)默写化学元素周期表前20号元素。___________
(2)默写金属金属活动性顺序。__________
(1)默写化学元素周期表前20号元素。
(2)默写金属金属活动性顺序。
您最近一年使用:0次
名校
9 . 1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
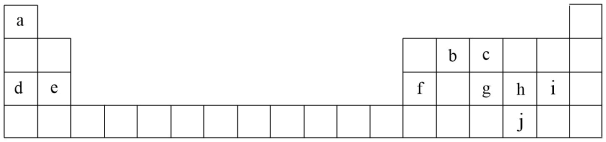
(1)元素c代表的元素是(写元素符号)_______
(2)请写出元素e在元素周期表中所在的位置_______
(3)请画出元素f的简单离子结构示意图_______ 。请写出单质f与d的最高价氧化物对应水化物的离子反应方程式_______ 。
(4)元素a和b能构成最简单的有机化合物(用结构式表示)_______ 。请写出元素a和b构成的最简单有机化合物与i单质发生的第一步化学反应方程式_______ 。
(5)元素h的最高价氧化物对应的水化物呈_______ (酸性、中性或碱性);请写出元素h的最高价氧化物对应的水化物与单质b的化学反应方程式_______ 。

(1)元素c代表的元素是(写元素符号)
(2)请写出元素e在元素周期表中所在的位置
(3)请画出元素f的简单离子结构示意图
(4)元素a和b能构成最简单的有机化合物(用结构式表示)
(5)元素h的最高价氧化物对应的水化物呈
您最近一年使用:0次
2021-09-29更新
|
573次组卷
|
2卷引用:广东省广州市仲元中学2020-2021学年高一下学期期中考试化学试题
名校
解题方法
10 . 有7种短周期元素,其原子半径及主要化合价如下:
完成下列填空:
(1)A在元素周期表中的位置是_______ 。
(2)上述7种元素形成的简单离子中,离子半径最大是_______ (用离子符号表示)
(3)甲是由G、H两种元素组成的18e-分子,用电子式表示其形成过程_______ 。
(4)用一个化学方程式表示E元素的非金属性比D强_______ 。
| 元素代号 | A | B | D | E | F | G | H |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
| 主要化合价 | +1 | +3 | +6,-2 | +7,-1 | +5,-3 | -2 | +1 |
完成下列填空:
(1)A在元素周期表中的位置是
(2)上述7种元素形成的简单离子中,离子半径最大是
(3)甲是由G、H两种元素组成的18e-分子,用电子式表示其形成过程
(4)用一个化学方程式表示E元素的非金属性比D强
您最近一年使用:0次



